Caso clínico: Hepatopatía grave tras la administración de rivaroxabán en un perro
Caso clínico: Hepatopatía grave tras la administración de rivaroxabán en un perro
 Allison P. Mosichuk
Allison P. Mosichuk  Candace Wimbish
Candace Wimbish  Kristen Poplawski
Kristen Poplawski , Adam Birkenheuer,
, Adam Birkenheuer,  Karyn Harrell
Karyn Harrell  Kursten V. Pierce*
Kursten V. Pierce*- Departamento de Ciencias Clínicas, Facultad de Medicina Veterinaria, Universidad Estatal de Carolina del Norte, Raleigh, Carolina del Norte, Estados Unidos
Se sabe que el rivaroxabán, un inhibidor específico del factor Xa y anticoagulante comúnmente utilizado, causa hepatotoxicidad e insuficiencia hepática en humanos. Aunque el rivaroxabán se utiliza con frecuencia en medicina veterinaria, no se ha informado previamente de hepatotoxicidad en perros. El presente informe de caso describe un perro que desarrolló hepatopatía grave después de la administración de rivaroxabán por un trombo grande de la arteria pulmonar derecha. Se estima que una perra mestiza esterilizada de 6 años de edad desarrolló anorexia y letargo 9 días después de comenzar la administración de rivaroxabán. Los análisis de laboratorio posteriores revelaron una hepatopatía hepatocelular grave y se suspendió el tratamiento con rivaroxabán. Los diagnósticos adicionales no revelaron una etiología subyacente, aunque la citología hepática podría ser compatible con una lesión tóxica. La hepatopatía y los signos clínicos mejoraron después de suspender el tratamiento con rivaroxabán. El tiempo de aparición, el tipo de hepatopatía y el tiempo de resolución fueron similares a los notificados para los casos humanos. Este caso proporciona un precedente para abogar por un seguimiento mejorado y más estrecho de los perros que reciben inhibidores del factor Xa. En los casos de sospecha de hepatotoxicidad sin otra causa identificable, se debe realizar un análisis de riesgo-beneficio y se debe considerar la interrupción de la administración de rivaroxabán o medicamentos anticoagulantes alternativos.
Introducción
El rivaroxabán es un inhibidor del factor Xa específico para humanos que se utiliza para la prevención y el tratamiento de la trombosis (1, 2). Los inhibidores del factor Xa se dirigen a la cascada de coagulación tanto en las vías intrínsecas como extrínsecas, lo que conduce a la reducción de la trombina y, en última instancia, a la formación de coágulos (3). El rivaroxabán inhibe competitivamente el factor Xa libre y unido a coágulos, además de inhibir la actividad de la protrombinasa, creando así un potente anticoagulante oral (4). En humanos, el rivaroxabán y otros inhibidores del factor Xa tienen muchas indicaciones aprobadas, incluida la reducción del accidente cerebrovascular en pacientes con fibrilación auricular, el tratamiento de la trombosis venosa profunda y la embolia pulmonar, y la profilaxis después de la cirugía (5). Aunque el rivaroxabán es un anticoagulante eficaz, se han notificado efectos adversos significativos, como hemorragia, malestar abdominal, dolor de espalda, anorexia, fiebre e insuficiencia hepática en humanos (3, 6-9).
El rivaroxabán se prescribe fuera de etiqueta para la anticoagulación tanto en perros como en gatos en medicina veterinaria (1, 10). Los pacientes con alto riesgo de trombosis incluyen perros con anemia hemolítica mediada por el sistema inmunitario (AIM), nefropatía perdedora de proteínas o enfermedad del gusano del corazón y felinos con miocardiopatía; Sin embargo, existen muchas otras afecciones en las que están indicados fármacos antitrombóticos (10-12). Si bien hay muchos anticoagulantes utilizados en medicina veterinaria, faltan recomendaciones basadas en la evidencia con respecto a protocolos de tratamiento específicos (13). En este momento, la dosis recomendada de rivaroxabán es de 1-2 mg/kg/día por vía oral en perros (13). El rivaroxabán parece ser seguro y bien tolerado en perros, y solo se han reportado hemorragias y vómitos leves como efectos adversos (1, 14, 15). Sin embargo, debe tenerse en cuenta que la evidencia de la seguridad y tolerancia general sigue siendo bastante limitada en pacientes veterinarios en comparación con los humanos debido al número limitado y al pequeño tamaño de las muestras de estos estudios. A diferencia de los seres humanos, la hepatotoxicidad por rivaroxabán aún no se ha notificado en perros.
El presente informe de caso describe un perro que desarrolló hepatopatía grave después de la administración de rivaroxabán. No se identificó ninguna otra causa incitante para la hepatopatía, que se resolvió después de la interrupción del rivaroxabán.
Presentación del caso
Una perra mestiza esterilizada de aproximadamente 6 años de edad (peso: 21 kg) se presentó al Servicio de Cardiología del Hospital Veterinario del Estado de Carolina del Norte para la evaluación de un soplo cardíaco de nueva aparición y cardiomegalia radiográfica generalizada (Día – 30; Figura 1). El soplo cardíaco fue reportado por primera vez por el veterinario principal del perro en una cita anual de bienestar 3 meses antes. En el momento de la presentación, el perro estaba asintomático. Había antecedentes de un episodio de disnea caracterizado por un esfuerzo espiratorio significativo y una frecuencia respiratoria normal (32 respiraciones por minuto) aproximadamente 2 meses antes. Este episodio se resolvió en 2 h sin tratamiento. El perro fue adoptado como adulto maduro aproximadamente 2 años antes con un historial médico previo desconocido. En el momento de la adopción, el perro dio positivo en la prueba de infección por gusano del corazón (Dirofilaria immitis) y exposición a Borrelia burgdorferi y Ehrlichia sp. (Ehrlichia canis, Ehrlichia ewingii o Ehrlichia chaffeensis). El perro fue tratado previamente en el momento de la adopción con un protocolo de tratamiento desconocido para el gusano del corazón y desde entonces dio negativo. El perro también fue tratado con doxiciclina (dosis y duración desconocidas) para las exposiciones a Borrelia y Ehrlichia.
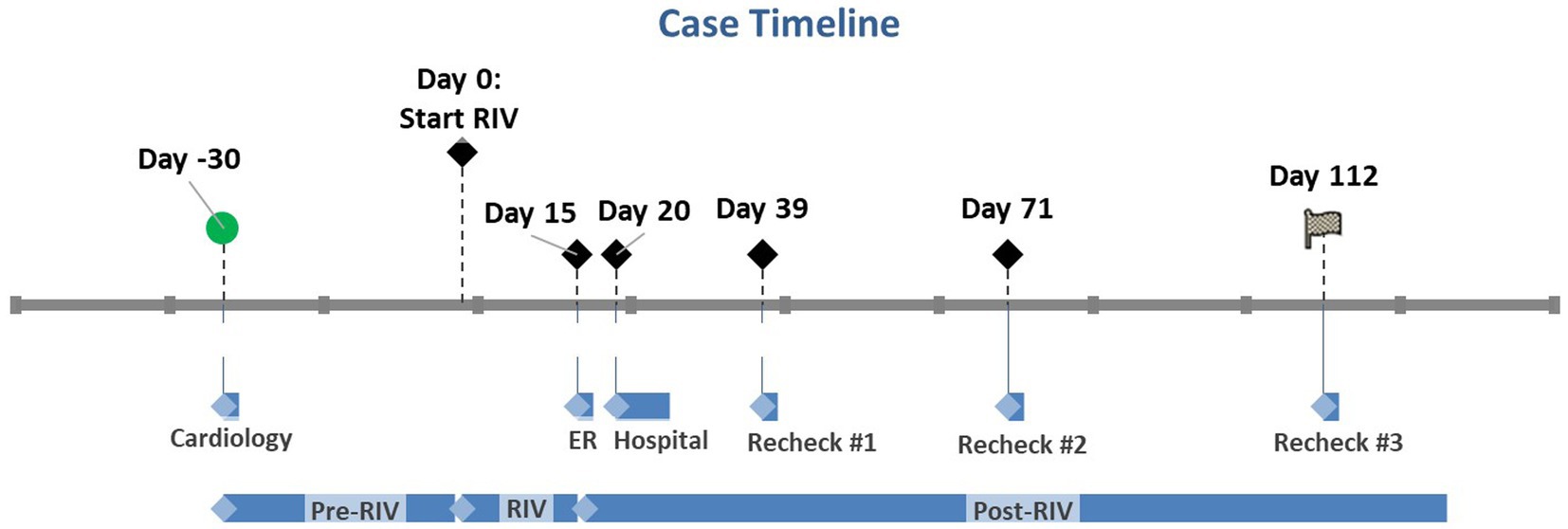 Figura 1. Cronología del caso en la que el día 0 marca el día en que se inició el rivaroxabán. El día 30 marca la cita inicial de cardiología del paciente. El día 15 marca la visita inicial a la sala de emergencias cuando se suspendió el rivaroxabán. Los días 20 a 27 marcan la estadía del paciente en el hospital. Los exámenes de revisión posteriores se marcan con los días 39, 71 y 112. RIV, Rivaroxaban.
Figura 1. Cronología del caso en la que el día 0 marca el día en que se inició el rivaroxabán. El día 30 marca la cita inicial de cardiología del paciente. El día 15 marca la visita inicial a la sala de emergencias cuando se suspendió el rivaroxabán. Los días 20 a 27 marcan la estadía del paciente en el hospital. Los exámenes de revisión posteriores se marcan con los días 39, 71 y 112. RIV, Rivaroxaban.
En el examen físico, se observó que el perro tenía un soplo cardíaco sistólico esternal derecho de grado II-III/VI. Se realizó un ecocardiograma que reveló agrandamiento moderado del ventrículo derecho, insuficiencia tricuspídea (TR) moderada e hipertensión pulmonar moderada (gradiente de presión TR ~60 mmHg). El hallazgo más significativo fue una estructura hiperecogénica de aproximadamente 1,5 cm por 5,5 cm dentro de la arteria pulmonar principal distal y la arteria pulmonar de la rama derecha (Figura 2A). Estos hallazgos ecocardiográficos dieron lugar a estudios adicionales que incluyeron análisis de laboratorio (hemograma completo, perfil químico sérico, análisis de orina, relación proteína/creatinina en orina y prueba IDEXX SNAP 4Dx Plus), tromboelastografía activada por caolín (TEG) y una tomografía computarizada (TC) torácica/abdominal anestesiada. Los hallazgos anormales de laboratorio incluyeron una alanina transaminasa ligeramente elevada (ALT 118 UI/L, RR 17-78 UI/L), proteinuria leve (tira reactiva de orina) e hipercolesterolemia leve (colesterol 498 mg/dL, RR 151-348 mg/dL) (Tabla 1). Se observó que el perro era persistentemente positivo para anticuerpos contra Borrelia burgdorferi y Ehrlichia sp. y negativo para anticuerpos contra el gusano del corazón. El TEG estaba dentro de los límites normales. En la TC se observó un extenso trombo arterial pulmonar derecho mineralizado y trombos parcialmente oclusivos en las arterias lobares media derecha, caudal derecha e izquierda (Figura 2B). Se sospechaba que la afección protrombótica subyacente era secundaria a su enfermedad del gusano del corazón diagnosticada previamente. A la luz de su tromboembolismo pulmonar (TEP) actual y para la prevención de TEP adicional, se le prescribió clopidogrel a la perra (1,8 mg/kg VO cada 24 h), con planes de iniciar rivaroxabán (0,5 mg/kg VO cada 12 h).
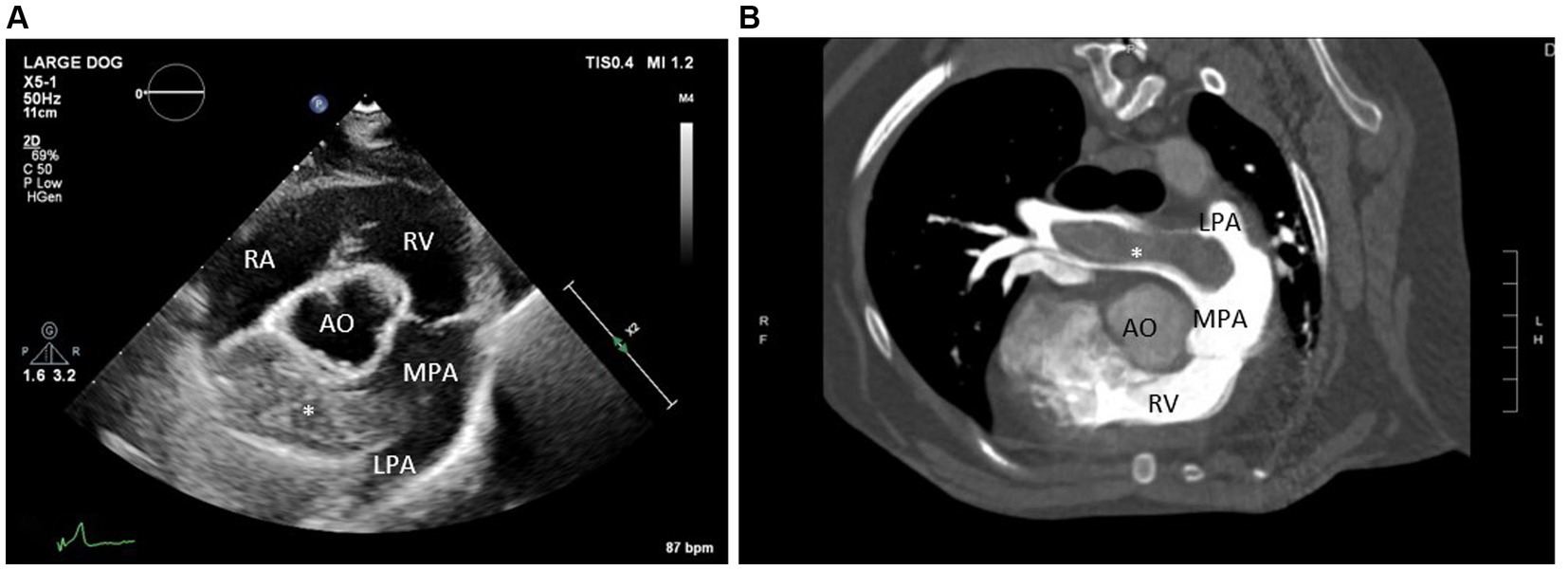 Figura 2. (A) Imagen de ecocardiograma (vista del eje corto paraesternal derecho a nivel de la arteria pulmonar) y (B) imágenes de tomografía computarizada (vista transversal) que identifican un trombo grande dentro de la arteria pulmonar de la rama derecha. AR: aurícula derecha; VD: ventrículo derecho; MPA: Arteria pulmonar principal; AO: Aorta; LPA: Rama izquierda de la arteria pulmonar; trombo grande en la rama derecha de la arteria pulmonar.*
Figura 2. (A) Imagen de ecocardiograma (vista del eje corto paraesternal derecho a nivel de la arteria pulmonar) y (B) imágenes de tomografía computarizada (vista transversal) que identifican un trombo grande dentro de la arteria pulmonar de la rama derecha. AR: aurícula derecha; VD: ventrículo derecho; MPA: Arteria pulmonar principal; AO: Aorta; LPA: Rama izquierda de la arteria pulmonar; trombo grande en la rama derecha de la arteria pulmonar.*
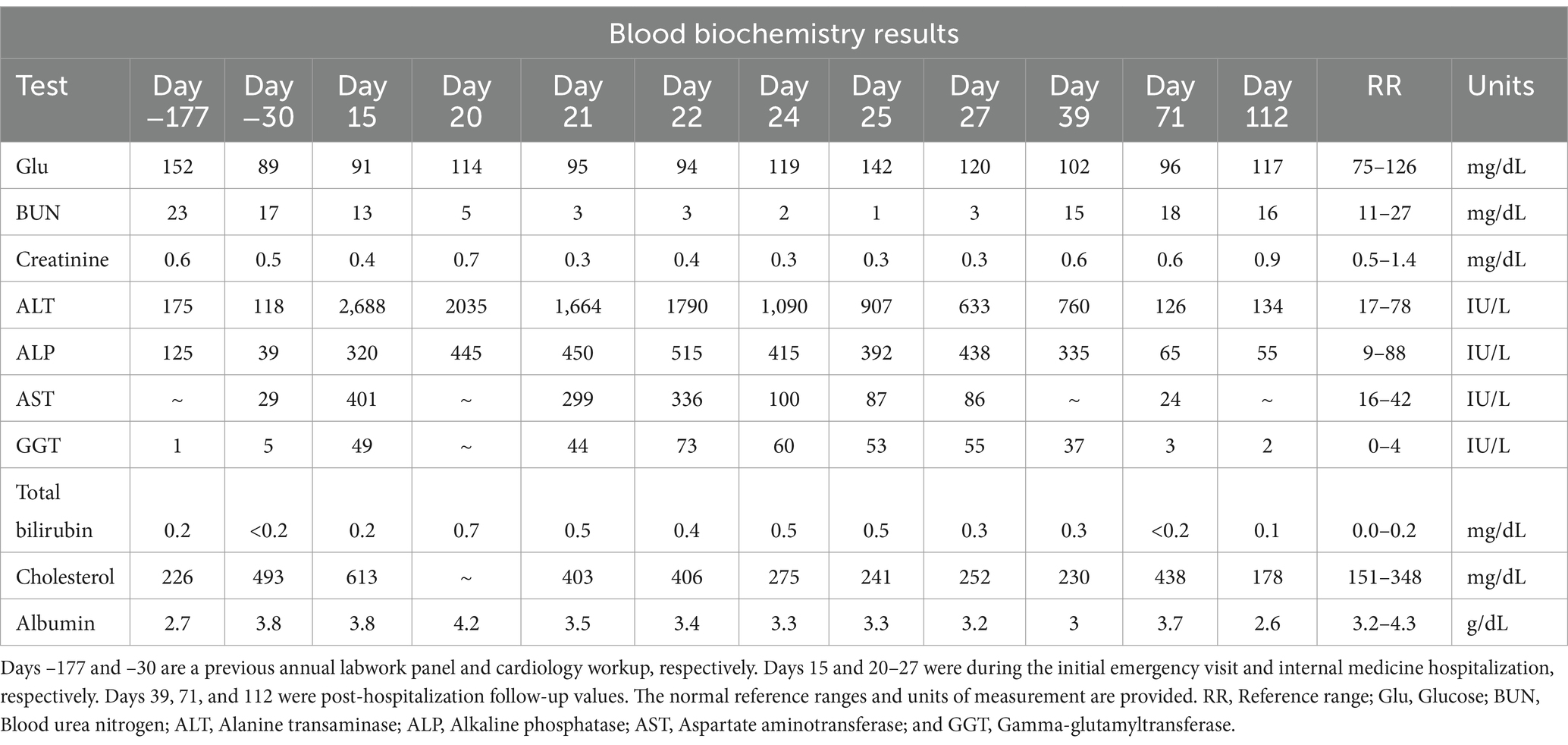 Tabla 1. Resultados seriados de bioquímica sérica, siendo el día 0 cuando se inició el tratamiento con rivaroxabán.
Tabla 1. Resultados seriados de bioquímica sérica, siendo el día 0 cuando se inició el tratamiento con rivaroxabán.
Tres días después de comenzar a tomar clopidogrel (Día 27), el perro desarrolló diarrea severa y persistente que era refractaria al tratamiento médico con una dieta blanda y probióticos. El clopidogrel se suspendió después de un total de siete dosis, y la diarrea mejoró significativamente aproximadamente 36 h después. Después de 7 días, el perro fue probado con una dosis reducida (0,9 mg/kg VO cada 24 h) de clopidogrel; sin embargo, volvió a desarrollar diarrea significativa 4 días después. En ese momento, el clopidogrel se suspendió definitivamente (Día – 7). No se obtuvieron datos de laboratorio durante este tiempo. El rivaroxabán aún no se había iniciado debido a un retraso en la recepción del medicamento por parte del propietario. A la perra se le administró la primera dosis (0,5 mg/kg VO cada 12 h) de rivaroxabán 30 días después de su presentación inicial en el servicio de cardiología y 7 días después de su dosis final de clopidogrel (Día 0; Figura 1).
En la revisión programada 5 días después de comenzar con rivaroxabán (día 5), el perro estaba bien en casa, sin signos respiratorios recurrentes, diarrea resuelta y sin efectos adversos observados. El ecocardiograma de esta visita reveló hallazgos similares en comparación con su visita anterior (tamaño estático del trombo de la arteria pulmonar derecha). Se recomendó la administración continuada de rivaroxabán a la misma dosis, y se programó una nueva revisión en el perro en 2 meses.
El perro fue representado a través del Servicio de Emergencia de Animales Pequeños del Hospital Veterinario del Estado de Carolina del Norte 10 días después de la visita de revisión de cardiología por hiporexia progresiva y letargo (Día 15; Figura 1). Estos signos habían comenzado aproximadamente 6 días antes (día 9) después de que el perro hubiera recibido 19 dosis totales de rivaroxabán. Su examen físico se mantuvo sin cambios. Se realizaron análisis de laboratorio (hemograma completo y perfil químico sérico), que revelaron una hepatopatía grave, principalmente hepatocelular, caracterizada por una elevación grave de la ALT a 2.688 UI/L (RR 17-78 UI/L; Tabla 1). Un radiólogo certificado realizó una ecografía abdominal, que se encontraba dentro de los límites normales y no se visualizaron anomalías informadas. La atención ambulatoria fue elegida por el propietario. La perra comenzó a tomar maropitant (2 mg/kg VO cada 24 h) y se suspendió su tratamiento con rivaroxabán debido a la preocupación por la hepatotoxicidad inducida por rivaroxabán. Maropitant se administró para el tratamiento preventivo y la prevención de las náuseas, el alivio del dolor visceral y con la esperanza de mejorar la ingesta de alimentos.
La perra permaneció anoréxica en casa y fue representada a través del Servicio de Emergencia de Animales Pequeños del Hospital Veterinario del Estado de Carolina del Norte 5 días después de la visita de emergencia anterior (Día 20; Figura 1). No se informaron signos clínicos adicionales. La repetición de los análisis de laboratorio mostró una hepatopatía estática (ALT 2035 UI/L; bilirrubina total 0,7 mg/dL, Tabla 1). El perro fue hospitalizado y trasladado al Servicio de Medicina Interna del Hospital Veterinario del Estado de Carolina del Norte a la mañana siguiente. El perro estuvo hospitalizado durante 7 días (días 21-27). Se realizaron perfiles químicos séricos repetidos durante la hospitalización (Tabla 1).
Se realizaron diagnósticos adicionales durante la hospitalización del perro, incluido un perfil de coagulación, TEG, ácidos biliares, amoníaco, ecografía hepática repetida, citología hepática/biliar, cultivo de bilis y serología y PCR de leptospirosis. El perfil de coagulación y el TEG fueron compatibles con trombocitopenia leve sin evidencia de hipercoagulabilidad. Los ácidos biliares preprandiales y el amoníaco se encontraban dentro de los límites normales. La repetición de la ecografía abdominal continuó sin mostrar cambios significativos en el hígado y se realizaron aspirados del parénquima hepático y de la bilis de la vesícula biliar. La muestra de bilis no presentaba signos citológicos de importancia. La citología hepática, realizada por un patólogo clínico certificado, mostró atipia hepatocelular con cambio vacuolar de glucógeno, más consistente con lesión por toxina, neoplasia hepática o regeneración. No se reportó crecimiento en el cultivo de bilis. La serología de leptospirosis y la PCR no fueron compatibles con infección actual o previa.
Durante la estancia hospitalaria de la perra, se mantuvo con 50 mL/kg/día de NaCl al 0,45% con aditivo KCl por vía intravenosa. El perro recibió ondansetrón (0,5 mg/kg IV cada 8 h), maropitant (1 mg/kg IV cada 24 h) y caprorodilina (3 mg/kg VO cada 24 h) para las náuseas, la prevención de los vómitos, el beneficio potencial de aliviar el dolor visceral y la estimulación del apetito, respectivamente. El perro comenzó con N-acetilcisteína (dosis de carga intravenosa de 140 mg/kg, luego 70 mg/kg IV cada 6 h) y ursodiol (5 mg/kg VO cada 12 h) para el apoyo hepático. Tras obtener los resultados del aspirado hepático y biliar, se inició el tratamiento con enrofloxacino (10 mg/kg IV cada 24 h) y ampicilina/sulbactam (30 mg/kg IV cada 8 h) al cuarto y quinto día de hospitalización, respectivamente (días 24 y 25). Debido a la persistencia de la anorexia a pesar del tratamiento antiemuseante actual, se aumentó la dosis de ondansetrón (1 mg/kg IV cada 8 h) y se inició una CRI de metoclopramida (dosis de carga intravenosa de 1 mg/kg y luego dosis intravenosa de 2 mg/kg/día IV).
Con el tiempo, los valores hepáticos mejoraron (Tabla 1); sin embargo, la perra continuó siendo anoréxica. Se colocó una sonda nasogástrica y se toleró la alimentación por sonda. El apetito de la perra mejoró lentamente y, al descargarse, comía pequeñas cantidades. En el momento del alta, al séptimo día de hospitalización, los valores hepáticos habían mejorado significativamente (ALT 600; bilirrubina total 0,3; Tabla 1). El perro fue dado de alta con trazodona, gabapentina, ondansetrón, denamarina, mirtazapina y amoxicilina/clavulanato. El apetito del perro comenzó a mejorar en casa; sin embargo, el propietario no pudo administrar ninguno de los medicamentos recetados. Repetir el análisis de laboratorio con su veterinario de atención primaria la semana después del alta mostró valores estáticos a levemente mejorados (Día 39; Figura 1; Tabla 1).
El perro regresó al Servicio de Cardiología del Hospital Veterinario del Estado de Carolina del Norte el día 71 para un ecocardiograma de revisión (Figura 1). Su apetito había mejorado significativamente y, por lo demás, estaba bien. Un perfil químico sérico mostró una mejoría significativa de los valores hepáticos (Tabla 1). Su ecocardiograma era estático de sus imágenes previas.
Los análisis de laboratorio realizados el día 112 revelaron que los valores hepáticos habían vuelto a la línea de base (Figura 1; Tabla 1). Desafortunadamente, el perro desarrolló insuficiencia cardíaca congestiva del lado derecho secundaria a hipertensión pulmonar progresiva, que actualmente se encuentra bajo tratamiento médico con furosemida, pimobendán y espironolactona.
Discusión
El rivaroxabán, un inhibidor oral del factor Xa específico para humanos, se utiliza en perros con un estado de hipercoagulabilidad debido a una serie de etiologías subyacentes (1, 11, 12). Sobre la base de los estudios actuales y la experiencia clínica, el rivaroxabán parece ser seguro y eficaz en perros, con efectos adversos mínimos informados (1, 14, 16). Sin embargo, se necesitan investigaciones adicionales, ensayos controlados y/o informes de farmacovigilancia debido al número limitado de estudios y a las limitaciones del tamaño de la muestra que existen en la literatura veterinaria actual. Los efectos adversos reportados en perros incluyen sangrado leve y vómitos (14). A pesar de los numerosos informes de hepatotoxicidad en humanos después de la administración de rivaroxabán y otros inhibidores del factor Xa, aún no se han reportado hallazgos similares en medicina veterinaria (6-8, 17-19). Es importante tener en cuenta que, aunque existen informes en la literatura médica humana, la hepatotoxicidad inducida por el factor Xa es un evento relativamente raro.
Actualmente se desconoce el mecanismo exacto de lesión secundaria a la terapia con rivaroxabán en humanos, aunque se han propuesto mecanismos de toxicidad directa, idiosincrásicos e inmunológicos (6, 9, 20). En humanos con hepatotoxicidad aguda por rivaroxabán, las hepatopatías hepatocelulares son las más frecuentes, aunque también se han descrito hepatopatías colestásicas y mixtas (6, 7, 21). En un estudio, hasta el 55% de los casos de hepatotoxicidad inducida por factor Xa se caracterizaron como hepatocelulares (7). El perro en este informe desarrolló una hepatopatía grave, principalmente hepatocelular, con hallazgos citológicos consistentes con lesiones tóxicas. En estudios con humanos, la elevación de la bilirrubina sérica total también se observa con frecuencia en los casos de hepatotoxicidad inducida por rivaroxabán (7, 21, 22). Aunque leve, la bilirrubina total del perro reportado se elevó levemente junto con la hepatopatía, que mejoró después de la interrupción del rivaroxabán.
El perro en este informe desarrolló una hepatopatía que se observó por primera vez en un análisis de laboratorio 15 días después de comenzar a tomar rivaroxabán. Los signos clínicos de anorexia y letargo comenzaron aproximadamente 6 días antes (día 9). Licata et al. (7) informaron que el tiempo entre el inicio del tratamiento y el inicio de la lesión hepática osciló entre 2 y 180 días, con una mediana de aproximadamente 15 días, lo que coincide con nuestro caso. El indicador más específico de una hepatopatía causada por la administración de rivaroxabán es la mejoría después de la interrupción del fármaco. (6, 23, 24). Si bien los datos prospectivos sobre el tiempo hasta la resolución de los trastornos del trabajo de laboratorio son limitados, múltiples informes de casos señalan una mejoría significativa en las enzimas hepáticas de 2 a 4 semanas después de suspender el rivaroxabán (6, 22 a 25). En el perro reportado, la hepatopatía se resolvió completamente 8 semanas después de suspender el rivaroxabán; sin embargo, se documentó una mejoría significativa a las 4 semanas. No se puede excluir por completo la posibilidad de que una hepatopatía subclínica preexistente altere el metabolismo y el proceso de eliminación de este fármaco, lo que resulta en una mayor propensión a la hepatotoxicidad.
Si bien todos los inhibidores del factor Xa han sido implicados en casos de hepatotoxicidad, el rivaroxabán puede ser el más común, según estudios recientes (6, 18, 19, 21, 22, 26). Un informe de caso observó una mejoría de la hepatopatía grave después de la interrupción de rivaroxabán y el inicio de apixabán, un inhibidor similar del factor Xa (22). Otro informe mostró hallazgos similares al cambiar al paciente de rivaroxabán a tinzaparina (27). Debido a la falta de datos generales sobre el uso de inhibidores del factor Xa en medicina veterinaria, no se sabe con certeza si los pacientes que experimentan hepatotoxicidad inducida por rivaroxabán podrían tolerar otro fármaco de esta clase. Cambiar a los perros afectados a un inhibidor del factor Xa diferente puede ser una opción de tratamiento alternativa válida. En este caso, después de discutirlo con el cliente, se optó por no seguir una terapia antitromba alternativa dado que no había evidencia diagnóstica de que el perro se encontrara actualmente en un estado de hipercoagulabilidad, y el propietario se mostró reacio debido a la preocupación por el desarrollo de posibles efectos secundarios adversos.
Si bien la hepatotoxicidad secundaria a rivaroxabán se priorizó como el diferencial más probable para este perro, no se pueden excluir por completo otras etiologías. A esta perra se le administraron antibióticos durante su hospitalización, lo que podría haber contribuido a una mejora de las enzimas hepáticas en el caso de que las elevaciones fueran secundarias a hepatitis bacteriana o colangiohepatitis. Vale la pena señalar que las enzimas hepáticas del perro habían comenzado a mejorar antes de comenzar cualquier terapia, incluidos los antibióticos, y no se observó evidencia de infección en la citología o el cultivo. La perra continuó mejorando en casa a pesar de que su dueño suspendió todos los medicamentos, lo que puede respaldar aún más el presunto diagnóstico de hepatotoxicidad inducida por rivaroxabán. Si bien no se observó ni se informó ninguna exposición adicional a toxinas, no se puede descartar por completo. Idealmente, se habrían realizado diagnósticos adicionales, incluida una biopsia hepática, para respaldar aún más este diagnóstico. Desafortunadamente, esto no se percibió como clínicamente indicado debido a la mejoría del paciente y tampoco era financieramente factible para el propietario.
Aunque no es el enfoque principal de este informe de caso, es clínicamente importante reconocer que la polifarmacia puede aumentar el riesgo de interacciones medicamentosas (28) y que el maropitant puede prescribirse en exceso en medicina veterinaria para perros que carecen de signos gastrointestinales manifiestos (29). La utilidad y seguridad de cada intervención terapéutica y farmacológica debe considerarse cuidadosamente.
Conclusión
Según el conocimiento del autor, este es el primer informe de caso de sospecha de hepatotoxicidad inducida por rivaroxabán en un perro. Este caso proporciona un precedente para abogar por un seguimiento mejorado y más estrecho de los perros que reciben inhibidores del factor Xa. Los perros tratados con rivaroxabán deben ser monitorizados para detectar signos clínicos y cambios en los análisis de laboratorio compatibles con hepatotoxicidad. En los casos de sospecha de hepatotoxicidad sin otra causa identificable, se debe realizar un análisis de riesgo-beneficio y se debe considerar la interrupción de la administración de rivaroxabán o medicamentos antitrombóticos alternativos.
Declaración de disponibilidad de datos
Las contribuciones originales presentadas en el estudio se incluyen en el artículo/material complementario, las consultas adicionales pueden dirigirse al autor correspondiente.
Declaración ética
Se obtuvo el consentimiento informado por escrito del propietario del perro para la publicación de este informe de caso.
Contribuciones de los autores
AM: Conceptualización, Curación de datos, Análisis formal, Investigación, Metodología, Administración de proyectos, Recursos, Software, Validación, Visualización, Redacción – borrador original, Redacción – revisión y edición. CW: Conceptualización, Curación de datos, Análisis formal, Investigación, Metodología, Administración de proyectos, Recursos, Software, Supervisión, Validación, Visualización, Redacción – borrador original, Redacción – revisión y edición. KP: Conceptualización, Curación de datos, Análisis formal, Investigación, Metodología, Administración de proyectos, Recursos, Software, Supervisión, Validación, Visualización, Redacción – borrador original, Redacción – revisión y edición. AB: Conceptualización, Curación de datos, Análisis formal, Investigación, Metodología, Administración de proyectos, Recursos, Software, Supervisión, Validación, Visualización, Redacción – borrador original, Redacción – revisión y edición. KH: Conceptualización, Curación de datos, Análisis formal, Investigación, Metodología, Administración de proyectos, Recursos, Software, Supervisión, Validación, Visualización, Redacción – borrador original, Redacción – revisión y edición. KVP: Conceptualización, Curación de datos, Análisis formal, Investigación, Metodología, Administración de proyectos, Recursos, Software, Supervisión, Validación, Visualización, Redacción – borrador original, Redacción – revisión y edición.
Financiación
El/los autor/es declaran/n que no se recibió apoyo financiero para la investigación, autoría y/o publicación de este artículo.
Conflicto de intereses
Los autores declaran que la investigación se llevó a cabo en ausencia de relaciones comerciales o financieras que pudieran interpretarse como un posible conflicto de intereses.
Nota del editor
Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, ni las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo, o afirmación que pueda ser hecha por su fabricante, no está garantizado ni respaldado por el editor.
Referencias
1. Conversy, B, Blais, MC, Dunn, M, Gara-Boivin, C, y Del Castillo, JRE. Actividad anticoagulante del rivaroxabán oral en perros sanos. Veterinario J. (2017) 223:5–11. doi: 10.1016/j.tvjl.2017.03.006
Resumen de PubMed | Texto completo de Crossref | Google Académico
2. Kvasnicka, T, Malikova, I, Zenahlikova, Z, Kettnerova, K, Brzezkova, R, Zima, T, et al. Rivaroxabán: metabolismo, propiedades farmacológicas e interacciones medicamentosas. Curr Drug Metab. (2017) 18:636–42. doi: 10.2174/1389200218666170518165443
Resumen de PubMed | Texto completo de Crossref | Google Académico
3. Turpie, S.A. Inhibidores orales directos del factor Xa en desarrollo para la prevención y tratamiento de enfermedades tromboembólicas. Arterioscler Tromb Vasc Biol. (2007) 27:1238–47. doi: 10.1161/ATVBAHA.107.139402
Resumen de PubMed | Texto completo de Crossref | Google Académico
4. Samama, MM. El mecanismo de acción de rivaroxabán, un inhibidor directo del factor Xa oral, en comparación con otros anticoagulantes. Res. de trombos. (2011) 127:497–504. doi: 10.1016/j.thromres.2010.09.008
Resumen de PubMed | Texto completo de Crossref | Google Académico
5. McCarty, D, y Robinson, A. Inhibidores del factor Xa: una nueva clase terapéutica para el tratamiento de la fibrilación auricular no valvular. Ther Adv Cardiovasc Dis. (2016) 10:37–49. doi: 10.1177/1753944715605011
Resumen de PubMed | Texto completo de Crossref | Google Académico
6. Liakoni, E, Rätz Bravo, AE y Krähenbühl, S. Hepatotoxicidad de los nuevos anticoagulantes orales (NOAC). Droga Saf. (2015) 38:711–20. doi: 10.1007/s40264-015-0317-5
Resumen de PubMed | Texto completo de Crossref | Google Académico
7. Licata, A, Puccia, F, Lombardo, V, Serruto, A, Minissale, MG, Morreale, I, et al. Hepatotoxicidad inducida por rivaroxabán: revisión de la literatura y reporte de nuevos casos. Eur J Gastroenterol Hepatol. (2018) 30:226–32. doi: 10.1097/MEG.000000000000001030
Resumen de PubMed | Texto completo de Crossref | Google Académico
8. Caldeira, D, Barra, M, Santos, AT, de Abreu, D, Pinto, FJ, Ferreira, JJ, et al. Riesgo de lesión hepática inducida por fármacos con los nuevos anticoagulantes orales: revisión sistemática y metaanálisis. Corazón. (2014) 100:550–6. doi: 10.1136/heartjnl-2013-305288
Resumen de PubMed | Texto completo de Crossref | Google Académico
9. LiverTox (2012). Información clínica y de investigación sobre la lesión hepática inducida por fármacos. Bethesda (MD): Instituto Nacional de Diabetes y Enfermedades Digestivas y Renales.
10. deLaforcade, A, Bacek, L, Blais, MC, Goggs, R, Lynch, A, y Rozanski, E. Consenso sobre el uso racional de antitrombóticos en cuidados críticos veterinarios (CURATIVO): dominio 1 que define poblaciones en riesgo. J Vet Emerg Crit Care. (2019) 29:37–48. doi: 10.1111/vec.12797
Resumen de PubMed | Texto completo de Crossref | Google Académico
11. deLaforcade, A, Bacek, L, Blais, MC, Boyd, C, Brainard, BM, Chan, DL, et al. Actualización de 2022 del consenso sobre el uso racional de antitrombóticos y trombolíticos en cuidados críticos veterinarios (CURATIVO) que define el dominio 1 de las poblaciones en riesgo. J Vet Emerg Crit Care. (2022) 32:289–314. doi: 10.1111/vec.13204
12. Goggs, R, Bacek, L, Bianco, D, Koenigshof, A, y Li, RHL. Consenso sobre el uso racional de los antitrombóticos en cuidados críticos veterinarios (CURATIVO): dominio 2 que define el uso terapéutico racional. J Vet Emerg Crit Care. (2019) 29:49–59. doi: 10.1111/vec.12791
Resumen de PubMed | Texto completo de Crossref | Google Académico
13. Blais, MC, Bianco, D, Goggs, R, Lynch, AM, Palmer, L, Ralph, A, et al. Consenso sobre el uso racional de los antitrombóticos en cuidados críticos veterinarios (CURATIVO): dominio 3 definitorio de protocolos antitrombóticos. J Vet Emerg Crit Care. (2019) 29:60–74. doi: 10.1111/vec.12795
Resumen de PubMed | Texto completo de Crossref | Google Académico
14. Sharp, CR, deLaforcade, AM, Koenigshof, AM, Lynch, AM, y Thomason, JM. Consenso sobre el uso racional de los antitrombóticos en cuidados críticos veterinarios (CURATIVO): dominio 4-refinamiento y monitorización de las terapias antitrombóticas. J Vet Emerg Crit Care. (2019) 29:75–87. doi: 10.1111/vec.12794
Resumen de PubMed | Texto completo de Crossref | Google Académico
15. Evans, LA, Tansey, C, Wiebe, M, Sloan, CQ, Patlogar, JE, Northcutt, S, et al. Evaluación prospectiva de rivaroxabán sobre parámetros hemostáticos en perros aparentemente sanos. Vet Med Sci. (2019) 5:317–24. doi: 10.1002/vms3.161
Resumen de PubMed | Texto completo de Crossref | Google Académico
16. Tracy, AL, Goggs, R, Brooks, MB, y Lynch, AM. Características clínicas y seguimiento posttratamiento de perros a los que se les administró rivaroxabán (2018-2020): 19 casos. J Vet Emerg Crit Care. (2022) 32:629–36. doi: 10.1111/vec.13199
Resumen de PubMed | Texto completo de Crossref | Google Académico
17. Russmann, S, Niedrig, DF, Budmiger, M, Schmidt, C, Stieger, B, Hürlimann, S, et al. Riesgo de lesión hepática después de la comercialización de rivaroxabán. J Hepatol. (2014) 61:293–300. doi: 10.1016/j.jhep.2014.03.026
Resumen de PubMed | Texto completo de Crossref | Google Académico
18. Björnsson, HK, Gudmundsson, DO, y Björnsson, ES. Lesión hepática causada por anticoagulantes orales: un estudio de cohorte retrospectivo basado en la población. Hígado Int. (2020) 40:1895–900. doi: 10.1111/liv.14559
Resumen de PubMed | Texto completo de Crossref | Google Académico
19. Raschi, E, Poluzzi, E, Koci, A, Salvo, F, Pariente, A, Biselli, M, et al. Lesión hepática con nuevos anticoagulantes orales: evaluación de los informes posteriores a la comercialización en el sistema de notificación de eventos adversos de la Administración de Alimentos y Medicamentos de EE. UU. Hno. J Clin Pharmacol. (2015) 80:285–93. doi: 10.1111/bcp.12611
Resumen de PubMed | Texto completo de Crossref | Google Académico
20. Peverelle, M, Asadi, K, and Sinclair, M. Drug-induced liver failure due to rivaroxaban. Ann Hematol. (2018) 97:2267–8. doi: 10.1007/s00277-018-3364-z
21. Watkins, PB, Desai, M, Berkowitz, SD, Peters, G, Horsmans, Y, Larrey, D, et al. Evaluation of drug-induced serious hepatotoxicity (eDISH): application of this data organization approach to phase III clinical trials of rivaroxaban after total hip or knee replacement surgery. Drug Saf. (2011) 34:243–52. doi: 10.2165/11586600-000000000-00000
Resumen de PubMed | Texto completo de Crossref | Google Académico
22. Anastasia, EJ, Rosenstein, RS, Bergsman, JA, y Parra, D. Uso de apixabán después del desarrollo de sospecha de esteatosis hepática inducida por rivaroxabán; A simple vista. Fibrinólisis de coágulos sanguíneos. (2015) 26:699–702. doi: 10.1097/MBC.00000000000000363
23. Lambert, A, Cordeanu, M, Gaertner, S, Nouri, S, Alt, M y Stephan, D. Lesión hepática inducida por rivaroxabán: resultados de un registro de tromboembolismo venoso. Int J Cardiol. (2015) 191:265–6. doi: 10.1016/j.ijcard.2015.04.248
Resumen de PubMed | Texto completo de Crossref | Google Académico
24. Liakoni, E, Rätz Bravo, AE, Terracciano, L, Heim, M, y Krähenbühl, S. Lesión hepática hepatocelular sintomática con hiperbilirrubinemia en dos pacientes tratados con rivaroxabán. Médico Pasante de JAMA. (2014) 174:1683–6. doi: 10.1001/jamainternmed.2014.3912
Resumen de PubMed | Texto completo de Crossref | Google Académico
25. Barrett, P, Vuppalanchi, R, Masuoka, H y Chalasani, N. Lesión cutánea y hepática grave inducida por fármacos por rivaroxabán. Dig Dis Sci. (2015) 60:1856–8. doi: 10.1007/s10620-014-3504-9
Resumen de PubMed | Texto completo de Crossref | Google Académico
26. Alonso, A, MacLehose, RF, Chen, LY, Bengtson, LG, Chamberlain, AM, Norby, FL, et al. Estudio prospectivo de anticoagulantes orales y riesgo de lesión hepática en pacientes con fibrilación auricular. Corazón. (2017) 103:834–9. doi: 10.1136/heartjnl-2016-310586
Resumen de PubMed | Texto completo de Crossref | Google Académico
27. Marrinan, A, Shackleton, L, Kelly, C, Lavin, M, Glavey, S, Murphy, P, et al. Lesión hepática durante el tratamiento con rivaroxabán en un paciente con amiloidosis AL. Eur J Clin Pharmacol. (2021) 77:1073–6. doi: 10.1007/s00228-020-03084-8
Resumen de PubMed | Texto completo de Crossref | Google Académico
28. Georgiev, KD, Hvarchanova, N, Stoychev, E, y Kanazirev, B. Prevalencia de polifarmacia y riesgo de posibles interacciones farmacológicas entre pacientes hospitalizados con énfasis en la farmacocinética. Sci Prog. (2022) 105:003685042110701. doi: 10.1177/00368504211070183
Resumen de PubMed | Texto completo de Crossref | Google Académico
29. McCormack, R, Olley, L, Glanemann, B, y Swann, JW. Estudio observacional prospectivo del uso de omeprazol y citrato maropitante en la atención veterinaria especializada. Sci Rep. (2020) 10:15727. doi: 10.1038/s41598-020-72950-3
Resumen de PubMed | Texto completo de Crossref | Google Académico
Palabras clave: rivaroxabán, hepatopatía, canino, anticoagulante, inhibidor del factor Xa
Cita: Mosichuk AP, Wimbish C, Poplawski K, Birkenheuer A, Harrell K y Pierce KV (2024) Reporte de caso: Hepatopatía grave tras la administración de rivaroxabán en un perro. Frente. Vet. Sci. 11:1364677. doi: 10.3389/fvets.2024.1364677
Recibido: 02 de enero de 2024; Aceptado: 06 de marzo de 2024;
Publicado: 04 Abril 2024.
Editado por:
Benito Soto-Blanco, Universidad Federal de Minas Gerais, Brasil
Revisado por:
Philippe Jacques Berny, VetAgro Sup, Francia
Kristin Zersen, Universidad Estatal de Colorado, Estados Unidos
Derechos de autor © 2024 Mosichuk, Wimbish, Poplawski, Birkenheuer, Harrell y Pierce. Este es un artículo de acceso abierto distribuido bajo los términos de la Licencia Creative Commons Attribution License (CC BY).
*Correspondencia: Kursten V. Pierce, kvpierce@ncsu.edu
Renuncia: Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, ni las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo o afirmación que pueda hacer su fabricante no está garantizado ni respaldado por el editor.
Date de alta y recibe nuestro 👉🏼 Diario Digital AXÓN INFORMAVET ONE HEALTH
Date de alta y recibe nuestro 👉🏼 Boletín Digital de Foro Agro Ganadero
Noticias animales de compañía
Noticias animales de producción
Trabajos técnicos animales de producción
Trabajos técnicos animales de compañía


