Cuidar al ternero recién nacido

Cuidar al ternero recién nacido
- Nicola Gladden analiza la importancia de una buena atención posparto, incluido el uso de analgesia y la provisión de calostro.
El parto puede ser un momento difícil tanto para la vaca como para el ternero.
El buen cuidado neonatal de la pantorrilla puede evitar que ocurran problemas y establecer una base de buena salud que tendrá un efecto beneficioso duradero en la pantorrilla.
Parto
Los animales deben alojarse en un ambiente seco y limpio para el parto, que puede estar en un corral grupal o en corrales de parto individuales (Figura 1).
Si los animales se mueven en el período previo al parto inmediato, es importante que el movimiento se sincronice adecuadamente para evitar aumentar inadvertidamente la probabilidad de distocia1.
Se sabe que la distocia se asocia con un mayor riesgo de muerte fetal en el ganado y se asocia con una menor probabilidad de supervivencia en los terneros que aún no han nacido2-10.
Un parto bien manejado puede, por lo tanto, ayudar mucho al ternero en sus primeros días o semanas de vida, en comparación con un parto mal manejado de manera inadecuada, lo que puede provocar la muerte del ternero o el parto de un ternero que carece del vigor requerido para la supervivencia.
Valoración del vigor neonatal de la pantorrilla
En los bebés, el vigor del recién nacido se evalúa utilizando un sistema de puntuación desarrollado hace más de 60 años por Virginia Apgar; Este sistema ahora se conoce como el puntaje APGAR (Apariencia, Pulso, Mueca, Actividad, Respiración) 11,12.
La puntuación APGAR se ha adaptado para su uso en especies veterinarias y evalúa la frecuencia cardíaca, el esfuerzo respiratorio, los reflejos, la motilidad y el color de la membrana mucosa. Los puntajes más bajos están asociados con una vigilancia más pobre 13-18.
Este sistema de puntuación es simple y no requiere equipo especializado; sin embargo, en una situación de granja ocupada, puede ser lento y laborioso para un agricultor evaluar y calificar cinco parámetros diferentes para cada ternero nacido.
El trabajo en terneros ha demostrado que la evaluación del reflejo de amamantamiento, en combinación con el grado de dificultad de parto que experimentan los terneros recién nacidos, es una herramienta simple, rápida y efectiva para evaluar la vitalidad de los terneros recién nacidos que puede ser más adecuada para su uso en un entorno de granja comercial19.
La evaluación del vigor con esta herramienta se puede utilizar para determinar cómo se debe manejar la pantorrilla en el período posparto para optimizar el potencial de un comienzo saludable de la vida.
Colocar la pantorrilla en esta posición es contraproducente ya que resulta en un movimiento craneal de las vísceras abdominales debido a la gravedad; Esto causa presión sobre el tórax y reduce la capacidad de los pulmones para inflarse, lo que dificulta la respiración de la pantorrilla.
Si la cabeza necesita colocarse hacia abajo para facilitar el drenaje de líquido de las vías respiratorias, la pantorrilla se puede colocar en decúbito esternal sobre una paca y la cabeza se coloca hacia abajo desde aquí, aunque esto rara vez es necesario.
La ventilación mecánica se puede realizar pasando un tubo endotraqueal, o usando una máscara con una bolsa inflable, para proporcionar ventilación con presión positiva; sin embargo, esto no siempre es posible en una situación en la granja.
Analgesia
Se dispone de datos limitados sobre el uso de analgesia en recién nacidos.
Si bien no se ha encontrado que la administración de analgesia con AINE después del nacimiento afecte la transferencia pasiva o los biomarcadores de estrés 21-23, se ha demostrado que los terneros tratados con analgesia con AINE muestran comportamientos consistentes con un estado de bienestar mejorado, en comparación con los terneros tratados con un placebo 24.
Dada la limitada evidencia disponible, sería prudente proporcionar analgesia a los terneros recién nacidos, especialmente si se requiere asistencia o se sospecha una lesión.
No se autorizan analgésicos en el Reino Unido para terneros recién nacidos; por lo tanto, la provisión de analgesia es, por lo tanto, se deben aplicar períodos de retiro fuera de licencia y legales.
Provisión de calostro
Los terneros nacen casi agammaglobulinémicos y la importancia de proporcionar un volumen adecuado de calostro de buena calidad dentro de un período de tiempo apropiado posparto ha sido reconocida por varios años 25-28.
Se ha demostrado que los terneros alimentados con su alimentación inicial de calostro más de cuatro horas después del nacimiento tienen más probabilidades de tener una falla en la transferencia pasiva que los terneros alimentados con calostro antes de las cuatro horas 29,30; por lo tanto, es importante que los terneros reciban calostro dentro de las primeras cuatro horas de vida.
El volumen de calostro requerido por un ternero recién nacido se ha considerado tradicionalmente como el 10% del peso al nacer, estimado entre 4 y 4.5 litros para un ternero Holstein.
El trabajo de Irlanda ha sugerido que un volumen de calostro equivalente al 8,5% del peso al nacer puede ser más apropiado 31.

La limpieza del calostro es de gran importancia, y el calostro debe cosecharse y almacenarse de manera higiénica para evitar la contaminación. Los cubos que contienen calostro deben estar cubiertos (Figura 2) y el calostro que no se va a usar rápidamente debe refrigerarse o congelarse lo antes posible 32,33. La calidad del calostro debe probarse en cada colección. Una concentración de Ig de 50 mg / ml y mayor se considera adecuada 34; el calostro con una concentración inferior a esta no debe administrarse a los terneros recién nacidos. La calidad del calostro varía entre las razas (las razas de Channel Island tienden a tener un calostro de mayor calidad que las Holsteins), así como también entre las edades del ganado, y los animales primíparos tienden a reducir la calidad del calostro en comparación con los animales multíparos. La calidad del calostro se puede medir fácil y económicamente en la granja, ya sea utilizando un calostrómetro (Figura 3)
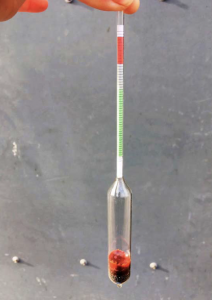
o un refractómetro Brix. Un calostrómetro es un peso de vidrio que se coloca en un cilindro que contiene el calostro a medir. Si el calostro es de alta calidad y, por lo tanto, más denso, el calostrómetro flotará en el calostro. Si el calostro es de baja calidad, menos denso, el calostrómetro se hundirá hasta el fondo del cilindro. Los calostrómetros tienen marcas verdes y rojas para indicar si el calostro es de buena calidad (la marca verde estará expuesta, lo que indica que la concentración de Ig es más de 50 mg / ml) o mala calidad (la marca verde estará sumergida en calostro y solo la marca roja quedará expuesta, lo que indica que la calidad de Ig es inferior a 20 mg / ml). Para usar un refractómetro Brix para medir la calidad del calostro, se coloca una gota de calostro en el refractómetro y se toma un registro de la escala Brix que se puede ver a través del ocular. El calostro de buena calidad debe medir 22% o más en la escala Brix; Esto es equivalente a una concentración de Ig de 50 mg / ml.
Cuidado adicional posparto

Todas las pantorrillas deben tener el ombligo tratado para alentar al muñón umbilical a sanar lo más rápido posible y minimizar el riesgo de infiltración bacteriana del ombligo.
El yodo se usa comúnmente, ya sea como un baño o un aeroso l; sin embargo, además del yodo, hay otros productos disponibles.
Si se usa yodo, es importante que no esté demasiado concentrado; concentraciones superiores al 7,5% son cáusticas y pueden causar daño tisular al ombligo.
Cualquiera que sea el producto elegido, es importante una aplicación cuidadosa para garantizar una cobertura adecuada del ombligo (Figura 4).
El momento de retirar el ternero de la presa puede ser controvertido; sin embargo, si la granja tiene problemas con enfermedades, como la enfermedad de Johne, cuanto antes se retire el ternero del entorno de alto riesgo (el corral de parto), menor será el riesgo de infección.
Se ha demostrado que la separación temprana da como resultado una respuesta conductual reducida tanto de la vaca como de la pantorrilla que la separación tardía 35,36, y por lo tanto, puede ser menos estresante para ambas partes, aunque la evidencia disponible para apoyar esta práctica es contradictoria y sigue siendo discutible. Número 36-38.
Este artículo ha sido revisado por Katherine Ellis, BVMS, CertCHP, PhD, DipECBHM, MRCVS.
Referencias
- Mee JF (2004). Managing the dairy cow at calving time, Vet Clin North Am Food Anim Pract 20(3): 521-546.
- Lombard JE, Garry FB, Tomlinson SM and Garber LP (2007). Impacts of dystocia on health and survival of dairy calves, J Dairy Sci 90(4): 1,751-1,760.
- Patterson DJ, Bellows RA, Burfening PJ and Carr JB (1987). Occurrence of neonatal and postnatal mortality in range beef cattle. I. Calf loss incidence from birth to weaning, backward and breech presentations and effects of calf loss on subsequent pregnancy rate of dams, Theriogenology 28(5): 557-571.
- Laster DB and Gregory KE (1973). Factors influencing peri- and early postnatal calf mortality, J Anim Sci 37(5): 1,092-1,097.
- Arthur PF, Archer JA and Melville GJ (2000). Factors influencing dystocia and prediction of dystocia in Angus heifers selected for yearling growth rate, Aust J Agric Res 51(1): 147-154.
- Tenhagen BA, Helmbold A and Heuwieser W (2007). Effect of various degrees of dystocia in dairy cattle on calf viability, milk production, fertility and culling. J Vet Med A Physiol Pathol Clin Med 54(2): 98-102.
- Barrier AC, Haskell MJ, Birch S, Bagnall A, Bell DJ, Dickinson J, Macrae AI and Dwyer CM (2013). The impact of dystocia on dairy calf health, welfare, performance and survival, Vet J 195(1): 86-90.
- Hossein-Zadeh NG (2014). Effect of dystocia on the productive performance and calf stillbirth in Iranian Holsteins, J Agric Sci Tech 16: 69-78.
- Gundelach Y, Essmeyer K, Teltscher MK and Hoedemaker M (2009). Risk factors for perinatal mortality in dairy cattle: cow and foetal factors, calving process, Theriogenology 71(6): 901-909.
- Berger PJ, Cubas AC, Koehler KJ and Healey MH (1992). Factors affecting dystocia and early calf mortality in Angus cows and heifers, J Anim Sci 70(6): 1,775-1,786.
- Apgar V (1953). A proposal for a new method of evaluation of the newborn infant, Curr Res Anesth Analg 32(4): 260-267.
- Finster M and Wood M (2005). The Apgar score has survived the test of time, Anesthesiology 102(4): 855-857.
- Veronesi MC, Panzani S, Faustini M and Rota A (2009). An Apgar scoring system for routine assessment of newborn puppy viability and short-term survival prognosis, Theriogenology 72(3): 401-407.
- Vannucchi CI, Rodrigues JA, Silva LC, Lúcio CF and Veiga GA (2015). Effect of dystocia and treatment with oxytocin on neonatal calf vitality and acid-base, electrolyte and haematological status, Vet J 203(2): 228-232.
- Murray CF and Leslie KE (2013). Newborn calf vitality: risk factors, characteristics, assessment, resulting outcomes and strategies for improvement, Vet J 198(2): 322-328.
- Doebeli A, Michel E, Bettschart R, Hartnack S and Reichler IM (2013). Apgar score after induction of anesthesia for canine cesarean section with alfaxalone versus propofol, Theriogenology 80(8): 850-854.
- Veronesi MC, Riccaboni P, Faustini M, Battocchio M, Cairoli F and Villani M (2005). Potential association between placental features and Apgar scores after normal parturition in the Thoroughbred horse, J Anim Vet Adv 4(12): 965-970.
- Murray CF (2014). Characteristics, risk factors and management programs for vitality of newborn dairy calves, PhD thesis, University of Guelph.
- Homerosky ER, Timsit E, Pajor EA, Kastelic J and Windeyer MC (2017). Predictors and impacts of colostrum consumption by 4h after birth in newborn beef calves, Vet J 228: 1-6.
- Nagy DW (2009). Resuscitation and critical care of neonatal calves, Vet Clin North Am Food Anim Pract 25(1): 1-11.
- Gladden N, McKeegan D, Viora L and Ellis KA (2018). Postpartum ketoprofen treatment does not alter stress biomarkers in cows and calves experiencing assisted and unassisted parturition: a randomised controlled trial, Vet Rec 183(13): 414.
- Pearson JM, Pajor E, Campbell J, Levy M, Caulkett N and Windeyer MC (2019). A randomised controlled trial investigating the effects of administering a non-steroidal anti-inflammatory drug to beef calves assisted at birth and risk factors associated with passive immunity, health, and growth, Vet Rec Open 6(1): e000364.
- Pearson JM, Pajor EA, Campbell JR, Caulkett NA, Levy M, Dorin C and Windeyer MC (2019). Clinical impacts of administering a non-steroidal anti-inflammatory drug to beef calves after assisted calving on pain and inflammation, passive immunity, health, and growth, J Anim Sci 97(5): 1,996-2,008.
- Gladden N, Ellis K, Martin J, Viora L and McKeegan D (2019). A single dose of ketoprofen in the immediate postpartum period has the potential to improve dairy calf welfare in the first 48h of life, Appl Anim Behav Sci 212: 19-29.
- Weaver DM, Tyler JW, VanMetre DC, Hostetler DE and Barrington GM (2000). Passive transfer of colostral immunoglobulins in calves, J Vet Intern Med 14(6): 569-577.
- McGuire TC, Pfeiffer NE, Weikell JM and Bartsch RC (1976). Failure of colostral immunoglobulin transfer in calves dying from infectious disease, J Am Vet Med Assoc 169(7): 713-718.
- Besser TE, Szenci O and Gay CC (1990). Decreased colostral immunoglobulin absorption in calves with postnatal respiratory acidosis, J Am Vet Med Assoc 196(8): 1,239-1,243.
- Godden S (2008). Colostrum management for dairy calves, Vet Clin North Am Food Anim Pract 24(1): 19-39.
- Chigerwe M, Tyler JW, Schultz LG, Middleton JR, Steevens BJ and Spain JN (2008). Effect of colostrum administration by use of oroesophageal intubation on serum IgG concentrations in Holstein bull calves, Am J Vet Res 69(9): 1,158-1,163.
- Beam AL, Lombard JE, Kopral CA, Garber LP, Winter AL, Hicks JA and Schlater JL (2009). Prevalence of failure of passive transfer of immunity in newborn heifer calves and associated management practices on US dairy operations, J Dairy Sci 92(8): 3,973-3,980.
- Conneely M, Berry DP, Murphy JP, Lorenz I, Doherty ML and Kennedy E (2014). Effect of feeding colostrum at different volumes and subsequent number of transition milk feeds on the serum Immunoglobulin G concentration and health status of dairy calves, J Dairy Sci 97(11): 6,991-7,000.
- Stewart S, Godden S, Bey R, Rapnicki P, Fetrow J, Farnsworth R, Scanlon M, Arnold Y, Clow L, Mueller K and Ferrouillet C (2005). Preventing bacterial contamination and proliferation during the harvest, storage, and feeding of fresh bovine colostrum, J Dairy Sci 88(7): 2,571-2,758.
- Denholm KS, Hunnam JC, Cuttance EL and McDougall S (2017). Influence of preservation methods on the quality of colostrum sourced from New Zealand dairy farms, NZ Vet J 65(5): 264-269.
- Denholm KS, Hunnam JC, Cuttance EL and McDougall S (2017). Associations between management practices and colostrum quality on New Zealand dairy farms, NZ Vet J 65(5): 257-263.
- Flower FC and Weary DM (2001). Effects of early separation on the dairy cow and calf, Appl Anim Behav Sci 70(4): 275-284.
- Meagher RK, Beaver A, Weary DM and von Keyserlingk MAG (2019). Invited review: a systematic review of the effects of prolonged cow–calf contact on behavior, welfare, and productivity, J Dairy Sci 102(7): 5,765-5,783.
- Ventura B, von Keyserlingk MA, Schuppli C and Weary D (2013). Views on contentious practices in dairy farming: the case of early cow-calf separation, J Dairy Sci 96(9): 6,105-6,116.
- Beaver A, Meagher RK, von Keyserlingk MAG and Weary DM (2019). Invited review: a systematic review of the effects of early separation on dairy cow and calf health, J Dairy Sci 102(7): 5,784-5,810.
Date de alta y recibe nuestro 👉🏼 Diario Digital AXÓN INFORMAVET ONE HEALTH
Date de alta y recibe nuestro 👉🏼 Boletín Digital de Foro Agro Ganadero
Noticias animales de compañía
Noticias animales de producción
Trabajos técnicos animales de producción
Trabajos técnicos animales de compañía
