Infertilidad reproductiva bovina: patogénesis e inmunoterapia

Infertilidad reproductiva bovina: patogénesis e inmunoterapia
 Vinod Kumar Gupta1*
Vinod Kumar Gupta1*  Tushar Kumar Mohanty1
Tushar Kumar Mohanty1  Mukesh Bhakat1
Mukesh Bhakat1  Raju Kumar Dewry1*†
Raju Kumar Dewry1*†  Rahul Katiyar2*
Rahul Katiyar2*  Dipti Nain1
Dipti Nain1  Nadeem Shah1
Nadeem Shah1  Manisha Sethi1
Manisha Sethi1  Rupali Rautela3
Rupali Rautela3  Mahak Singh4
Mahak Singh4  Sourabh Deori2
Sourabh Deori2- 1Centro de Investigación de Mejoramiento Artificial (ABRC), ICAR-Instituto Nacional de Investigación Lechera, Karnal, India
- 2División de Ciencias Animales y Pesqueras, Complejo de Investigación ICAR para la Región NEH, Umiam, Meghalaya, India
- 3CAR-Instituto Central de Investigación sobre Búfalos, Hisar, India
- 4Complejo de investigación CAR para la región NEH, Centro Nagaland, Medziphema, India
La infertilidad es uno de los principales factores para la reproducción del ganado en el escenario actual. La inmunoinfertilidad relacionada con la reproducción implica principalmente la inmunización contra los antígenos relacionados con las hormonas reproductivas (LHRH, GnRH, esteroides gonadales, PGF2α y oxitocina), espermatozoides, plasma seminal y óvulo. La anovulación, el retraso en la ovulación, la inmovilización de los espermatozoides, el fracaso de la fertilización, la involución uterina prolongada, el intervalo de parto prolongado, el estro posparto prolongado y la reducción de la tasa de concepción podrían ser el resultado de la inmunoinfertilidad que ocurre debido al bloqueo del sitio receptor por anticuerpos formados contra hormonas, espermatozoides y óvulos. La inmunoinfertilidad se puede tratar en el animal dando descanso sexual a las hembras, mediante el uso de diversas tecnologías reproductivas como la fertilización in vitro, la transferencia de trompas intra de Falopio de gametos y la inyección intracitoplasmática de espermatozoides, lavado de espermatozoides y tratando a los animales con inmunomoduladores como LPS, glucógeno de ostra, etc. Esta revisión resume las diferentes causas de la inmunoinfertilidad reproductiva bovina y las estrategias de mejora para superarla.
Introducción
La infertilidad es el principal problema en la reproducción bovina en la industria láctea. Hay varias causas de infertilidad, como fisiológicas, anatómicas, nutricionales y de manejo que pueden diagnosticarse, sin embargo, la mayoría de las veces la inmunoinfertilidad es inexplicable y mal diagnosticada (1, 2). La inmunoinfertilidad se refiere a la condición en la que el sistema inmune reconoce los gametos (espermatozoides y óvulos) como extraños y lanza una respuesta inmune contra ellos, lo que lleva a dificultades en la concepción (1, 3). En el contexto de las biotecnologías reproductivas, como la fertilización in vitro (FIV), la inmunoinfertilidad puede plantear desafíos. Las respuestas inmunes contra los espermatozoides y los óvulos pueden deberse a la presencia de antígenos en la superficie de estas células que el sistema inmunitario reconoce como no propios. Las reacciones inmunes pueden dificultar la fertilización y la implantación del embrión, lo que resulta en infertilidad. Esto es más común en los casos en que el ganado macho y hembra tienen variaciones genéticas en sus genes del complejo principal de histocompatibilidad (MHC), que desempeñan un papel clave en el reconocimiento inmunológico. Para abordar la inmunoinfertilidad en las biotecnologías reproductivas, se pueden utilizar técnicas como la inyección intracitoplasmática de espermatozoides (ICSI). La ICSI consiste en inyectar un solo espermatozoide directamente en un óvulo, evitando la necesidad de que los espermatozoides naveguen a través del tracto reproductivo femenino, donde podría encontrar una respuesta inmune (4). La inmunoinfertilidad ha implicado principalmente la inmunización contra antígenos que tienen una relación con la reproducción. Estos antígenos podrían estar relacionados con hormonas reproductivas (LHRH, GnRH, esteroides gonadales, PGF2α y oxitocina), espermatozoides, plasma seminal y óvulo (5). Los anticuerpos que se forman contra estos antígenos pueden bloquear el sitio receptor de las hormonas, óvulos y espermatozoides; y puede conducir a anovulación, retraso en la ovulación, fracaso de la fertilización, muerte embrionaria temprana, reproducción repetida, intervalo interestral prolongado, involución uterina prolongada, infecciones uterinas como endometritis, intervalo de parto prolongado, estro posparto prolongado y tasa de concepción reducida que causan enormes pérdidas económicas (6). Los trastornos reproductivos, particularmente la endometritis, son uno de los principales problemas reproductivos para los bovinos y la resistencia a los antibióticos está complicando aún más el problema. Los inmunomoduladores tienen el potencial de reemplazar el uso de antibióticos contra la endometritis (7). La presente revisión tiene como objetivo resumir los hallazgos sobre la inmunoinfertilidad, incluido su diagnóstico, prevención y control, y superar su efecto mediante diversos inmunomoduladores.
Patogénesis de la inmunoinfertilidad
Inmunoinfertilidad debido a la ruptura de la barrera sangre-testículo
La inmunoinfertilidad puede ocurrir como autoinmunidad tanto en hombres como en mujeres o isoinmunidad en mujeres (1). La autoinmunidad surge cuando se producen anticuerpos contra los espermatozoides en el cuerpo de la hembra (8). La autoinmunidad en los hombres se ha asociado con la isoinmunidad en las mujeres (9). La tolerancia inmune al autoantígeno se establece en el período neonatal, de ahí que los nuevos antígenos en desarrollo que aparecen en la superficie de los espermatozoides durante el secuestro inmunogénico de la espermatogénesis, detrás de la barrera sangre-testículo formada por uniones estrechas de células de Sertoli, impidan la generación de autoanticuerpos contra los espermatozoides (1). Sin embargo, una vez que se rompe la barrera sangre-testículo debido a cambios mecánicos, infecciosos, inflamatorios o degenerativos, resulta en la exposición de antígenos espermáticos inmunogénicos al sistema inmunológico de los animales (10). Por lo tanto, se inicia una respuesta inmune, lo que resulta en una reacción antiinflamatoria y la formación de anticuerpos antiespermatozoides. Se ha informado que los óvulos son menos inmunogénicos en comparación con los espermatozoides (11).
Inmunoinfertilidad inducida por infección uterina
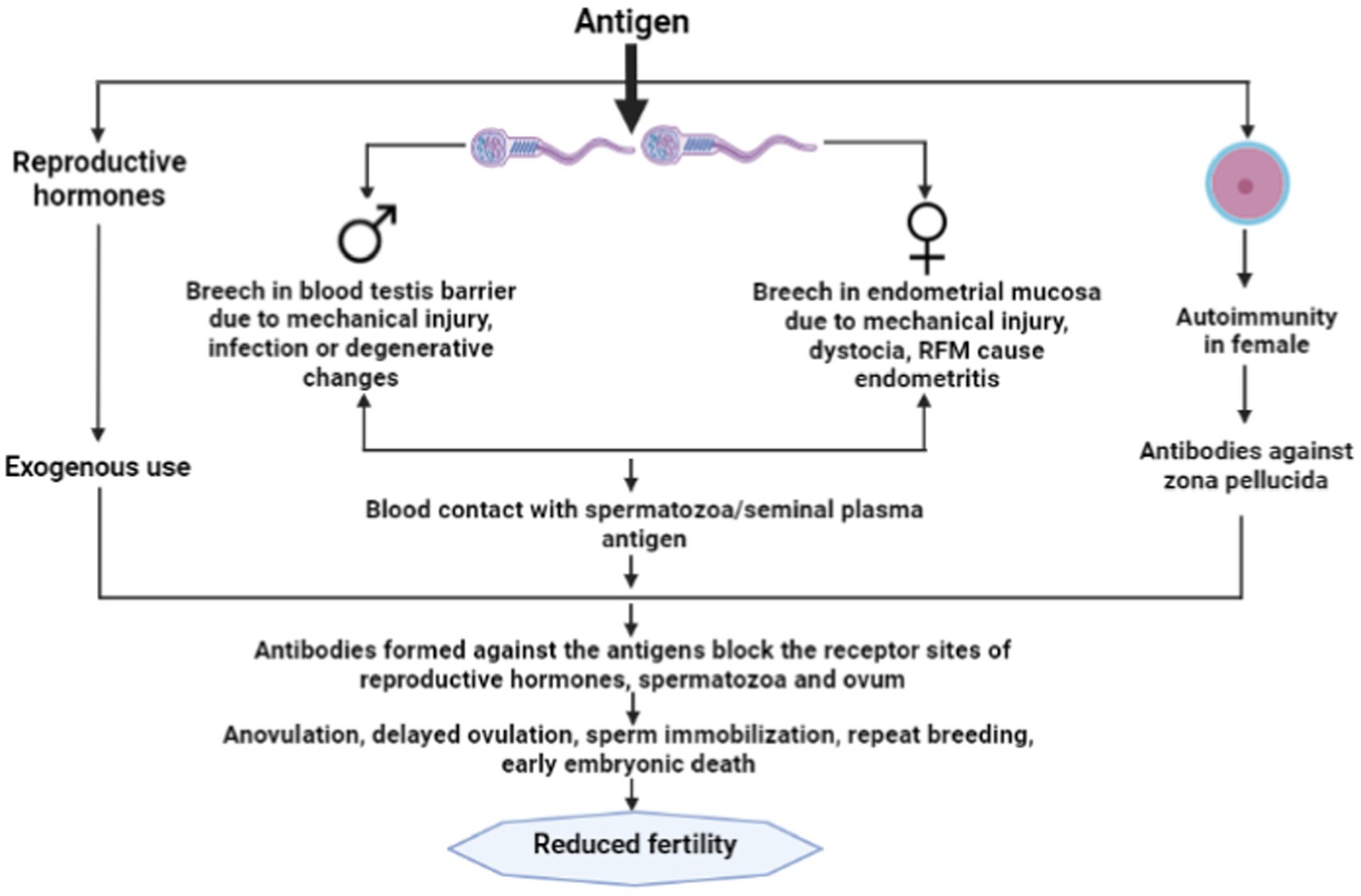
En general, durante el apareamiento natural, el tracto reproductor femenino está expuesto a los espermatozoides, pero no inicia la respuesta inmune contra los espermatozoides debido a la presencia de sustancias inmunoinhibitorias como la 19-hidroxi prostaglandina E, poliaminas, transglutaminasa y proteína de unión al receptor Fc de alto peso molecular presente en el plasma seminal, el líquido folicular y uterino, así como el moco cervical (1, 12) que pueden proteger a los espermatozoides del daño inmunogénico y prevenir la sensibilización de una hembra a los antígenos espermáticos. Sin embargo, en el caso de la endometritis que puede ocurrir debido a cualquier lesión física o infección bacteriana en la mucosa del endometrio, la sangre se expone a los espermatozoides o antígenos plasmáticos seminales en el momento de la inseminación artificial o el servicio natural (6). Esta exposición resulta en la formación de anticuerpos antiespermatozoides en el cuerpo de las hembras y secretados en el moco cervical y el líquido uterino que podrían inmovilizar los espermatozoides (12). Se ha informado que la infección en el tracto reproductivo femenino, particularmente la endometritis, podría desempeñar un papel potencial en la inmunoinfertilidad en animales hembras (13). Las vacas lecheras posparto temprano con frecuencia experimentan infecciones bacterianas uterinas. Dentro de las primeras 2 semanas después del parto, el 90% de las vacas sufren infecciones bacterianas del útero (14). Las dos principales bacterias patógenas que con frecuencia se ven relacionadas con las infecciones uterinas de las vacas son Escherichia coli y Trueperella pyogenes (14). La producción de lipopolisacárida (LPS) por bacterias gramnegativas, que es un componente importante de la membrana celular, estimula el sistema inmune innato que resulta en la respuesta inflamatoria (15). El LPS presente en la circulación periférica puede translocarse a líquido folicular resultando en aberraciones ovulatorias, sin embargo, el mecanismo de translocación sigue siendo un tema de debate (16). La alta concentración de LPS en el líquido folicular puede alterar la transcripción de la transcripción de las gonadotropinas. Se ha observado que el LPS perjudica la esteroidogénesis folicular y actúa por acción directa sobre las células de la teca y la granulosa. Los niveles bajos de estradiol en el líquido folicular y la alta expresión de ARNm de caspasa-3 en folículos con alto contenido de LPS apuntan a una conexión con la atresia folicular (17). Por lo tanto, la inmunidad del útero durante el período posparto juega un papel importante en la competencia de desarrollo del ovocito (Figura 1).
Tabla 1. Tabla que muestra diferentes pruebas diagnósticas para detectar anticuerpos antiespermatozoides y su principal en diversas razas / especies.
Tratamiento de la inmunoinfertilidad
Antígenos plasmáticos seminales y espermatozoides
Los antígenos en los espermatozoides y el plasma seminal juegan un papel importante en la función y la concepción de los espermatozoides. Los antígenos plasmáticos seminales como PH-20, PH-30, antígeno de fertilización-1 (18) albúmina, globulina, glicoproteínas, lactoferrina (19) y antígenos espermatozoides como hialuronidasa, acrosina, neuraminidasa y enzima dispersora corona son el antígeno importante que ayuda en la fosforilación de proteínas tirosina, capacitación, reacción acrosomal, fusión de gametos y fertilización. Los antígenos MHC1a y HY se encuentran en los espermatozoides necesarios para la implantación del embrión (20). IZUMO1 es una proteína de superficie de los espermatozoides que ayuda en la capacitación y la fusión de ovocitos de los espermatozoides (21). Las proteínas de la superficie de los espermatozoides como ADAM1, ADAM2 y ADAM3 tienen un potente papel en la unión espermatozoide-ovocito (22). Varios antígenos plasmáticos seminales se encuentran en forma de citoquinas y péptidos antimicrobianos que regulan las respuestas inmunes e inflamatorias y mantienen la fertilidad (13). La beta defensina 126 es un péptido antimicrobiano secretado por el epitelio epididimario bovino que se encuentra en el semen y se asocia con la motilidad de los espermatozoides, el quimioatrayente, la señalización celular, la unión epitelio ospermático-oviductal y la unión espermatozoide-ovocitos (23). Se requiere para la maduración de los espermatozoides en el epidídimo masculino y la protección de los espermatozoides en el tracto reproductor femenino (13). Los anticuerpos formados contra estos antígenos pueden impedir su funcionalidad y dificultar la motilidad de los espermatozoides.
Antígenos de óvulos
Los antígenos de la zona pelúcida en mamíferos son de especial interés debido a su posible implicación en la inmunoinfertilidad y como diana candidata para la inmunoanticoncepción. La zona pelúcida del óvulo comprende tres glicoproteínas bioquímica e inmunológicamente distintas, es decir, ZP1, ZP2 y ZP3 de las cuales los espermatozoides se unen a ZP3. El bloqueo de la función de la proteína con anticuerpos resulta en infertilidad y esto se ha demostrado experimentalmente en el caballo y los monos (5, 24). Por lo tanto, ZP3 puede considerarse un objetivo proteico importante para la inmunoanticoncepción en caballos y monos (24) y se está utilizando actualmente para la producción de vacunas anticonceptivas.
Antígenos en extensores de semen
El componente importante del diluyente de semen es la yema de huevo y las proteínas de la yema de huevo pueden actuar como antígenos, lo que se confirmó mediante el aislamiento de anticuerpos contra los antígenos de la yema de huevo en novillas inseminadas en el período posparto temprano (25), así como en la vagina y el útero de vacas inseminadas (26).
Anticuerpos e infertilidad
Los impactos de los anticuerpos anti-espermatozoides en la infertilidad dependen de la concentración. Las concentraciones bajas y moderadas de anticuerpos de esperma en la sangre no afectan la función reproductiva del ganado, mientras que las concentraciones altas generalmente se asocian con infertilidad (27). Las vacas reproductoras repetidas mostraron un título de 1:512 cuando se probaron con los toros que se usaron previamente para inseminaciones, mientras que las vacas concebidas mostraron un título de 1:16 o menos en el primer servicio (25). La exposición frecuente a antígenos seminales a través de la inseminación repetida eleva el título de anticuerpos y da como resultado una disminución de la fertilidad y un mayor número de inseminaciones por concepción. El título de anticuerpos de esperma en el suero sanguíneo de la vaca no excede 1:16 cuando ocurrió la concepción, pero los servicios repetidos llevaron a un aumento en el título a 1:512. La presencia de anticuerpos fue confirmada por múltiples medios (25).
Anticuerpos antiespermatozoides
Las células germinales en crecimiento expresan nuevos antígenos de superficie durante la espermatogénesis, aunque estos son difíciles de distinguir. Los antígenos de superficie exclusivos de los espermatozoides surgen inicialmente en el espermatocito primario de paquiteno (28). Cuando estos antígenos de superficie específicos de los espermatozoides entran en contacto con la sangre en el momento del trauma quirúrgico, diversas enfermedades microbianas como la prostitis y la orquitis, el cáncer testicular y el varicocele, la formación de AAS puede acelerarse. Los anticuerpos antiespermatozoides se pueden encontrar en un toro con orquitis 18 meses después de la manifestación inicial. Esto representa los efectos prolongados de las infecciones genitales sobre la fertilidad (29). La ubicación, la especificidad regional y la especificidad del antígeno de los anticuerpos antiespermatozoides definen sus efectos sobre la fertilidad. Los anticuerpos antiespermatozoides se encontraron en el plasma seminal o en suero en la forma no unida, sin embargo, solo se encontró que los anticuerpos antiespermatozoides unidos a los espermatozoides tenían un efecto perjudicial. Sardoy et al. (11) encontraron que las inmunoglobulinas como IgA e IgG, pero no IgM, tienen una influencia perjudicial sobre la fertilidad. Las principales razones de la infertilidad asociada con los anticuerpos antiespermatozoides son la prevención de la fertilización o la mortalidad embrionaria temprana. Los posibles mecanismos implicados en el fracaso de la fecundación mediada por anticuerpos espermatozoides son la inmovilización de los espermatozoides, la inhibición de la migración a través del tracto genital femenino, la inactivación de las enzimas acrosomales para la fecundación, la inhibición de la unión de los espermatozoides y la penetración en la zona pelúcida de los óvulos y la muerte embrionaria. La formación de ASA es inducida por los efectos sobre los espermatozoides fertilizantes y por las acciones sobre el desarrollo del conceptus (11). Los anticuerpos antiespermatozoides también pueden influir en la supervivencia del embrión periimplantacional. Los antígenos producidos a partir de los espermatozoides pueden permanecer en el oolemma después de la fertilización. Debido a la producción de antígenos embrionarios que podrían reaccionar de forma cruzada con los espermatozoides, se pueden producir anticuerpos antiespermatozoides durante la etapa embrionaria temprana. Estos anticuerpos pueden hacer que las células activadas en el sistema inmunitario femenino produzcan linfocinas citotóxicas, lo que puede afectar indirectamente el desarrollo fetal (30) (Figura 2).
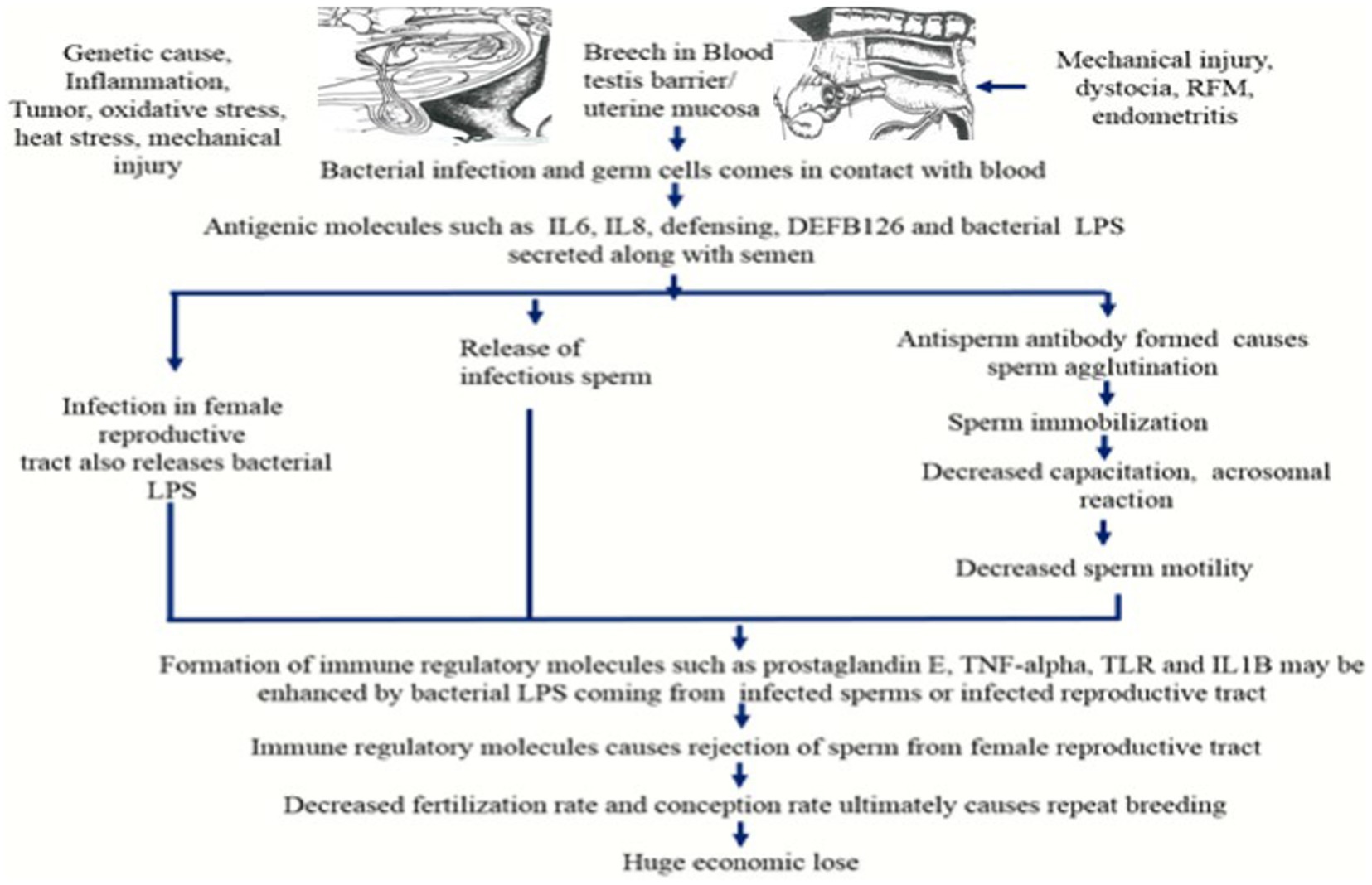 Figura 2. Producción de anticuerpos antiespermatozoides por el sistema inmune y su impacto en la motilidad y fertilidad de los espermatozoides (RFM, Retensión de la membrana fetal; IL6: interleucina 6; IL8: interleucina 8; LPS: lipopolisacárido; TNF-alfa: factor necrótico tumoral alfa; TLR: receptor similar a Toll; IL1B, Interleucina 1B).
Figura 2. Producción de anticuerpos antiespermatozoides por el sistema inmune y su impacto en la motilidad y fertilidad de los espermatozoides (RFM, Retensión de la membrana fetal; IL6: interleucina 6; IL8: interleucina 8; LPS: lipopolisacárido; TNF-alfa: factor necrótico tumoral alfa; TLR: receptor similar a Toll; IL1B, Interleucina 1B).
Consecuencias económicas de la inmunoinfertilidad
La inmunodeficiencia en el ganado de granja puede tener consecuencias económicas significativas. Cuando el ganado tiene sistemas inmunológicos debilitados, son más susceptibles a diversas enfermedades reproductivas, lo que lleva a una menor recuperación, menor tasa de concepción, mayores tasas de mortalidad y reducción de la productividad general. Esto resulta en mayores gastos veterinarios, así como pérdidas debido a la disminución de la producción de leche. Además, la inmunodeficiencia podría requerir el uso de antibióticos y otros tratamientos, lo que aumenta aún más los costos. Los brotes de enfermedades pueden dar lugar a restricciones comerciales y prohibiciones de las exportaciones de ganado, que afectan a toda la industria. La confianza de los consumidores también puede verse socavada, lo que lleva a una disminución de la demanda de productos ganaderos (31). En general, mantener la salud inmunológica del ganado agrícola es crucial para minimizar las pérdidas económicas y mantener un sector agrícola rentable. Por lo tanto, el diagnóstico de los factores causales involucrados en la inmunoinfertilidad se vuelve esencial.
Diagnóstico de anticuerpos antiespermatozoides
ASA puede ser detectado por pruebas directas e indirectas. Las pruebas indirectas incluyen la prueba de aglutinación de espermatozoides, la prueba de inmovilización de espermatozoides, el ensayo de inmunoperlas, ELISA, mientras que la prueba directa incluye reacción de aglutinación mixta, ensayo de inmunofluoroscencia, ensayo de antiglobulina radiomarcada, citometría de flujo, etc. Las medidas preventivas para reducir la inmunoinfertilidad incluyen el descanso sexual, el cambio de terapia masculina y la seroterapia (32). Se observó que las vacas tenían títulos altos de anticuerpos contra antígenos seminales de toros que se usaban comúnmente con fines de reproducción en comparación con los toros que se usaban con menos frecuencia o mostraban títulos bajos contra antígenos seminales. En un estudio, un grupo de nueve reproductores repetidores con títulos altos de AAS fueron tratados con un cambio de macho, y seis animales fueron encontrados concebidos (32) (Tabla 1).
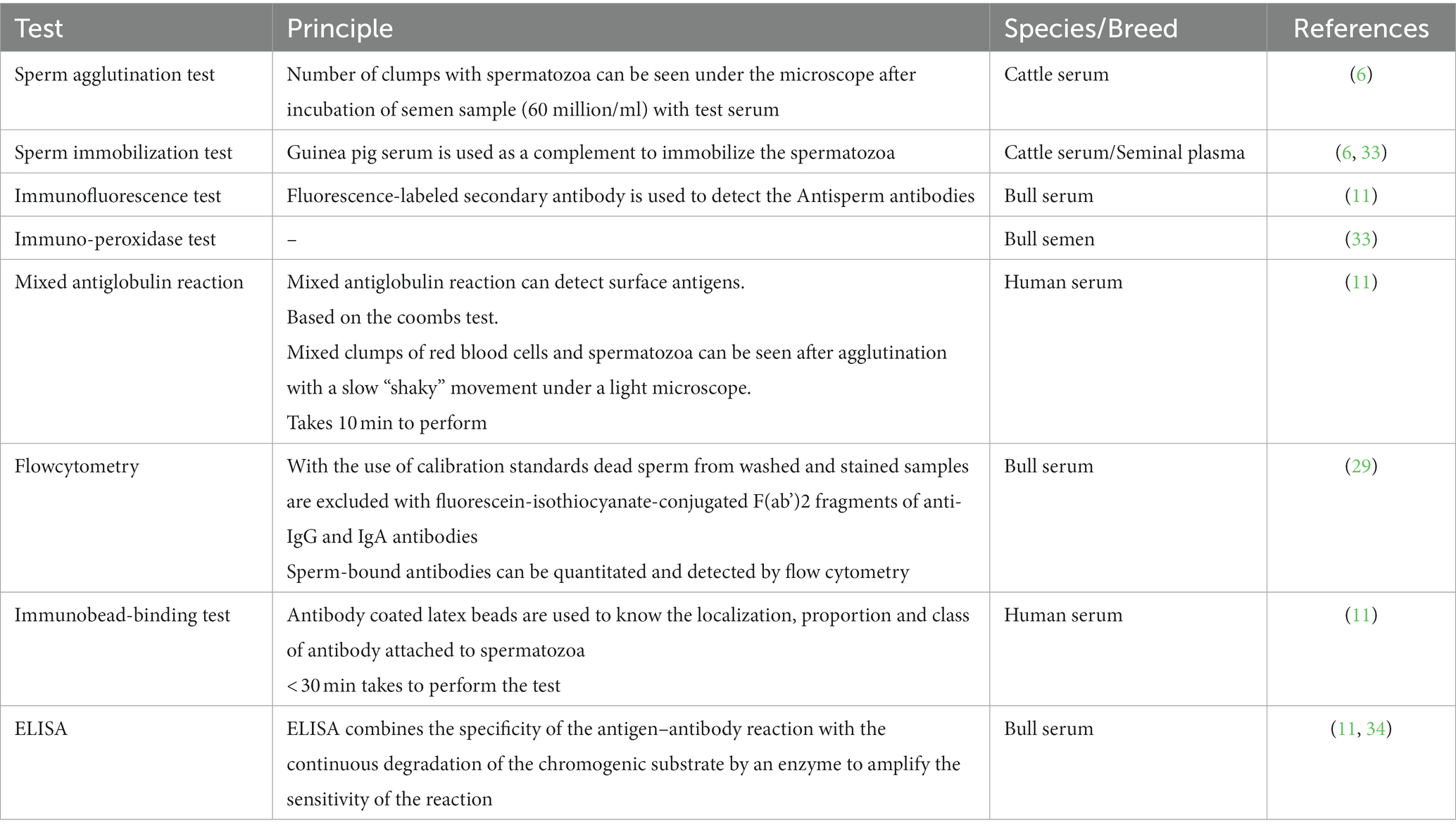 Tabla 1. Tabla que muestra diferentes pruebas diagnósticas para detectar anticuerpos antiespermatozoides y su principal en diversas razas / especies.
Tabla 1. Tabla que muestra diferentes pruebas diagnósticas para detectar anticuerpos antiespermatozoides y su principal en diversas razas / especies.
Tratamiento de la inmunoinfertilidad
Se pueden usar varias estrategias para tratar la infertilidad mediada por anticuerpos antiespermatozoides. El inmunoagotamiento, el lavado de espermatozoides y el tratamiento con proteasa IgA son ciertos métodos para la eliminación de anticuerpos antiespermatozoides de los espermatozoides (35). Los anticuerpos antiespermatozoides en muestras de esperma se pueden aislar recubriendo microperlas magnéticas con antiinmunoglobulina y combinándolas con espermatozoides. Las muestras de semen se someten a un clasificador magnético de células y los espermatozoides ASA positivos se extraen de la muestra (36). Se ha observado una reducción significativa en el número de espermatozoides unidos a anticuerpos antiespermatozoides mediante la aplicación de este proceso. El uso de este proceso en técnicas de reproducción asistida como la inseminación intrauterina, la inseminación intracervical, la fertilización in vitro, la transferencia de trompas intrafalopianas de gametos, la inyección subzonal de espermatozoides y la inyección intracitoplasmática de espermatozoides reduce las posibilidades de que los gametos estén expuestos a anticuerpos antiespermatozoides, lo que mejora la función de los gametos (37). El tratamiento de los espermatozoides con proteasa o quimotripsina antes de la inseminación intrauterina puede reducir los anticuerpos antiespermatozoides contra la superficie de los espermatozoides (37). Una mayor concentración de zinc seminal se considera beneficiosa para la motilidad de los espermatozoides porque desempeña un papel importante en las funciones de la próstata, el epidídimo y el testículo y genera energía para la motilidad de los espermatozoides a través del catabolismo lipídico (38). La suplementación de sulfato de zinc y propionato de zinc a toros de ganado cruzados en su dieta ha mejorado la calidad del semen (39).
Infección uterina e infertilidad
Anatómicamente las descargas de moco de la glándula endometrial; epitelio columnar pseudoestratificado que cubre el endometrio e inmunológicamente, células inflamatorias polimorfonucleares (PMN) y anticuerpos humorales (40). Cuando estos sistemas se alteran, las infecciones oportunistas, principalmente los microbios presentes en el tracto gastrointestinal posterior y que rodean el área perineal, pueden invadir el endometrio y causar endometritis (41). El coito, la gripe aviar o, más comúnmente, el parto puede causar inflamación endometrial en el ganado. La mayoría del ganado tiene microorganismos en su luz uterina de 1 a 4 semanas después del parto, aunque normalmente se autocuran dentro de las 6 semanas. Las vacas que no pueden contrarrestar la infección pueden desarrollar endometritis. El diagnóstico generalmente se realiza durante un control de rutina de las vacas después del parto o cuando se crían. La endometritis hace que la concepción del animal se retrase significativamente (42).
El útero de una vaca posparto ha producido una amplia gama de bacterias, incluyendo aerobios y anaerobios grampositivos y gramnegativos (43). Arcanobacter pyogenes es la bacteria más comúnmente aislada. (44). Otras bacterias han sido cultivadas y asociadas con endometritis de diversa gravedad, incluyendo Streptococci, Staphylococci, y Escherchia coli (45). Debido a que tanto los organismos patógenos como los no patógenos habitan en el endometrio bovino, y muchos de ellos son selectivos, ha sido difícil identificar las bacterias más importantes asociadas con la endometritis (46). Fusobacterium necrophorum y Bacteroides melaninogenicus han sido identificados en los anaerobios cultivados a partir de casos de endometritis. Probablemente, actúan sinérgicamente con A. pyogenes en endometritis severa (47). Una biopsia endometrial o un cultivo de secreción uterina pueden identificar fácilmente la endometritis (48, 49), sin embargo, estas estrategias no se pueden utilizar como una herramienta de detección de campo de rutina para identificar a todas las vacas que necesitan tratamiento. La haptoglobina en la sangre periférica ha sido utilizada como marcador de endometritis por algunos investigadores. Es una proteína de fase aguda producida en el hígado en respuesta al daño tisular, y su función principal es unirse a la hemoglobina libre y proteger al huésped de la actividad oxidativa de la hemoglobina (50).
Mecanismo inmune implicado en la inmunomodulación de la infección uterina
El microbio es fagocitado por células inflamatorias nucleares polimorfas (PMN), monocitos sanguíneos y macrófagos tisulares a través de diversos procedimientos como quimiotaxis, adhesión y unión de PMN a antígenos de superficie celular mostrados por el patógeno (51). Durante el parto normal sin asistencia, después de 48 h no sólo los leucocitos, sino también los microorganismos contaminantes se acumulan en la luz uterina. Esto indica el inicio de un proceso normal de limpieza e involución uterina (52). La actividad fagocítica de las células PMN uterinas disminuye inicialmente durante la metritis puerperal en bovinos, sin embargo, la actividad fagocítica de las células PMN uterinas aumenta después de 2-3 semanas, (53).
Las actividades fagocíticas de neutrófilos también están influenciadas por fluctuaciones hormonales. El aumento de los niveles de progesterona o cortisol en sangre, por ejemplo, disminuye la actividad fagocítica de neutrófilos en el útero y la circulación periférica (54). El número de neutrófilos en la sangre periférica aumentó constantemente desde aproximadamente 6 semanas antes del parto hasta un pico el día del parto, aunque el cortisol materno y fetal puede tener una función limitada de los neutrófilos durante este tiempo (55). Poco después del parto, la actividad fagocítica de los neutrófilos sanguíneos disminuye, aunque los mecanismos de defensa celular de la luz uterina se mantienen al aumentar los niveles de PMN (56). La cantidad de células PMN en la sangre periférica disminuye durante las primeras 1-3 semanas después del parto, muy probablemente debido a la migración de células PMN a la glándula mamaria y la luz uterina. La actividad fagocítica de las células PMN disminuyó significativamente en vacas envejecidas en comparación con las más jóvenes (57). Tanto en bovinos como en yeguas, la actividad fagocítica de los neutrófilos se encontró mayor en la sangre periférica que en la luz uterina (56). Cuando los microorganismos patógenos conocidos fueron inoculados experimentalmente intrauterinos, el orden de aparición de inmunoglobulinas en las secreciones cervicales y vaginales fue IgM, IgA e IgG, mientras que el orden de eliminación de las inmunoglobulinas fue IgM, IgG e IgA (58).
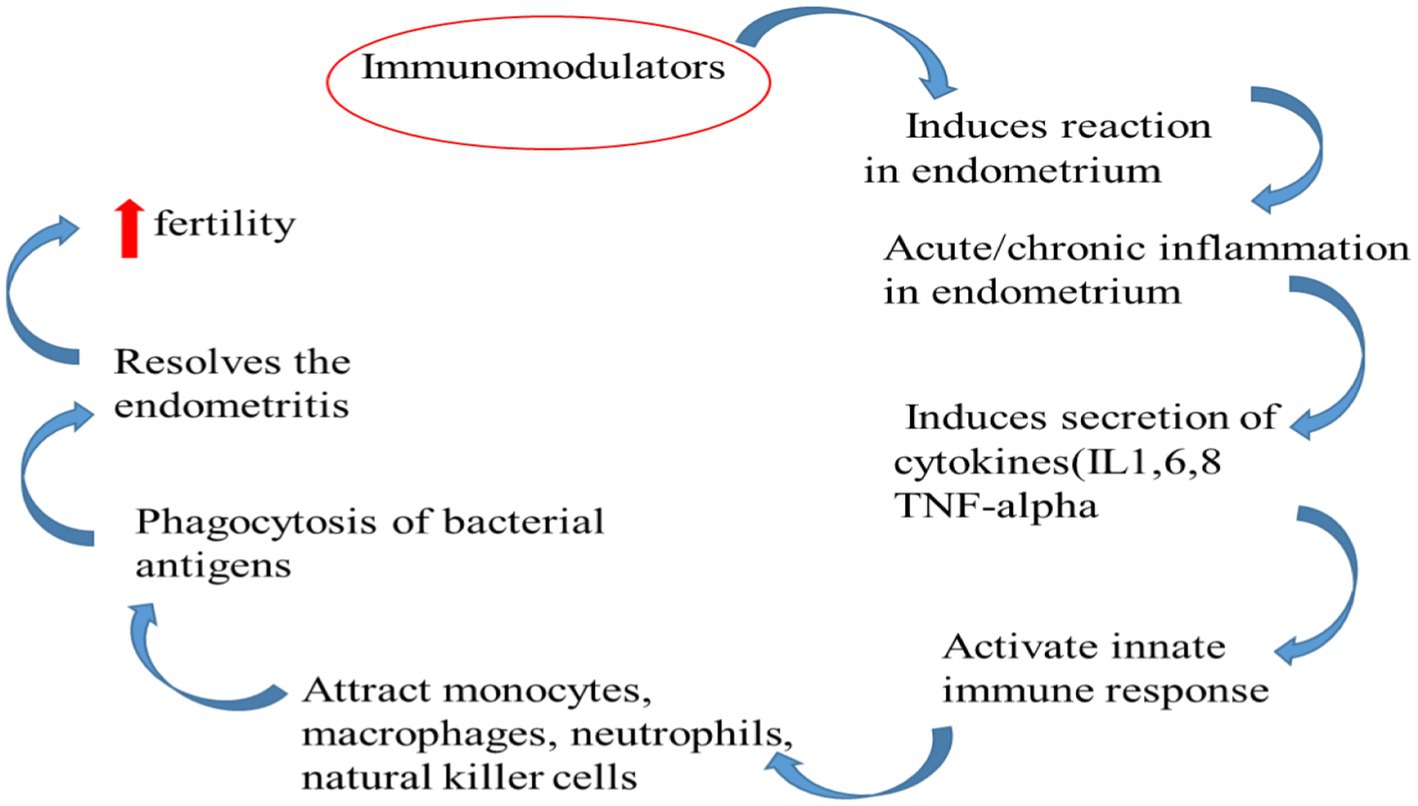
La IgG predomina en la luz uterina, mientras que la IgA predomina en el canal vaginal (59). Aunque las concentraciones de IgG en las secreciones vaginales son más altas durante el celo (60), pocas investigaciones han analizado la influencia específica de las hormonas esteroides en las concentraciones de inmunoglobulina. Las cantidades de IgG e IgM en los loquios de vacas sanas disminuyen después del parto (61). Aquellas vacas que tienen puerperio anormal, la concentración de inmunoglobulinas como IgA e IgG aumenta en la secreción uterina a medida que se desarrolla la endometritis (62). La IgA se produce en la superficie mucosa del útero bovino. El endometrio produce la mitad de la fracción IgG1, mientras que el equilibrio de la IgG1 y toda la IgG2 provienen de la circulación periférica (63) (Figura 3).
Inmunomoduladores como terapia sustitutiva de los antibióticos
Varias terapias antibióticas comúnmente utilizadas para tratar problemas posparto en el ganado pueden tener un impacto negativo en la respuesta inmune celular uterina (64). La extracción manual de las membranas fetales, por ejemplo, puede reducir la actividad fagocítica leucocitaria uterina durante varios días (65), como la administración intrauterina de la mayoría de los antisépticos y desinfectantes (51). Los antibióticos administrados por vía intrauterina reducen la actividad leucocítica uterina, lo que podría tener consecuencias importantes en el tratamiento de la metritis si las bacterias involucradas se vuelven resistentes al antibiótico. El uso extensivo de antibióticos no solo causa resistencia a los medicamentos antimicrobianos, sino que también es responsable de la secreción de residuos de medicamentos en la leche (7). Además de los antibióticos, la necrosis endometrial y la fibrosis pueden ser causadas por sobredosis o uso continuo de una variedad de medicamentos diferentes, como el yodo de Lugol y la polivinilpirrolidona yodada (66-68). Como resultado, los inmunomoduladores deben usarse como una terapia alternativa para los problemas reproductivos bovinos.
Papel de los inmunomoduladores en el tratamiento de la infertilidad
Se ha llevado a cabo un extenso trabajo de investigación para el tratamiento de la metritis y la endometritis con inmunomoduladores en bovinos y yeguas. El papel de los inmunomoduladores en los sistemas de defensa uterinos se discute a continuación.
Hormonas reproductivas utilizadas como inmunomodulador en el tratamiento de la infección uterina
La patogenicidad de los microorganismos presentes en el útero posparto en todas las etapas del estro está regulada por el patrón cíclico de la concentración de hormonas esteroides. El endometrio es más susceptible a la infección bajo dominancia de progesterona que la dominancia de estrógeno, como lo demuestra el aumento del flujo sanguíneo al útero, el aumento de la producción de moco y el aumento de la actividad de PMN durante la fase de estrógeno del ciclo ovárico, pero la reducción de la permeabilidad bacteriana en el epitelio endometrial retrasa la estimulación leucocitaria durante la fase lútea (56). Chacin et al. (69) observaron que cuando los animales fueron expuestos al estrógeno, su actividad PMN aumentó. La progesterona exhorta a una acción inhibitoria sobre la contracción miometrial que el estradiol porque la progesterona inhibe la conductividad eléctrica en el miometrio (70). Como resultado, la eliminación de escombros a través de un cuello uterino abierto es ineficaz (71). Además de estas dos hormonas, PGF2α que se sintetiza principalmente en el endometrio caruncular del útero puede contraerse y eliminar los desechos uterinos (72). La oxitocina causa la secreción de PGF2 del útero, lo que estimula la liberación de oxitocina del cuerpo lúteo, que finalmente induce la secreción de PGF2 del endometrio. Hasta que se completa la luteólisis, este proceso de retroalimentación positiva opera (73). Como resultado, desde el día 16 del ciclo estral hasta el celo, la progesterona en sangre periférica disminuye. La involución se retrasa si la duración de la liberación de PGF2 después del parto es demasiado corta; Si el intervalo se prolonga, el proceso de involución se acelera (74). Después del parto normal, las concentraciones de metabolitos PGF2 en la sangre periférica son altas y no se recuperan a la línea de base hasta 14 días después del parto (72). Por el contrario, la metritis o endometritis aguda en vacas causada por una infección microbiana uterina oscurece la involución (75).
Como resultado, hay tres razones para tratar la endometritis con PGF2. La terapia con prostaglandinas exógenas administrada a terneros con un cuerpo lúteo funcional causa luteólisis y hace que el animal entre en celo, disminuyendo el efecto inhibitorio de la progesterona sobre el sistema de defensa uterino o aumentándolo con estrógeno. Las contracciones miometriales también son causadas por PGF2 (76), que puede ser un mecanismo que expulsa desechos y microorganismos que contaminan la luz uterina después del parto. En tercer lugar, PGF2 puede tener un efecto estimulante sobre la actividad fagocítica de PMN uterina (77). Como resultado, la endometritis en vacas con un cuerpo lúteo funcional se ha tratado utilizando la actividad luteolítica de PGF2.
Escherichia coli lipopolisacáridos
Se cree que los PMN son atraídos a la luz uterina por el efecto quimioatrayente de los lipopolisacáridos de E. coli (LPS). Este aumento de PMN en el endometrio podría ayudar a las vacas y yeguas a recuperarse de la endometritis (78). Targowski (79) encontró que una infusión intrauterina de 100 g de E. coli LPS aumentó el número de PMN encontrados en las secreciones uterinas a las 6 y 24 h después del tratamiento en vacas sanas. Rashid Dar et al. (7) evaluaron el efecto inmunomodulador de la curcumina 30 M, lipopolisacárido (LPS) y/o flagelina (100 ng/mL cada uno) sobre la producción de prostaglandina E2 (PGE2) y citoquinas proinflamatorias (PIC) utilizando células primarias del estroma endometrial bubalínico. Descubrieron que el LPS estimula fuertemente la producción de PGE2, pero la flagelina tiene un impacto estimulante menor. LPS aumentó significativamente las transcripciones de IL8 e IL6 en células del estroma endometrial bubalina en comparación con IL1 y TNF. La curcumina previno la regulación positiva inducida por LPS de PIC mientras reducía significativamente los niveles de IL8. Los efectos inhibitorios de la curcumina sobre los mediadores inflamatorios sugieren que podría usarse para tratar la endometritis bovina.
Glucógeno de ostra
El glucógeno de ostra originalmente sintetizado por células animales para el almacenamiento de energía es un polímero y tiene acción inmunomoduladora (80). Tiene la propiedad de atraer células PMN a la luz uterina (81). En vacas sanas, la migración de PMN a la luz uterina se acelera después de la administración intrauterina de glucógeno de ostra (OG), y los neutrófilos representan hasta el 90% de todas las células identificadas en las secreciones uterinas (82). Las dosis de OG que variaron de 0,1 a 10% en 60 ml del vehículo produjeron resultados similares, con un pico en el nivel de PMN 12 h después del tratamiento (81). Hubo concentraciones detectables de IgG en las secreciones uterinas después del tratamiento, pero no IgA; Las vacas ovariectomizadas tuvieron resultados similares después de las inyecciones de progesterona exógena y estrógeno (69).
10 mg/ml instilaron la administración intrauterina de glucógeno ostra (OG) para curar la endometritis subclínica en vacas cruzadas de reproducción repetida a informes anteriores (80). Aunque la tasa de recuperación fue mayor (p < 0,05) que el control (16,7%), no hubo diferencia significativa en la tasa de concepción entre los grupos tratado y control. A las 24 h después del tratamiento, las vacas tratadas tenían un TLC significativamente mayor (P0,01) que las vacas control. Desde el día del tratamiento, la infusión de OG resultó en una disminución significativa (p < 0,05) en los niveles plasmáticos de mediadores inflamatorios (LPO y NO; 71,58 ± 2,57, 76,67 ± 4,59 μmol/L) hasta el estro posterior (60,00 ± 2,06, 60,08 ± 2,17 μmol/L), respectivamente. Por lo tanto, el tratamiento con OG puede resolver no solo la endometritis subclínica en vacas cruzadas reproductoras repetidas, sino que también reduce las posibilidades de estrés oxidativo en el plasma sanguíneo debido a su efecto inmunomodulador. Se han realizado estudios similares en vacas endometríticas para determinar el efecto inmunomodulador del glucógeno de ostra (83). Administraron a las vacas en celo 500 mg de glucógeno de ostra en solución salina tamponada con fosfato intrauterino. El recuento de células nucleares polimorfas (PMN) en el líquido uterino aumentó significativamente (13,14 ± 1,35 vs. 73,71 ± 3,59) antes y después de 24 h de tratamiento. Después de la primera inseminación posterior al tratamiento, encontraron que las vacas con endometritis tenían una tasa de concepción del 60%, en comparación con el 70% en las vacas normales.
Leucotrieno B4
El metabolito del ácido araquidónico leucotrieno B4 (LT B4) es un potente quimioatrayente que puede inducir la migración de células nucleares polimorfas a la luz uterina bovina. Una sola infusión de 30 nmol/L de leucotrieno B4 puede aumentar la cantidad de células nucleares polimorfas intrauterinas hasta 5-10 veces en 24 h (84). Los PMN comprendían el 25-30% del recuento total de leucocitos antes de la estimulación; Después de la terapia, constituyeron el 85% del recuento total de leucocitos (85). Para el tratamiento de la endometritis subclínica en vacas cruzadas reproductoras recurrentes, Krishnan et al. (80) infundieron 50 ml de 30 nmol/L de leucotrieno B4 (LTB4) intrauterino. La tasa de recuperación fue mayor (83,3%; p < 0,05) que control (16,7%). El grupo tratado vio un aumento no significativo en la tasa de concepción en comparación con el grupo control. En comparación con las vacas control, las vacas tratadas mostraron mayor TLC (P0.01) 24 h después del tratamiento. Desde el día de la terapia, la infusión de LTB4 resultó en una disminución significativa (p < 0,05) en los niveles plasmáticos de mediadores inflamatorios (LPO y NO; 667,15 ± 42,85, 753,73 ± 32,78 nmol/L) hasta el estro posterior (555,56 ± 42,53, 630,88 ± 31,16 nmol/L), respectivamente. Informaron que administrar LTB4 a vacas cruzadas reproductoras repetidas cura la endometritis subclínica y reduce el estrés oxidativo, como se ve por niveles plasmáticos más bajos de LPO y NO después del tratamiento inmunomodulador.
Inmunomoduladores de origen vegetal
Varios inmunomoduladores de origen vegetal están disponibles para tratar trastornos reproductivos en bovinos. El efecto inmunomodulador se debe a la presencia del ingrediente activo en estas plantas. Los ingredientes activos como la alicina en el ajo (86), los sitoindosides VII-X y withaferin en ashwagandha (87), hidroalcohólicos e hidroacetónicos en neem (88) y el eugenol en tulsi (89) son algunos ejemplos que tienen propiedades antibacterianas y antifúngicas. Actualmente se están estudiando las propiedades inmunomoduladoras de varias plantas. La endometritis se ha tratado tradicionalmente con Cordifolia. Las vacas endometriósicas fueron tratadas con 50 ml (dosis total de 3,000 mg) de extractos acuosos de Tinospora cordifolia durante 3 días y vieron una tasa de recuperación del 66.67 por ciento y una tasa de concepción del 27.27 por ciento, respectivamente (90). Se encontró que nuevas sustancias antifúngicas, como Rosemarinus officinalis y Thymus vulgaris, tienen un buen impacto terapéutico, así como una capacidad inmunoestimulante y eliminadora de radicales libres, contra la endometritis micótica causada por Candida albicans (91). Otras plantas como el Neem se han utilizado por su actividad inmunomoduladora y terapéutica contra la endometritis (88). Los extractos de 30 ml de corteza hidroalcohólica de Neem y corteza hidroacetónica de Neem se administraron intrauterinos durante 7 días a partir del día del estro. Aunque se informó recuperación clínica y mejora de la concepción en ambos grupos, se concluyó que el extracto hidroalcohólico de Neem tenía un mejor valor terapéutico. Se sabe que algunas hierbas inmunomoduladoras, como Withenia somnifera, tienen un efecto gonadotrópico en animales, elevando el peso gonadal al aumentar el tamaño del folículo femenino y las capas de células del tubo seminífero masculino (92). Withenia somnifera mejora la actividad espermatogénica puede deberse al apoyo del eje hormonal hipotalámico-hipofisario-gonadal y al equilibrio de testosterona en los testículos (92). Además, Withenia somnifera aumenta la concentración de testosterona y progesterona en ratas macho y disminuye los triglicéridos y el colesterol en ratas macho y hembra (93) (Tabla 2).
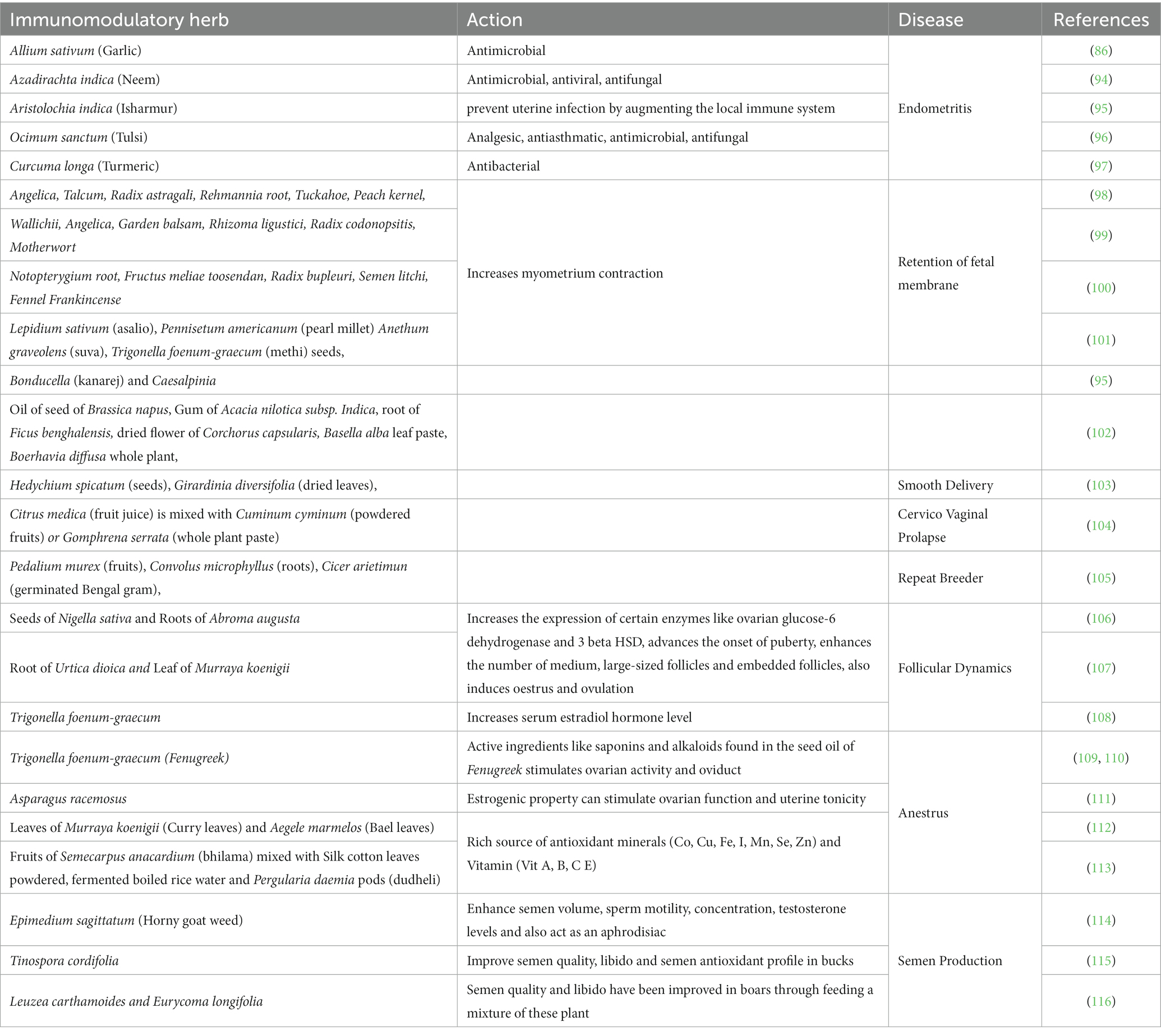 Tabla 2. Diferentes hierbas inmunomoduladoras y su acción utilizadas en diversos trastornos reproductivos.
Tabla 2. Diferentes hierbas inmunomoduladoras y su acción utilizadas en diversos trastornos reproductivos.
Conclusión
El fracaso reproductivo es la principal causa de infertilidad y se ha identificado como una enfermedad. Los antígenos de las hormonas reproductivas, los espermatozoides y los óvulos pueden contribuir al desarrollo de anticuerpos que pueden interferir con los receptores de las hormonas, inmovilizar los espermatozoides y, en última instancia, provocar inmunoinfertilidad. Esto resulta en anovulación, retraso en la ovulación, fracaso de la fertilización, involución uterina prolongada, intervalo de parto prolongado, estro posparto prolongado y reducción de la tasa de concepción. El nivel de estos anticuerpos puede disminuir en la sangre dando descanso sexual a las hembras, aplicando tecnologías de reproducción asistida y tratando a los animales con inmunomoduladores como LPS, glucógeno de ostra, etc.
Contribuciones del autor
VG: conceptualización y redacción. TM: conceptualización y revisión. MB: revisión y edición. RD: redacción, revisión y edición. RK: edición. DN: revisión y edición. MSe, RR, SD, NS y MSi: revisión. Todos los autores contribuyeron al artículo y aprobaron la versión presentada.
Conflicto de intereses
Los autores declaran que la investigación se llevó a cabo en ausencia de cualquier relación comercial o financiera que pudiera interpretarse como un posible conflicto de intereses.
Nota del editor
Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, o las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo, o reclamo que pueda ser hecho por su fabricante, no está garantizado ni respaldado por el editor.
Referencias
1. Brazdova, A, Senechal, H, Peltre, G, y Poncet, P. Aspectos inmunes de la infertilidad femenina. Int J Fertilidad y esterilidad. (2016) 10:1. doi: 10.22074/ijfs.2016.4762
Resumen de PubMed | Texto completo de CrossRef | Google Académico
2. Parkinson, TJ. Infertilidad en la vaca debido a deficiencias funcionales y de manejo. Veter Reprod Obstetricia WB Saunders. (2019) 2:361–407. doi: 10.1016/B978-0-7020-7233-8.00022-7
3. Wigby, S, Suarez, SS, Lazzaro, BP y Wolfner, Pizzari T MF (2019). Éxito de los espermatozoides e inmunidad. Curr Top Dev Biol 135: 287–313. doi: 10.1016/bs.ctdb.2019.04.002
Resumen de PubMed | Texto completo de CrossRef | Google Académico
4. Dhama, ASVK, Chakraborty, S, Abdul Samad, HK, Latheef, S, Sharun, K, Khurana, SK, et al. Papel de los anticuerpos antiespermatozoides en la infertilidad, el embarazo y el potencial para los diseños de vacunas anticonceptivas y antifertilidad: progreso de la investigación y visión pionera. Vacunas. (2019) 7:116. doi: 10.3390/vaccines7030116
5. Cooper, DW, y Larsen, E. Immunocontraception of mammalian wildlife: ecological and immunogenetic issues. Reproducción. (2006) 132:821–8. doi: 10.1530/REP-06-0037
Resumen de PubMed | Texto completo de CrossRef | Google Académico
6. Srivastava, SK, Shinde, S, Singh, SK, Mehrotra, S, Verma, MR, Singh, AK, et al. Anticuerpos antiespermatozoides en vacas reproductoras repetidas: frecuencia, detección y validación de niveles umbral empleando inmovilización de espermatozoides, aglutinación de espermatozoides y ensayo de inmunoperoxidasa. Reprod Domest Anim. (2017) 52:195–202. DOI: 10.1111/RDA.12877
Resumen de PubMed | Texto completo de CrossRef | Google Académico
7. Rashid Dar, R, Ali, A, Ahmad, SF, Kumar Singh, S, Patra, MK, Panigrahi, M, et al. Efecto inmunomodulador de la curcumina en la producción de prostaglandina E2 inducida por lipopolisacáridos y / o flagelinas y expresión relativa de citoquinas proinflamatorias en las células del estroma endometrial bubalina primarias. Reprod Domest Anim. (2019) 54:917–23. DOI: 10.1111/RDA.13435
8. Fayemi, O. Anticuerpos de esperma y eficiencia reproductiva en el ganado cebú en el suroeste de Nigeria. Pakistán Vet J. (2005) 25:111.
9. Mathur, S, Williamson, HO, Genco, PV, Rust, PF y Fundenberg, HH. La isoinmunidad de las hembras a los espermatozoides se asocia con la autoinmunidad de los espermatozoides en sus maridos. J Clin Immunol. (1985) 5:166–71. doi: 10.1007/BF00915507
Resumen de PubMed | Texto completo de CrossRef | Google Académico
10. Ferrer, MS, Laflin, S, Anderson, DE, Miesner, MD, Wilkerson, MJ, George, A, et al. Prevalencia de anticuerpos antiespermatozoides unidos a espermatozoides bovinos y su asociación con la calidad del semen. Teriogenología. (2015) 84:94–100. doi: 10.1016/j.theriogenology.2015.02.017
Resumen de PubMed | Texto completo de CrossRef | Google Académico
11. Sardoy, MC, Anderson, DE, George, A, Wilkerson, MJ, Skinner, S, and Ferrer, MS. Estandarization of a method to detect bovine sperm-bound antisperm antibodies by flow cytometry. Teriogenología. (2012) 78:1570–7. doi: 10.1016/j.theriogenology.2012.06.026
Resumen de PubMed | Texto completo de CrossRef | Google Académico
12. Lazarevic, M, Suljkanovic, A, Mickov, L, Sabanovic, M, Paprikic, N, y Mlinar, S. La influencia de los anticuerpos antiespermatozoides Ig G e Ig a de sueros de vaca y moco cervical sobre la motilidad de los espermatozoides de toro. Acta Vet-Beogr. (2013) 63:499–511. doi: 10.2298/AVB1306499L
13. Archana, SS, Selvaraju, S, Binsila, BK, Arangasamy, A, y Krawetz, SA. Moléculas inmunoreguladoras como modificadores del semen y la fertilidad: una revisión. Mol Reprod Dev. (2019) 86:1485–504. DOI: 10.1002/MRD.23263
Resumen de PubMed | Texto completo de CrossRef | Google Académico
14. Sheldon, IM, Noakes, DE, Rycroft, AN, Pfeiffer, DU, and Dobson, H. Influence of uterine bacterial contamination after parturition on ovarian dominant follicle selection and follicle growth and function in cattle. Reproducción. (2002) 123:837–45. doi: 10.1530/rep.0.1230837
15. Beutler, B, Hoebe, K, Du, X, y Ulevitch, RJ. Cómo detectamos microbios y respondemos a ellos: los receptores tipo toll y sus transductores. J Leukoc Biol. (2003) 74:479–85. DOI: 10.1189/JLB.0203082
Resumen de PubMed | Texto completo de CrossRef | Google Académico
16. Herath, S, Williams, EJ, Lilly, ST, Gilbert, RO, Dobson, H, Bryant, CE, et al. Las células foliculares ováricas tienen capacidades inmunes innatas que modulan su función endocrina. Reproducción. (2007) 134:683–93. doi: 10.1530/REP-07-0229
Resumen de PubMed | Texto completo de CrossRef | Google Académico
17. Magata, F. Lipopolysaccharide-induced mechanisms of ovarian dysfunction in cows with uterine inflammatory diseases. J Reprod Dev. (2020) 66:311–7. DOI: 10.1262/JRD.2020-021
Resumen de PubMed | Texto completo de CrossRef | Google Académico
18. Shibahara, H, Shiraishi, Y, and Suzuki, M. Diagnosis and treatment of immunologically infertile male with antisperm antibodies. Reprod Med Biol. (2005) 4:133–41. doi: 10.1111/j.1447-0578.2005.00102.x
19. Jain, P, Ojha, SK, Kumar, V, Bakhshi, S, Singh, S, and Yadav, S. Differential seminal plasma proteome signatures of acute lymphoblastic leukemia survivors. Reprod Biol. (2019) 19:322–28. doi: 10.1016/j.repbio.2019.11.002
20. Robertson, S.A., y Sharkey, DJ. El papel del semen en la inducción de la tolerancia inmune materna al embarazo. Semin Immunol. (2001) 13:243–54. doi: 10.1006/SMIM.2000.0320
21. Hagaman, JR, Moyer, JS, Bachman, ES, Sibony, M, Magyar, PL, Welch, JE, et al. Enzima convertidora de angiotensina y fertilidad masculina. Proc Natl Acad Sci. U S A. (1998) 95:2552–557. DOI: 10.1073/PNAS.95.5.2552
22. Evans, JP. Las bases moleculares de las interacciones de la membrana espermatozoide-ovocitos durante la fertilización de mamíferos. Actualización de Hum Reprod. (2002) 8:297–311. doi: 10.1093/humupd/8.4.297
Resumen de PubMed | Texto completo de CrossRef | Google Académico
23. Narciandi, F, Fernandez-Fuertes, B, Khairulzaman, I, Jahns, H, King, D, Finlay, EK, et al. La beta-defensina 126 que recubre espermatozoides es un dímero resistente a la disociación producido por el epitelio epididimario en el tracto reproductivo bovino. Biol Reprod. (2016) 95:121–1. doi: 10.1095/biolreprod.116.138719
Resumen de PubMed | Texto completo de CrossRef | Google Académico
24. Prasad, SV, Wilkins, B, Skinner, SM, and Dunbar, BS. Evaluating zone pellucida structure and function using antibodies to rabbit 55 kDa ZP protein expressed in baculovirus expression system. Gameto Res. (1996) 43:519–29. doi: 10.1002/(SICI)1098-2795(199604)43:4<519::AID-MRD15>3.0.CO; 2-U
Resumen de PubMed | Texto completo de CrossRef | Google Académico
25. Bratanov, K, Dikov, V, Radex, G, y Danov, D. Studies on the immunology of reproduction. VII. El papel de los anticuerpos espermáticos en la inseminación de vacas con involución uterina incompleta y vacas con involución uterina incompleta y vacas con endometritis latente. Medicina veterinaria. Nauki, Sof. (1965) 2:323–31.
26. Griffin, JFT, Nunn, WR, y Hartigan, PJ. Una respuesta inmune al diluyente de semen de yema de huevo en vacas lecheras. Reproducción. (1971) 25:193–9. DOI: 10.1530/JRF.0.0250193
Resumen de PubMed | Texto completo de CrossRef | Google Académico
27. Ahuja, AK, Cheema, RS, and Kumar, A. Status of naturally developing antisperm antibodies in serum of terneros, vaquillas, cows and their effect on in vitro capacitation and acrosome reaction. J Bio Innov. (2016) 5:874–89.
28. Bronson, RA. Anticuerpos antiespermatozoides: una evaluación crítica y guías clínicas. J Reprod Immunol. (2000) 45:159–83. doi: 10.1016/S0165-0378(99)00044-3
Resumen de PubMed | Texto completo de CrossRef | Google Académico
29. Vlok, I, Ferrer, M, Sardoy, M, Anderson, D, and Koopman, T. Serum anti-sperm antibodies associated with orcitis in a bull. Theriogenol clínico. (2009) 1:251.
30. Bronson, R. Biología del tracto reproductor masculino: sus consideraciones celulares y morfológicas. Am J Reprod Immunol. (2011) 65:212–9. doi: 10.1111/j.1600-0897.2010.00944.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
31. Blayney, DP, Dyck, J, y Harvey, D. Economic effects of animal diseases linked to trade dependency. Olas ámbar. (2006) 4:22.
32. Shibahara, H, y Koriyama, J. Métodos para pruebas directas e indirectas de anticuerpos antiespermatozoides en: Spermatogenesis. Totowa, NJ: Humana Press (2013). 51–60.
33. Gupta, VK, Srivastava, SK, Ghosh, SK, Srivastava, N, Singh, G, Verma, MR, et al. Efecto de las hormonas endógenas, anticuerpos antiespermatozoides y estrés oxidativo sobre la calidad del semen de toros cruzados. Anim Biotechnol. (2022) 33:1441–8. doi: 10.1080/10495398.2021.1905656
34. Dondero, F, Gandini, L, Lombardo, F, Salacone, P, Caponecchia, L, y Lenzi, A. Antisperm antibody detection: 1. Methods and standard protocol. Am J Reprod Immunol. (1997) 38:218–23. doi: 10.1111/j.1600-0897.1997.tb00302.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
35. Mazumdar, S, y Levine, AS. Anticuerpos antiespermatozoides: etiología, patogénesis, diagnóstico y tratamiento. Esterilidad fertilizante. (1998) 70:799–810. doi: 10.1016/S0015-0282(98)00302-1
36. Vigano, P, Fusi, FM, Brigante, C, Busacca, M y Vignali, M. Separación inmunomagnética de espermatozoides humanos marcados con anticuerpos de espermatozoides humanos libres de anticuerpos como tratamiento para la infertilidad inmunológica. informe preliminar Andrologia. (1991) 23:367–71. doi: 10.1111/j.1439-0272.1991.tb02582.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
37. Naz, RK. Modalidades para el tratamiento de la infertilidad mediada por anticuerpos antiespermatozoides: nuevas perspectivas. Am J Reprod Immunol. (2004) 51:390–7. doi: 10.1111/j.1600-0897.2004.00174.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
38. Gupta, VK, Srivastava, SK, Ghosh, SK, Srivastava, N, Katiyar, R, Verma, M, et al. Efecto del zinc seminal, calcio, estrés oxidativo y perfil proteico en la calidad del semen de toros cruzados. J Animal Res. (2020) 10:347–52. doi: 10.30954/2277-940X.03.2020.3
39. Kumar, N, Verma, RP, Singh, LP, Varshney, VP, y Dass, RS. Efecto de diferentes niveles y fuentes de suplementación de zinc sobre los atributos cuantitativos y cualitativos del semen y el nivel de testosterona sérica en toros cruzados de ganado vacuno (Bos indicus $\bf\times $ Bos taurus). Reprod Nutr Dev. (2006) 46:663–75. doi: 10.1051/rnd:2006041
Resumen de PubMed | Texto completo de CrossRef | Google Académico
40. Swangchan-Uthai, T, Lavender, CR, Cheng, Z, Fouladi-Nashta, AA, y Wathes, DC. Evolución temporal de los mecanismos de defensa en el endometrio bovino en respuesta al lipopolisacárido. Biol Reprod. (2012) 87:135–1. doi: 10.1095/biolreprod.112.102376
Resumen de PubMed | Texto completo de CrossRef | Google Académico
41. Ibrahim, M, Peter, S, Wagener, K, Drillich, M, Ehling-Schulz, M, Einspanier, R, et al. Las células epiteliales endometriales bovinas escalan su respuesta proinflamatoria in vitro a la patógena Trueperella pyogenes aislada del útero bovino de una manera específica para cada cepa. Las células frontales infectan microbiol. (2017) 7:264. DOI: 10.3389/fcimb.2017.00264
Resumen de PubMed | Texto completo de CrossRef | Google Académico
42. Arias, LAQ, Fernández, MV, Gonzalez, JJB, Lopez, MB, Herradón, PJG, y Martinez, AIP. Endometritis subclínica en ganado lechero. Nuevos conocimientos sobre. Teriogenología. (2018):79–97. doi: 10.5772/intechopen.74197
43. Azawi, OI. Infección uterina posparto en bovinos. Anim Reprod Sci. (2008) 105:187–208. doi: 10.1016/j.anireprosci.2008.01.010
44. Sheldon, IM, Price, SB, Cronin, J, Gilbert, RO y Gadsby, JE. Mecanismos de infertilidad asociados con endometritis clínica y subclínica en ganado lechero de alta producción. Reprod Domest Anim. (2009) 44:1–9. doi: 10.1111/j.1439-0531.2009.01465.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
45. Pasolini, MP, Prete, CD, Fabri, S, and Auletta, L. Endometritis and infertility in yegues-the challenge in the equine breeding industry-a review. Infert de infección genital. (2016):285–328. DOI: 10.5772/62461
46. Studer, E (1981). Algunos medicamentos son de poco valor 21, 32 o incluso perjudiciales. 9 Dependiendo. En Actas de la reunión anual (p. 4). La Sociedad.
47. El-Azab, MA, Whitmore, HL, Kakoma, I, Brodie, BO, McKenna, DJ, y Gustafsson, BK. Evaluación del ambiente uterino en metritis bovina experimental y espontánea. Teriogenología. (1988) 29:1327–34. doi: 10.1016/0093-691X(88)90012-X
48. Callahan, CJ, y Horstman, LA. Tratamiento de la metritis posparto en vacas lecheras causada por Actinomyces pyogenes. Practicante bovino. (1993) 27:162–5.
49. Dohmen, MJW, Lohuis, JACM, Gy, H, Nagy, P, y Gacs, M. La relación entre bacteriología y hallazgos clínicos en vacas con endometritis subaguda/crónica. Teriogenología. (1995) 43:1379–88. doi: 10.1016/0093-691X(95)00123-P
50. Gruys, E, Van Ederen, AM, Alsemgeest, SM, Kalsbeek, HC, and Wensing, T. Acute phase protein values in blood of cattle as indicator of animals with pathological processes. Arch Lebensmittelhyg. (1993) 44:107–11.
51. Vandeplassche, M (1984). Estimulación e inhibición de la fagocitosis en animales domésticos. En: Actas del 10º congreso internacional sobre reproducción animal e IA. Urbana, Champaign, III, pp. 475-477.
52. Morrow, DA. Actividad ovárica posparto e involución del útero y cuello uterino en bovinos lecheros. Ámbito veterinario. (1969) XIV:2-13.
53. Vandeplassche, M. Nuevos aspectos comparativos de la involución y la metritis puerperal en yegua, vaca y cerda. (1981) 36:804–7.
54. Shoushtari, SMA, Rezaie, SA, Khaki, A, Belbasi, A y Tahmasebian, H. Contenido de calcio y magnesio del líquido uterino y el suero sanguíneo durante el ciclo estral y la fase prepuberal en búfalos de agua En: Foro de investigación veterinaria, vol. 54. Urmia, Irán: Facultad de Medicina Veterinaria, Universidad de Urmia (2014). 301.
55. Lulay, AM (2011). Efectos de la prostaglandina F2 alfa sobre las poblaciones de neutrófilos, la salud uterina y el rendimiento reproductivo en vacas lecheras. Estados Unidos: M.Sc Tesis, Universidad Estatal de Oregón.
56. Dhaliwal, GS, Murray, RD, y Woldehiwet, Z. Algunos aspectos de la inmunología del útero bovino relacionados con los tratamientos para la endometritis. Anim Reprod Sci. (2001) 67:135–52. doi: 10.1016/S0378-4320(01)00124-5
Resumen de PubMed | Texto completo de CrossRef | Google Académico
57. Gilbert, RO, Grohn, YT, Miller, PM, y Hoffmann, DJ. El efecto de la paridad sobre la función periparto de neutrófilos en vacas lecheras. Veterinario Immunol Immunopathol. (1993) 36:75–82. doi: 10.1016/0165-2427(93)90007-Q
Resumen de PubMed | Texto completo de CrossRef | Google Académico
58. Corbeil, LB, Schurig, JR, Duncan, JR, Corbeil, RR, y Winter, AJ. Clases de inmunoglobulinas y función biológica de los anticuerpos fetales de Campylobacter (Vibrio) en suero y moco cervicovaginal. Infectar inmune. (1974) 10:422–9. DOI: 10.1128/IAI.10.3.422-429.1974
Resumen de PubMed | Texto completo de CrossRef | Google Académico
59. Watson, ED, Diehl, NK, y Evans, JF. Respuesta de anticuerpos en el tracto genital bovino a la infusión intrauterina de Actinomyces pyogenes. Res Vet Sci. (1990) 48:70–5. doi: 10.1016/S0034-5288(18)31512-1
Resumen de PubMed | Texto completo de CrossRef | Google Académico
60. Whitmore, HL, y Archbald, LF. Demostración y cuantificación de inmunoglobulinas en suero bovino, líquido folicular y secreciones uterinas y vaginales con referencia a la diarrea viral bovina. Am J Vet Res. (1977) 38:455–7.
61. Georgiv, S. Estudio de la respuesta inmunológica general y el contenido microbiano del útero de vacas en el período puerperal. Ciencias Veterinarias (1978) 15:69–77.
62. Aknazarov, BK. Estudio de factores humorales de función protectora local en vacas. Veterinario Dermatol. (1988) 8:41–3.
63. Butt, BM, Bessre, TE, y Senger, PLPR. Anticuerpo específico contra Haemophilus somnus en el útero bovino después de la inmunización intramuscular. Infectar inmune. (1993) 61:2558–62. DOI: 10.1128/IAI.61.6.2558-2562.1993
Resumen de PubMed | Texto completo de CrossRef | Google Académico
64. Bouters, R, y Vandeplassche, M. Postpartum infection in cattle. Diagnóstico y tratamiento preventivo y curativo. J S Afr Vet Assoc. (1977) 48:237–9.
65. Vandeplassche, M, y Bouters, R (1981). El impacto de los problemas ginecológicos y obstétricos resultantes del embarazo y el parto. Seminario CEE Factores que influyen en la fecundidad en el posparto, 30 de septiembre-3 de octubre.
66. Carleton, CL, y Threfall, WR (1984) Determinación de cambios en la tasa de absorción y cambios histológicos del endometrio después de la infusión intrauterina de Lugol de la vaca posparto. En: Proceedings of the 10th international congress on animal reproduction and AI. Urbana, Champaign, III. 412–418.
67. Gustafsson, BK. Estrategias terapéuticas que implican el tratamiento antimicrobiano del útero de animales grandes. J Am Vet Med Assoc. (1984) 185:1194–8.
68. Nakao, T, Moriyoshi, M, and Kawata, K. Effect of postpartum intrauterine treatment with 2% polyvinyl-pyrrolidone-iodine solution on reproductive efficiency in cows. Teriogenología. (1988) 30:1033–43. doi: 10.1016/0093-691X(88)90277-4
Resumen de PubMed | Texto completo de CrossRef | Google Académico
69. Chacin, ML, Hansen, PJ, and Drost, M. Effects of stage of the estrous cycle and steroid treatment on uterine immunoglobulin content and polymorphonuclear leukocytes in cattle. Teriogenología. (1990) 34:1169–84. doi: 10.1016/S0093-691X(05)80016-0
70. Al-Eknah, MM, y Noakes, DE. Actividad uterina en vacas durante el ciclo estral, después de la ovariectomía y después del estradiol exógeno y la progesterona. H. Veterinario J. (1989) 145:328–36. DOI: 10.1016/0007-1935(89)90030-4
Resumen de PubMed | Texto completo de CrossRef | Google Académico
71. Guyton, AC. El sistema linfático en: Libro de texto de fisiología médica. 8ª ed. Filadelfia: Saunders (1991). 180–4.
72. Guilbaut, LA, Thatcher, WW, Drost, M, and Hopkins, SM. Source of F series prostaglandins during the early postpartum period in cattle. Biol Reprod. (1984) 31:879–87. doi: 10.1095/biolreprod31.5.879
Resumen de PubMed | Texto completo de CrossRef | Google Académico
73. Cooke, RG, Ahmad, N, and Nicholson, T. Effect of progesterone and estradiol-17 on oxytocin-induced PGF2 release and endometrial oxytocin receptor concentration in ovariectomized goats. Prostaglandinas otras mediatas lipídicas. (1998) 55:109–20. doi: 10.1016/S0090-6980(98)00013-6
74. Fredriksson, G, Kindahl, H, Sandstedt, K, y Edqvist, LE. Hallazgos bacterianos intrauterinos y liberación de PGF2 en la vaca lechera posparto. Zbl vet-med A. (1985) 32:368–80.
75. Bolinder, A, Seguin, B, Kindahl, H, Bouley, D, and Otterby, D. Retained fetal membranes in cows: manual removal versus non-removal and its effect on reproductive performance. Teriogenología. (1988) 30:45–56. doi: 10.1016/0093-691X(88)90262-2
Resumen de PubMed | Texto completo de CrossRef | Google Académico
76. Lindell, JO, y Kindahl, H. La prostaglandina exógena F2 promueve la involución uterina en la vaca. Acta Vet Scand. (1983) 24:269–74. doi: 10.1186/BF03546730
Resumen de PubMed | Texto completo de CrossRef | Google Académico
77. Paisley, LG, Mickelsen, WD y Anderson, PB. Mecanismos y terapia para las membranas fetales retenidas y las infecciones uterinas de las vacas: una revisión. Teriogenología. (1986) 25:353–81. doi: 10.1016/0093-691X(86)90045-2
Resumen de PubMed | Texto completo de CrossRef | Google Académico
78. Asbury, AC, y Hansen, PJ. Efectos de la susceptibilidad de las yeguas a la endometritis y etapa del ciclo sobre la actividad fagocítica de neutrófilos de origen uterino. J Reprod Fertil Suppl. (1987) 35:311–6.
79. Targowski, SP (1984). Inflamación uterina inducida inmunológicamente en 10. Congreso internacional sobre reproducción animal e inseminación artificial, Universidad de Illinois en Urbana-Champaign, Illinois (EE.UU.), 10-14 de junio de 1984. Universidad de Illinois en Urbana-Champaign.
80. Krishnan, BB, Kumar, H, Mehrotra, S, Singh, SK, Goswami, TK, Khan, FA, et al. Efecto del leucotrieno B4 y el glucógeno de ostra en la resolución de la endometritis subclínica en vacas cruzadas de reproducción repetida. Indio J Animal Res. (2015) 49:218–22. doi: 10.5958/0976-0555.2015.00112.0
81. Anderson, KL, Hamida, NA, Frank, A, Whitmore, HL, y Gustafsson, BK. Recolección y evaluación fagocítica de leucocitos neutrófilos uterinos. Teriogenología. (1985) 24:305–17. doi: 10.1016/0093-691X(85)90221-3
82. Subandrio, AL, y Noakes, DE. Migración de neutrófilos en la luz uterina de la vaca: la influencia de las hormonas esteroides sexuales endógenas utilizando dos quimioatrayentes intrauterinos. Teriogenología. (1997) 47:825–35. doi: 10.1016/S0093-691X(97)00038-1
Resumen de PubMed | Texto completo de CrossRef | Google Académico
83. Biswal, SS, Das, S, and Mohanty, DN. Immunomodulatory effect of oyster glycogen on endometritic crossbreed cows. Indio J Animal Reprod. (2013) 34:21–4.
84. Zerbe, H, Schuberth, HJ, Hoedemaker, M, Grunert, E, y Leibold, W. Un nuevo sistema modelo para la endometritis: conceptos básicos y caracterización de las propiedades fenotípicas y funcionales de los neutrófilos uterinos bovinos. Teriogenología. (1996) 46:1339–56. doi: 10.1016/S0093-691X(96)00314-7
85. Hughes, JP y Couto, MA (1989). Endometritis en la yegua. En el 11º congreso internacional sobre reproducción animal e inseminación artificial, campus de Belfield, University College Dublin (Irlanda), 26-30 de junio de 1988.
86. Bnh, S, Prerna, L, Humtsoe, H, y Mishra, A. Antibacterial activity of garlic against bacillus subtilis. Int Rev App Biotechnol Biochem. (2014) 2:107–19.
87. Umadevi, M, Rajeswari, R, Rahale, CS, Selvavenkadesh, S, Pushpa, R, Kumar, KS, et al. Usos tradicionales y medicinales de Withania somnifera. Pharma Innov. (2012) 1:102.
88. Kumar, H, Singh, B, Goswami, TK, y Rawat, M. Use of neem preparation for the treatment of endometritis in cows. Adv Anim Vet Sci. (2013) 1:194–96.
89. Bhatt, MK, Shankar, MB, Saluja, AK, Dholwani, KK, y Capitán, AD. Evaluación de la actividad antimicrobiana del extracto metanólico de Ocimum Sanctum. J Pharmaceutical Scientific Innov. (2012) 1:39–41.
90. Kumar, P, Srivastava, SK, Rawat, M, Yadav, MC, and Kumar, H. Effect of certain immunomodulators on uterine infections and fertility in post partum buffaloes. Asia-Australas J Anim Sci.. (2004) 17:930–35. DOI: 10.5713/AJAS.2004.930
91. Hanafi, EM, Abdel-khader, MM, Kassem, SS, y Danial, EN. Aromaterapia para la endometritis inducida por candida albicans. Int J Acad Res. (2010) 2:112–9.
92. Kumar, A, Kumar, R, Rahman, MS, Iqubal, MA, Anand, G, Niraj, PK, et al. Efecto fitorremedial de Withania somnifera contra la toxicidad testicular inducida por arsénico en ratas Charles Foster. Avicena J Phytomed. (2015) 5:355–64.
93. Saiyed, A, Jahan, N, Makbul, SAA, Ansari, M, Bano, H, and Habib, SH. Effect of combination of Withania somnifera Dunal and Tribulus terrestris Linn on letrozole induced polycystic ovarian syndrome in rats. Integrative Med Res. (2016) 5:293–300. doi: 10.1016/j.imr.2016.10.002
Resumen de PubMed | Texto completo de CrossRef | Google Académico
94. Sarkar, P, Patra, MK, and Kumar, H. Strategic treatment with immunomodulators to resolve endometritis in cow: a review. Agric Rev. (2016) 37:186–95.
95. Ali Sagar, HA, y Pandey, SK Karla (2003) Optimization of reproductive health through herbs. XIX convención anual y simposio nacional sobre tecnologías reproductivas actuales para mejorar la producción ganadera en la India, Calcuta.
96. Mandhwani, R, Bhardwaz, A, Kumar, S, Shivhare, M, and Aich, R. Insights into bovine endometritis with special reference to phytotherapy. Mundo Veterinario. (2017) 10:1529–32. doi: 10.14202/vetworld.2017.1529-1532
Resumen de PubMed | Texto completo de CrossRef | Google Académico
97. Rathaur, P, Raja, W, Ramteke, PW, y John, SA. Cúrcuma: la especia dorada de la vida. Int J Pharmaceutical Sci Res. (2012) 3:1987–94.
98. Chen, G, Lin, C y Wu, B (2015). La composición medicinal tradicional china utilizada para retener la placenta bovina después del parto, comprende Angélica, talco, raíz de Rehmannia, Radix astragali, Tuckahoe, semilla de melocotón, agripalma, Radix codonopsitis, cártamo y regaliz. Patente NO. CN104352628.
99. Li, H, Wang, X, Tian, W, Cao, R, y Cong, X (2015). Composición medicinal tradicional china útil para, por ejemplo, El tratamiento de la placenta retenida y el fortalecimiento de las contracciones uterinas en el ganado, contiene Angélica, bálsamo de jardín, Rhizoma ligustici wallichii, Radix codonopsitis y agripalma. Patente No. CN104173660, 2015.
100. Sarswat, CS, y Purohit, GN. Uso de la medicina etnoveterinaria para la terapia de trastornos reproductivos en bovinos. J Entomol Zoolog Stud. (2020) 8:1006–16.
102. Kumar, R, y Bharati, KA. Nuevas afirmaciones en medicamentos veterinarios populares de Uttar Pradesh, India. J Etnofarmacol. (2013) 146:581–93. doi: 10.1016/j.jep.2013.01.030
Resumen de PubMed | Texto completo de CrossRef | Google Académico
103. Kumar, D, Tripathi, HC, Tandon, SK, Chandra, S, Jawaharlal, A, y Malick, JK. Medicamentos veterinarios a base de hierbas populares empleados en trastornos reproductivos y para mejorar la producción de leche en India y Nepal: una actualización. Indio J Anim Sci. (1999) 69:953–7.
104. Ali, ZA. Medicina veterinaria popular en el distrito de Moradabad (Uttar Pradesh), India. Fitoterapia. (1999) 70:340–7. doi: 10.1016/S0367-326X(99)00039-8
105. Das, P, Das, SK, Arya, HPS, Subba Reddy, G, y Mishra, A. Veterinary science and animal husbandry In: Inventory of indigenous technical knowledge in agriculture, Document-1. Nueva Delhi: ICAR (2002). 185–285.
106. Kabir, KK, Varshney, JP, Rawal, CVS, Srivastava, RS, y Ansari, MR. Comparative efficacy of herbal preparation in the management of anoestrus in non-descriptive rural buffaloes. Indio J Animal Reprod. (2001) 22:143–5.
107. Perumal, P, Veeraselvam, M, y Nahak, AK. Tratamiento a base de hierbas en reproducción animal. Int J Gestión del estrés de los recursos biológicos. (2013) 4:460–7.
108. Rajkumar, R (2004). Estudios sobre la eficacia de la inducción del celo de ciertas plantas medicinales y fármacos homeopáticos en vacas anoestres. Tesis de maestría en ciencias presentada al IVRI, Deemed University, Izatnagar, U.P., India, 2004.
109. Hassan, AM, Khalil, WKB, y Ahmed, KA. Estudio genético y patológico sobre el efecto del fenogreco sobre la cinética del tejido de ratones. Medicina Veterinaria J. (2006) 54:189–204.
110. Mohammed, Ahmed Beyan. Efecto de las semillas de fenogreco (Trigonella foenumgraecum) como aditivo para piensos en el rendimiento de producción de cabras lecheras, Ph.D. trabajo de tesis, NDRI, Karnal, (2009).
111. Kumar, S, Mehla, RK, Gupta, AK, y Meena, RK. Influencia de la suplementación con espárragos racemosus (Shatavari) durante diferentes etapas de la lactancia en el comportamiento del estro y el rendimiento reproductivo en vacas cruzadas de papas fritas Karan. Livest Res Rural Dev. (2010) 22:125–38.
112. Kumawat, B, Das, G, Narayanan, K, Mehrotra, S, Prasad, J, Ghosh, S, et al. Efecto de Aegle Marmelos y Murraya Koenigii sobre la inducción del celo, la concepción y la tasa de parto en novillas puberales retrasadas en condiciones de campo. Indio J Animal Reprod. (2016) 37:17–19.
113. Kumar, A, Katiyar, R, Ahmad, SF, Balamurugan, B, Deepak, D, y Prasad, JK. Aspectos actuales del tratamiento de los trastornos reproductivos bovinos. Theriogenol Insight-An Int J Reprod Animales. (2018) 8:101–9. doi: 10.30954/2277-3371.03.2018.2
114. Rost, A. Natural Healing Wisdom & Know how: Prácticas útiles, recetas y fórmulas para una vida de salud. Nueva York: Black Dog & Leventhal Pub (2009). 90 págs.
115. Jayaganthan, P, Perumal, P, Balamurugan, TC, Verma, RP, Singh, LP, Pattanaik, AK, et al. Efectos de la suplementación con Tinospora cordifolia sobre la calidad del semen y el perfil hormonal en carneros. Anim Reprod Sci. (2013) 140:47–53. doi: 10.1016/j.anireprosci.2013.05.003
Resumen de PubMed | Texto completo de CrossRef | Google Académico
116. Frydrychova, S, Opletal, L, Macakova, K, Lustykova, A, Rozkot, M, y Lipensky, J. Effects of herbal preparation on libido and semen quality in jabalíes. Reprod Domest Anim. (2011) 46:573–8. doi: 10.1111/j.1439-0531.2010.01703.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
Palabras clave: bovino, endometritis, inmunoinfertilidad, inmunomoduladores, LPS
Cita: Gupta VK, Mohanty TK, Bhakat M, Dewry RK, Katiyar R, Nain D, Shah N, Sethi M, Rautela R, Singh M y Deori S (2023) Inmunoinfertilidad reproductiva bovina: patogénesis e inmunoterapia. Frente. Vet. Sci. 10:1248604. doi: 10.3389/fvets.2023.1248604
Recibido: 27 de junio de 2023; Aprobado: 14 de septiembre de 2023;
Publicado: 05 octubre 2023.
Editado por:
Omer Ucar, Universidad Muğla Sıtkı Koçman, Türkiye
Revisado por:
Petru Rosca, Ion Ionescu de la Brad Universidad de Ciencias Agrícolas y Medicina Veterinaria de Iași, Rumania Stefan Gregore Ciornei, Ion Ionescu de la Brad Universidad de Ciencias Agrícolas y Medicina Veterinaria de Iași, Rumania
Derechos de autor © 2023 Gupta, Mohanty, Bhakat, Dewry, Katiyar, Nain, Shah, Sethi, Rautela, Singh y Deori. Este es un artículo de acceso abierto distribuido bajo los términos de la Licencia de Atribución Creative Commons (CC BY). S
*Correspondencia: Vinod Kumar Gupta, vinodkumargupta123439@gmail.com; Raju Kumar Dewry, de rajudewry@gmail.com; Rahul Katiyar, rahul.katiyarvet@gmail.com
†ORCID: Raju Kumar Dewry, https://orcid.org/0000-0001-8771-939X
Renuncia: Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, o las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo o reclamo que pueda ser hecho por su fabricante no está garantizado ni respaldado por el editor.
Date de alta y recibe nuestro 👉🏼 Diario Digital AXÓN INFORMAVET ONE HEALTH
Date de alta y recibe nuestro 👉🏼 Boletín Digital de Foro Agro Ganadero
Noticias animales de compañía
Noticias animales de producción
Trabajos técnicos animales de producción
Trabajos técnicos animales de compañía