Stents nasofaríngeos impresos en 3D específicos para cada paciente en perros: un estudio piloto cadavérico
 Craig Sutter1*†
Craig Sutter1*† Brian Hardy2†
Brian Hardy2† Steven Lucero3
Steven Lucero3 Lynelle Johnson2
Lynelle Johnson2 William Culp4
William Culp4- 1Hospital Docente de Medicina Veterinaria, Universidad de California, Davis, Davis, CA, Estados Unidos
- número arábigoDepartamento de Medicina y Epidemiología, Universidad de California, Davis, Davis, CA, Estados Unidos
- 3Departamento de Ingeniería Biomédica, Universidad de California, Davis, Davis, CA, Estados Unidos
- 4Departamento de Ciencias Quirúrgicas y Radiológicas, Universidad de California, Davis, Davis, CA, Estados Unidos
Fondo: Las opciones de tratamiento disponibles actualmente para la estenosis nasofaríngea y la nasofaringe imperforada en perros y gatos están plagadas de complicaciones y fracasos.
Objetivo: Desarrollar stents nasofaríngeos específicos para cada paciente utilizando moldes impresos en 3D y evaluar la colocación y el ajuste de los stents dentro de la nasofaringe.
Animales: Seis cadáveres caninos.
Métodos: Se generaron stents nasofaríngeos de silicona específicos para cada paciente utilizando moldes impresos en 3D basados en tomografías computarizadas. Se desarrolló un protocolo de colocación. Después de la colocación, se evaluó la bondad del ajuste dentro de la nasofaringe y se comparó con los métodos utilizados actualmente. Se compararon las propiedades mecánicas de los stents de silicona con los stents basados en catéter y nitinol.
Resultados: El desarrollo y la colocación de stents fueron exitosos en los seis cadáveres. Los stents de silicona ofrecían una rigidez (fuerza requerida para la compresión, N) y una deformación post-carga comparable a la de los stents de nitinol (1,8-6,2 vs. 1,2-3,3 N y 0,02-0,08 vs. 0,01-0,14 mm, respectivamente). Los stents específicos del paciente ofrecieron un ajuste superior en la nasofaringe (81-90%) en comparación con los catéteres bilaterales de goma roja (16,2-33,8%).
Conclusión: El desarrollo y la colocación de stents específicos para cada paciente mediante moldes impresos en 3D fueron exitosos en los seis cadáveres. Los nuevos stents mostraron propiedades mecánicas similares y una bondad de ajuste superior en comparación con los stents disponibles comercialmente, lo que podría ofrecer una mejor alternativa a los stents disponibles comercialmente. Se necesitan más investigaciones en animales con estenosis nasofaríngea para determinar la eficacia y evaluar la utilidad en pacientes vivos.
Introducción
La estenosis nasofaríngea (NPS) y la nasofaringe imperforada (INP) son procesos patológicos poco frecuentes, pero clínicamente significativos, en perros y gatos. Estas enfermedades dan lugar a la oclusión parcial o completa de la nasofaringe, lo que provoca una disminución o ausencia del flujo de aire a través de la nasofaringe y, posteriormente, del resto de las vías respiratorias. Los signos clínicos son comunes y a menudo se manifiestan como respiración bucal, dificultad respiratoria, estertor, arcadas y secreción nasal crónica.
Se han descrito numerosos métodos de tratamiento, como la corrección quirúrgica o la extirpación de tejido anormal, la ablación con láser y la colocación de stents en la región estenótica (1). En la actualidad, la dilatación con balón con o sin stent se recomienda a menudo como tratamiento de elección, pero presenta una tasa de fracaso de hasta el 50% en gatos y el 100% en perros (2). Las opciones de colocación de stents reportadas han incluido stents metálicos cubiertos o descubiertos y stents temporales no metálicos (por ejemplo, tubos torácicos o catéteres de goma roja) (1, 3, 4). Si bien las técnicas actuales de colocación de stents tienden a dar lugar a una mejoría inmediata de los signos clínicos, están plagadas de complicaciones a corto y largo plazo, como infección, atrapamiento de cuerpo extraño, colapso del stent, fractura del stent, migración del stent y el desarrollo de fístulas oronasales (1, 2, 5, 6). Los stents también suelen tener un crecimiento de la mucosa nasofaríngea, lo que dificulta enormemente su extracción sin intervención quirúrgica (2). La dilatación con balón por sí sola también ofrece un alivio clínico inmediato, pero este procedimiento conlleva una alta tasa de recurrencia (1). Dadas las numerosas y frecuentes complicaciones con los stents disponibles actualmente, se necesita más investigación sobre opciones alternativas de colocación de stents.
Recientemente, la literatura de medicina humana se ha centrado en el uso de la impresión 3D para el desarrollo de stents específicos para cada paciente (7-9). Estos stents han demostrado ser prometedores para proporcionar una resolución a largo plazo de la obstrucción y también ofrecen una mayor comodidad para el paciente (10) y una disminución del tiempo de procedimiento para la colocación (11, 12). Además, al utilizar un material flexible que puede comprimirse y relajarse con la respiración fisiológica normal, los stents de silicona específicos del paciente pueden proporcionar menos complicaciones que las opciones rígidas utilizadas habitualmente. La principal desventaja del uso de stents específicos para cada paciente es el tiempo de producción del stent en comparación con los stents disponibles en el mercado. Con el fin de minimizar el tiempo de producción, se requeriría equipo de producción interno.
Con la disminución del costo y la creciente disponibilidad de impresoras 3D, la impresión 3D se utiliza cada vez más en medicina veterinaria. La cirugía ortopédica de pequeños animales también está utilizando esta tecnología para imprimir modelos 3D anatómicamente precisos basados en imágenes de tomografía computarizada (TC) que se pueden utilizar con fines de planificación quirúrgica (13, 14). La impresión 3D también se utiliza de forma rutinaria para la planificación quirúrgica en el campo de la odontología veterinaria y la cirugía oromaxilofacial (15-17). Sin embargo, la impresión 3D con fines de colocación de stents no se ha descrito en medicina veterinaria. Dadas las complicaciones frecuentes y graves encontradas con las opciones terapéuticas actuales para el NPS y el INP, es necesario investigar alternativas a las opciones de stent actualmente disponibles.
Los objetivos de este estudio fueron describir el desarrollo de stents nasofaríngeos específicos para cada paciente utilizando un molde impreso en 3D, comparar las propiedades mecánicas de este nuevo stent 3D (3DNS) con los stents metálicos autoexpandibles disponibles actualmente, definir la técnica para la colocación de 3DNS en cadáveres caninos y evaluar el ajuste de 3DNS en la nasofaringe.
Materiales y métodos
Animales
Los cadáveres caninos se compraron a un proveedor comercial 1 o se adquirieron como parte de un programa de uso sin restricciones en la institución de los autores. Las muestras cadavéricas se mantuvieron congeladas antes de la evaluación y se descongelaron durante 48-72 h a 4 °C antes de la evaluación por TC. Se eligieron cadáveres de perros de diferentes tamaños (5,7-37,5 kg) para evaluar el desarrollo y la colocación del stent en una variedad de tamaños nasofaríngeos. Tres de los perros eran mesocefálicos, dos dolicocéfalos y uno braquicéfalo.
Producción y desarrollo de stents
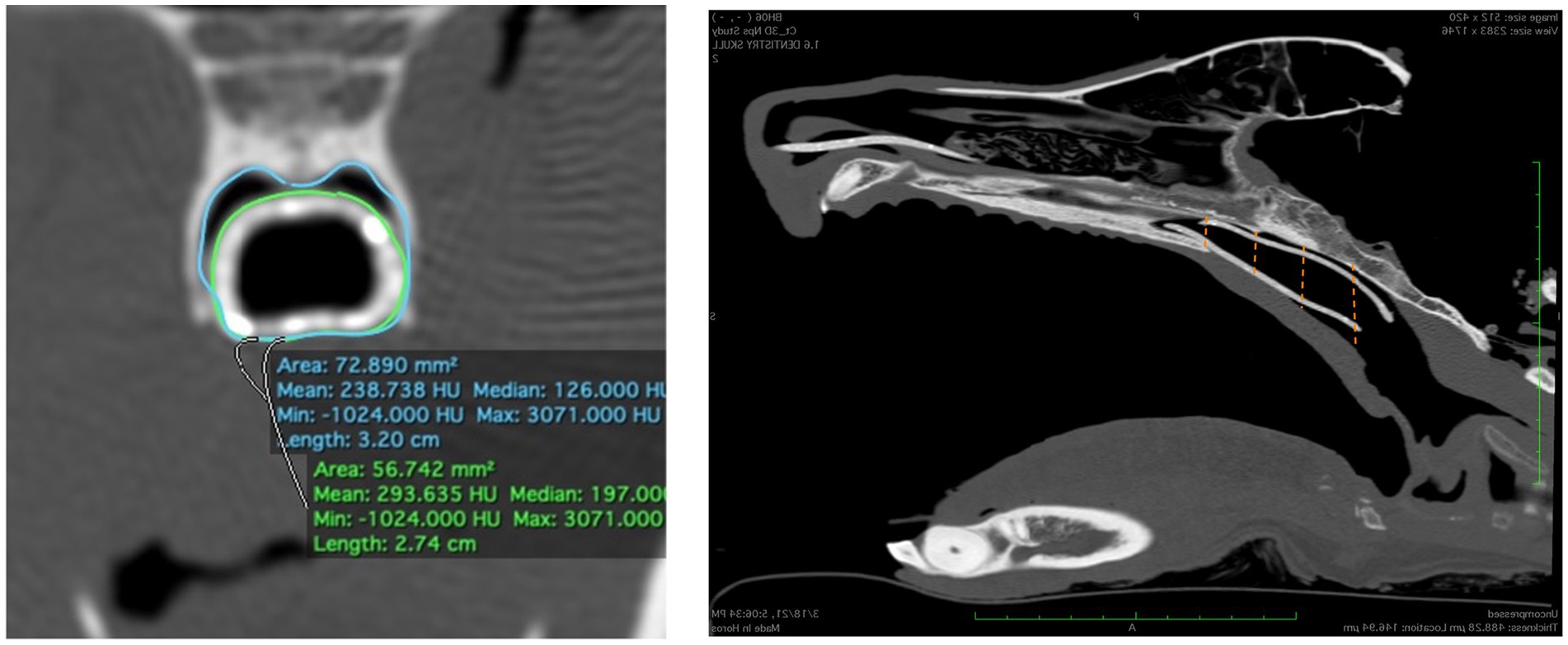
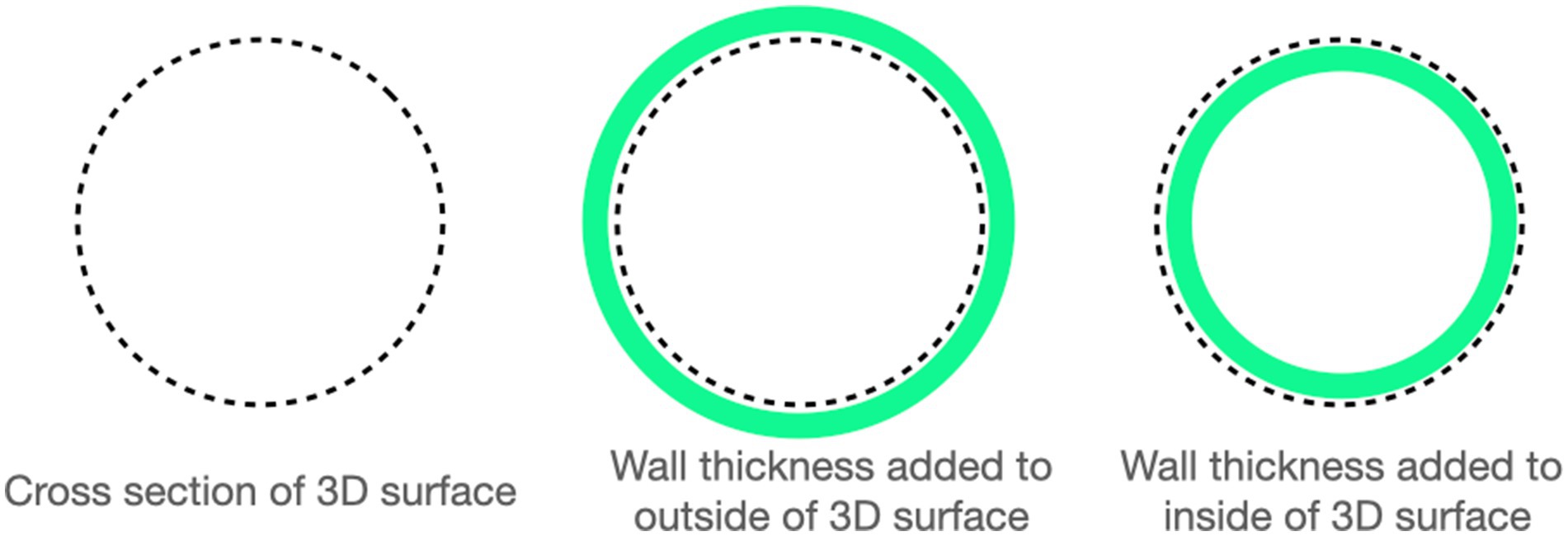
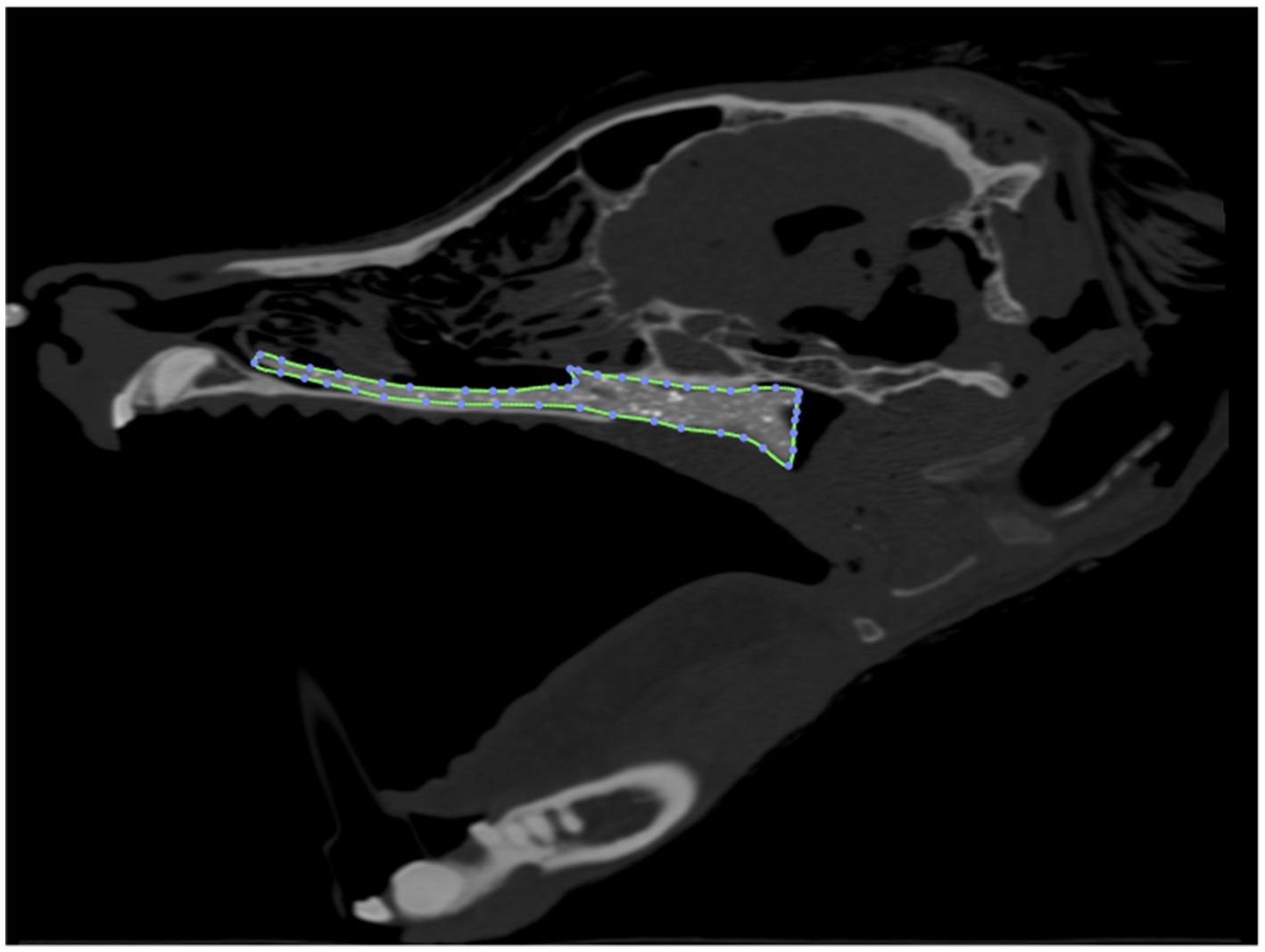
Las imágenes tomográficas computarizadas de cada cabeza de cadáver se adquirieron con posicionamiento de boca abierta utilizando un escáner de TC helicoidal de 16 cortes (Lightspeed, escáner helicoidal de 16, General Electric Co., Milwaukee, WI, EE. UU.) con un grosor de corte de 0,625 mm. Las imágenes DICOM se importaron a InVesalius (Centro de Tecnología de la Información Centro Renato Archer, Campinos, São Paulo, Brasil) para su segmentación. Se utilizaron valores entre aproximadamente 226-3.071 para segmentar el hueso y 25-139 para el tejido blando del aire y para convertir las imágenes DICOM en un único archivo de lenguaje de teselación estándar (.stl). A continuación, este archivo se importó a Autodesk Meshmixer para generar una superficie de malla 3D que delineaba la nasofaringe desde el nivel del hueso vómer hasta el 75% de la longitud del paladar blando en su dirección caudal (Figura 1). La superficie 3D no tiene espesor, por lo tanto, para generar el stent, el grosor de la pared se agregó inicialmente al exterior de la superficie 3D para los primeros tres stents (por ejemplo, la superficie 3D forma la superficie interna del stent). Después de observar problemas con el plegado de los stents después de la colocación (Figura 2), se cambió el protocolo para agregar el grosor de la pared al interior de la superficie 3D (por ejemplo, la superficie 3D forma la superficie exterior del stent; Figura 3). El espesor de la pared del stent fue de 1,75 mm para los especímenes de cadáver 1, 2, 4 y 5. El espesor de la pared se redujo a 1,25 mm para los perros 3 y 6 (razas pequeñas) para mantener las dimensiones lumínicas adecuadas.

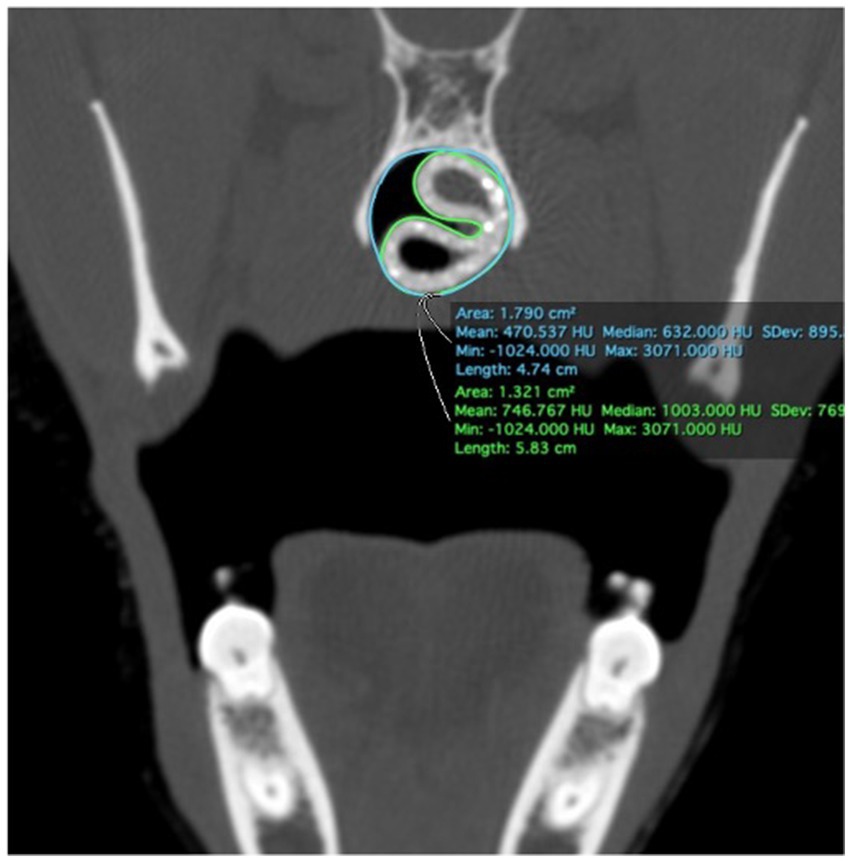
A continuación, se imprimió en 3D un molde de 3 piezas con resina UMA90 en una impresora Carbon M2 configurada en resolución estándar. Las 3 piezas del molde estaban compuestas por las 2 mitades externas y una tercera pieza suspendida en el centro del molde para formar la luz del stent (Figura 4). Partes iguales de la silicona polimerizable de dos componentes (Smooth-On Rebound 40) se combinaron y mezclaron minuciosamente a mano de acuerdo con las instrucciones del fabricante. Esta mezcla se inyectó utilizando un inyector de potencia (Albion Dispensing Solutions) en el molde, se mantuvo al vacío a -12 psi durante 5-7 min para eliminar las burbujas de aire y se dejó curar durante la noche a presión ambiente.

Se crearon varios prototipos de stents a partir de silicona con diferentes durezas shore y espesores de pared (Figura 5). La dureza shore es una escala utilizada para medir la dureza de los cauchos flexibles que oscila en una escala de cero a cien con valores numéricos crecientes que corresponden a un aumento de la dureza. Se consideró subjetivamente que Shore A 10 era demasiado blando para resistir la reestenosis, y que Shore A 60 era demasiado firme para permitir la colocación y extracción del stent, así como la comodidad del paciente. Por lo tanto, se utilizó Shore A 40 para producir el 3DNS. Se encontró que el primer stent (3DNS-1) se doblaba hacia adentro a nivel del vómer en la colocación inicial. Se retiró el 3DNS-1 y se retiró una pieza en forma de cuña de la cara dorso-rostral del stent para acomodar el vómer y aliviar así la compresión (Figura 6).


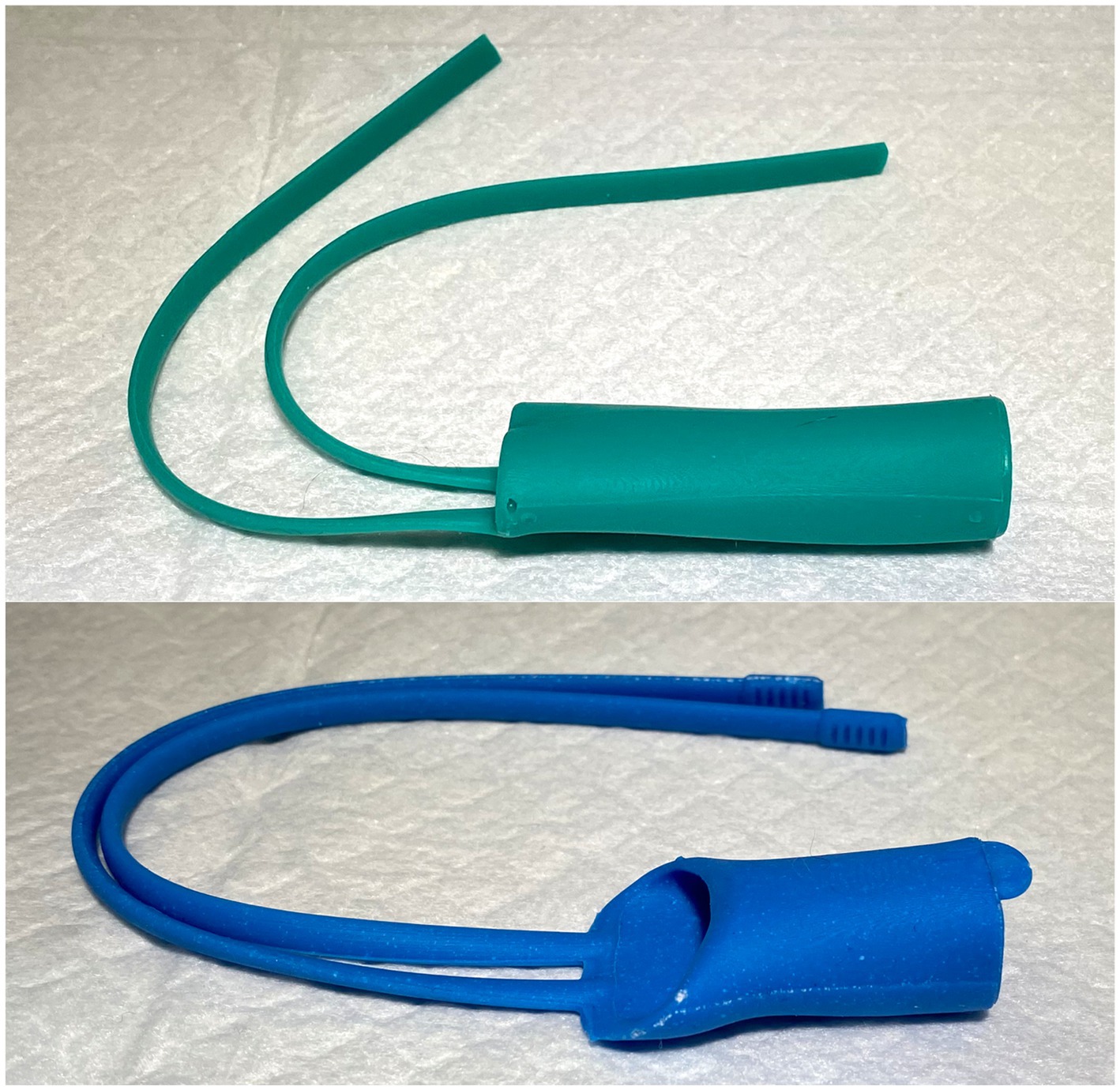
3DNS-2 incorporó varios cambios con respecto a la experiencia con 3DNS-1 (Figura 7). El primero consistió en impregnar la silicona con polvo de sulfato de bario para mejorar la visualización del arco en C. En concreto, se añadieron 5 g de polvo de sulfato de bario (98% de pureza) a 100 g de silicona y se mezclaron bien antes de la inyección en el molde. En segundo lugar, se colocaron correas rostrales para ayudar en la colocación y seguridad del 3DNS. Se agrandaron las puntas de las correas rostrales y se añadieron ranuras para mejorar la tracción durante la colocación. En tercer lugar, se añadió una lengüeta de agarre caudal para facilitar la retirada del stent. El cambio final fue la creación de un ángulo con el aspecto rostral del 3DNS para que coincida con el vómer. Este cambio permitió que los stents se asentaran rostralmente contra el vómer, pero no se colapsaran. Los números 3DNS-3 a 6 se produjeron de manera similar.
Colocación del stent
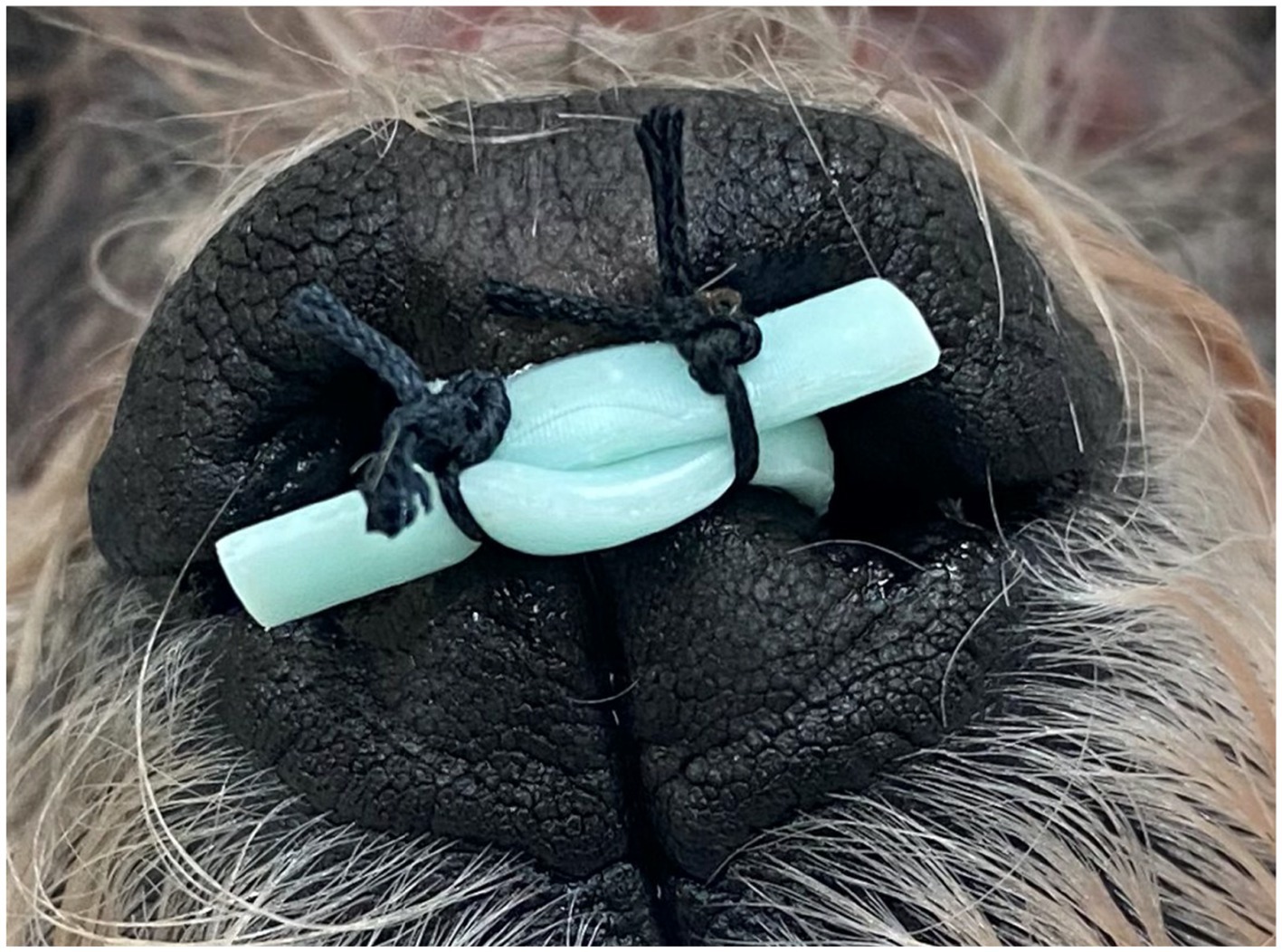
El cadáver se colocó en decúbito lateral derecho con una mordaza bucal única en los dientes caninos. Se pasó un videoendoscopioflexible 2 a través de la cavidad oral y se retroflexionó hasta la nasofaringe. Una guía hidrofílica de 0,035 pulgadas de diámetro por 150 cm de longitud, con punta angular 3, se avanzó anterógrado a través de la naris izquierda y el meato nasal ventral bajo guía fluoroscópica y endoscópica hasta su visualización en la cavidad oral. La guía se agarró con un gancho de esterilización y se sacó por la boca. Se pasó una vaina de 8 Fr y un dilatador4 a través de la guía hasta la cavidad nasal. A continuación, se retiraron la guía y el dilatador, dejando la vaina en su posición. Este procedimiento se repitió a través de la nariz derecha. Las pinzas de biopsia endoscópica flexible 5 se pasaron bilateralmente a través de las vainas de acceso para entrar en la nasofaringe y la cavidad oral. Una vez colocadas, se utilizaron ambas pinzas para agarrar las correas en la cara rostral del stent que se colocó en la cavidad oral. A continuación, las pinzas, las vainas y las correas se retrajeron bajo guía fluoroscópica, y el stent se guió dorsal y rostralmente hasta la nasofaringe (Figura 8). La posición final se determinó mediante una combinación de nasofaringoscopia y fluoroscopia para asegurar que el stent estuviera firmemente asentado en la nasofaringe y no se extendiera más allá de la región deseada del paladar blando. A continuación, las correas se cruzaron por delante del surco nasal para asegurar el stent en su lugar y se utilizó la sutura de seda 0 6 para rodear ambas correas en dos ubicaciones; se recortaron los extremos de las correas (Figura 9).
Evaluación del ajuste del stent
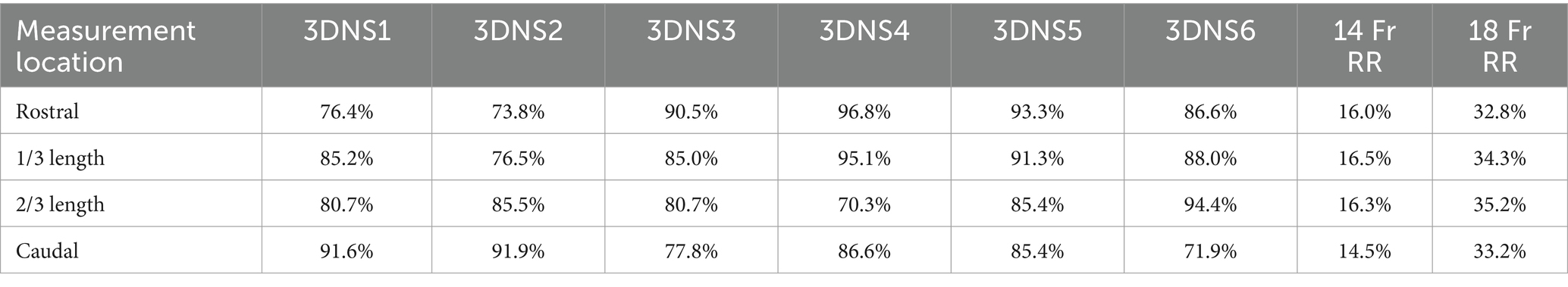
Inmediatamente después de la colocación del stent, se repitió una tomografía computarizada con boca abierta para cada cadáver. Como medida objetiva del ajuste del 3DNS, se calculó el porcentaje de la nasofaringe ocupada por el stent a partir de imágenes transversales de la TC. Las imágenes transversales se adquirieron en 4 puntos a lo largo de la longitud del stent: las porciones rostral y caudal de toda la circunferencia del stent, y 1/3 y 2/3 de la distancia entre estos dos puntos. Las áreas de la sección transversal de la nasofaringe y el stent se midieron con un programa de software disponible comercialmente (Osirix) utilizando la función de polígono abierto en el corte equivalente en las 4 ubicaciones de cada cadáver. Se calculó el área porcentual ocupada por el stent para cada stent (Figura 10). También se utilizaron dos catéteres de caucho rojo de 14 Fr y 18 Fr con el cadáver de 3DNS-1 para estimar el ajuste del stent, ya que los catéteres de caucho rojo se utilizan en la institución de los autores como stents removibles para ciertos casos.

Extracción de stents
La extracción se inició cortando la sutura de seda que asegura las correas rostrales del stent. El videoendoscopio flexible se retroflexionó en la nasofaringe con pinzas de biopsia flexibles precolocadas a través del canal de trabajo del endoscopio. Las pinzas de biopsia se extendieron para agarrar el extremo caudal del stent, y se aplicó una combinación de tracción caudal y rotacional suave para desalojar y posteriormente retirar el stent a través de la cavidad oral.
Ensayos mecánicos
Las pruebas mecánicas se realizaron en el Laboratorio de Investigación Ortopédica Veterinaria JD Wheat de la Facultad de Medicina Veterinaria de UC Davis. Debido a la forma asimétrica de los stents específicos del paciente, se fabricaron cilindros para pruebas mecánicas utilizando una técnica, grosor de pared (1,25 o 1,75 mm) y silicona (Shore A 40) idénticos a los stents específicos del paciente. Estos cilindros tenían 40 mm de largo, con diámetros interiores de 8 mm (1,25 mm de espesor de pared), 14 mm (1,75 mm de espesor de pared) y 20 mm (1,75 mm de espesor de pared). Estos diámetros se eligieron en función del diámetro medio aproximado de la nasofaringe de los 3 primeros especímenes cadavéricos. A modo de comparación, también se probaron 2 stents disponibles en el mercado; un stent de nitinol tejido de 12 mm × 77 mm7, y un stent de nitinol de 12 mm × 60 mm cortado con láser. 8 Un tubo torácico de polivinilo de 24 Fr 9 (ID 5,72 mm) y un tubo de caucho polivinílico rojo de 18 Fr 10 (ID 3,88 mm) se sometieron a las mismas pruebas mecánicas. Los stents se probaron en un sistema de ensayos mecánicos electromecánicos (Instron modelo 5.965) con una célula de carga de 1 kN y placas de compresión de 4 cm de diámetro (Figura 11). Cada stent se comprimió al 50% de su diámetro interno inicial a una velocidad de 12,5 mm/min. Esto se realizó de acuerdo con las normas definidas por ASTM International (ASTM 2412). A lo largo de la compresión, la carga y el desplazamiento se registraron a 0,05 mm/s. Cada stent se descargó a la misma velocidad que la posición inicial de la platina para registrar la deformación residual. Posteriormente, se produjeron curvas de carga-deformación y se recopilaron parámetros específicos con software personalizado (Matlab 2019, Mathworks). Los puntos se capturaron con una deflexión de 5 y 50% de diámetro interior. En cada punto de captura de datos, se registraron el desplazamiento y la fuerza y se calculó la energía como la integral bajo la curva hasta ese punto. Con una deflexión del diámetro interior del 5%, la rigidez se calculó como el ajuste lineal de mínimos cuadrados a través de todos los puntos de datos hasta el punto de deflexión del 5%. La deformación residual se calculó como la diferencia en el desplazamiento a la postcompresión a carga cero en relación con la precarga.

Resultados
Producción, desarrollo y colocación de stents
Utilizando tomografías computarizadas individuales, se desarrollaron 3DNS para 6 cadáveres. Cada prototipo fue modificado para mejorar el ajuste y la funcionalidad del stent y para cumplir con el primer objetivo de este estudio. Estas modificaciones se discutieron anteriormente, pero incluyen la adición de bario impregnado en la silicona para mejorar la visualización, la adición de correas rostrales para ayudar a asegurar el stent en su lugar, modificaciones adicionales a las correas rostrales para ensanchar y ranurar las puntas, la adición de una lengüeta caudal para ayudar en la extracción del stent, y por último, un aspecto rostral inclinado del stent para evitar la compresión por parte del vómer. Todos los stents se colocaron y retiraron con éxito sin complicaciones.
Ajuste de stent
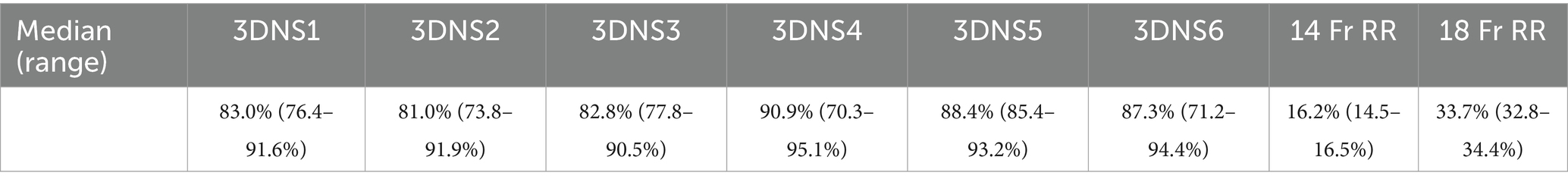
El 3DNS-1 ocupó entre el 76,4 y el 91,6% del área de la sección transversal de la nasofaringe en los 4 sitios de medición a lo largo de la longitud del stent. Los modelos 3DNS-2 a 6 mostraron resultados similares, oscilando entre el 70,3 y el 95,0% de la nasofaringe ocupada por el stent. Los catéteres de caucho rojo de 14 Fr ocuparon el 14,5-16,5% y los de 18 Fr ocuparon el 32,8-35,2% del área de la sección transversal de la nasofaringe en los mismos 4 sitios de medición a lo largo de la longitud del stent. En las tablas 1 y 2 se resumen los resultados de cada uno de los stents.
Pruebas de stent mecánico
En general, el catéter de caucho rojo y el tubo torácico exhibieron la mayor fuerza requerida para la compresión, con el tubo torácico de 24 Fr que requirió 13,77 N para una compresión del 5% y el catéter de goma roja de 18 Fr que requirió 7,11 N para una compresión del 5%. El stent de nitinol tejido requirió 0,61 N para una compresión del 5% del diámetro interno en comparación con los 0,15 N requeridos por el stent de nitinol cortado con láser.
Los 3DNS mostraron un rango de rigidez, de 0,17 a 0,66 N/mm para una compresión del 5% que fue inversamente proporcional a su diámetro interior (Figura 12).
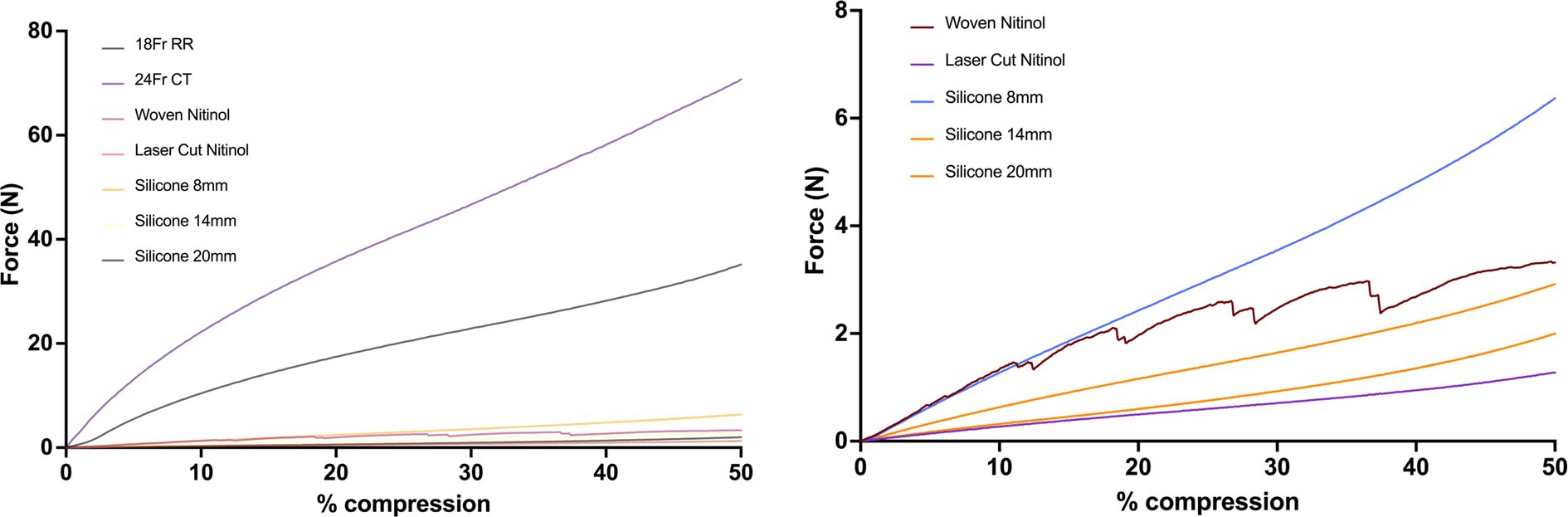
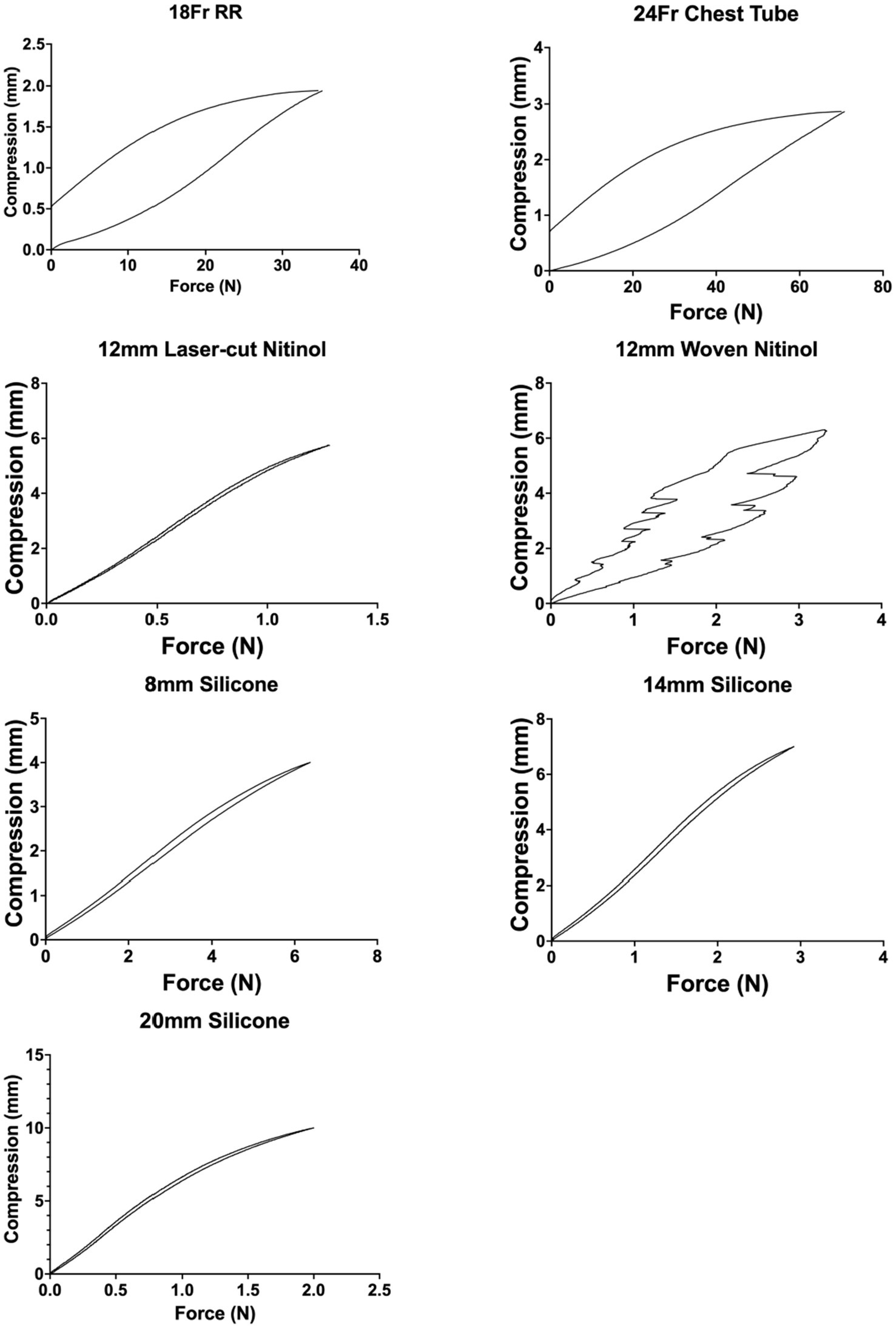
La deformación postcarga fue mayor para el tubo torácico de 24 Fr y el catéter de caucho rojo de 18 Fr, con 0,73 mm y 0,47 mm de deformación documentada, respectivamente. El stent de nitinol tejido y el stent de nitinol cortado con láser mostraron 0,14 mm y 0,01 mm de deformación, respectivamente. Los stents de silicona de 8 mm, 14 mm y 20 mm presentaron 0,02, 0,06 y 0,08 mm de deformación, respectivamente (Figura 13).
Discusión
Este estudio describe el desarrollo y la colocación exitosos de stents nasofaríngeos específicos para cada paciente utilizando moldes impresos en 3D en una variedad de tamaños de perros y conformaciones de cráneo. Las modificaciones del stent a lo largo del proceso condujeron a mejoras en la facilidad subjetiva de colocación y un mejor ajuste en la nasofaringe. El procedimiento en sí fue relativamente fácil de realizar. La capacidad de desplegar y ajustar el ajuste del stent en la nasofaringe permitió una colocación rápida y ajustes fáciles si el ajuste del stent no era ideal en la primera colocación. La retirada del stent también fue fácil, rápida y mínimamente invasiva, independientemente de que el stent se ajustara bien o mal. Además, a medida que avanza la tecnología de impresión 3D, es probable que sea posible imprimir directamente stents flexibles y biocompatibles específicos para cada paciente sin necesidad de un molde, eliminando un paso del proceso de producción de stents descrito en este estudio.
No hay ensayos clínicos y solo hay unos pocos informes de casos de stents específicos de pacientes creados con impresión 3D en la literatura humana. La mayoría de estos estudios se centran en la colocación de stents en las vías respiratorias inferiores, sin embargo, los beneficios de los stents específicos del paciente exhibidos en esos estudios brindan apoyo para investigar esta técnica en las vías respiratorias superiores de pacientes veterinarios (7-12). Estos beneficios reportados incluyen una mayor comodidad, una menor necesidad de procedimientos repetidos y una mejor funcionalidad para restaurar la permeabilidad de una vía aérea estenótica o malacica.
Durante el proceso de desarrollo se detectó un problema en el tamaño de los stents. En un esfuerzo por crear una fuerza hacia afuera para mantener el stent en su posición dentro de la nasofaringe, como se hace para los stents tejidos y cortados con láser, el grosor de la pared de los stents iniciales se agregó al exterior de la superficie nasofaríngea delineada. Debido al ajuste preciso de estos stents específicos para el paciente, esto agregó suficiente material para causar el pliegue interno del stent en el momento de la colocación debido al sobredimensionamiento. En el caso de los 2 últimos stents, este grosor se añadió al aspecto interno, lo que dio lugar a la aposición de la mucosa sin compresión.
Las pruebas mecánicas de los stents de silicona mostraron una rigidez y una fuerza requeridas para la compresión comparables a las de los stents de nitinol comúnmente utilizados. Si bien se desconoce la fuerza o rigidez ideal necesaria para prevenir la reestenosis de la nasofaringe, tener resultados comparables a los stents de nitinol sugiere que los stents específicos del paciente en este estudio probablemente tendrían la rigidez necesaria para prevenir la reestenosis. Los stents de silicona personalizados también tuvieron menos deformación post-carga que los catéteres de caucho rojo que se utilizan actualmente en la institución de los autores como stents. Se esperaría que los stents con menos deformación posterior a la carga mantuvieran su forma original en un paciente vivo donde se aplican con frecuencia fuerzas de compresión al stent durante la respiración y la deglución. La fractura del stent se ha descrito tanto en stents de nitinol como en stents de silicona (18, 19), pero se necesitan más estudios para comparar la tasa de fractura entre los dos tipos de stent.
En última instancia, se necesitará un ensayo clínico para evaluar el éxito y las posibles complicaciones de la colocación de 3DNS en pacientes con estenosis nasofaríngea.
Nuestro estudio tuvo una serie de limitaciones, caracterizadas principalmente por su naturaleza de prueba de concepto y el uso de cadáveres con anatomía nasofaríngea normal. Además, no es posible evaluar las complicaciones o el éxito del mantenimiento de la permeabilidad de estos stents. Sospechamos que estos stents tendrán un éxito similar en términos de prevención de la reestenosis a los stents comerciales, dadas sus pruebas mecánicas similares. También sospechamos que proporcionarán un mejor resultado estético y una mayor comodidad para el paciente, dada la falta de sutura mucosa necesaria para la retención de los stents en la región nasofaríngea, pero se requerirán estudios futuros para evaluar esto. Una limitación adicional viene a la hora de interpretar nuestras pruebas de stents mecánicos, ya que las pruebas de compresión requieren objetos cilíndricos y los stents específicos del paciente no son perfectamente cilíndricos.
Una desventaja de estos stents propuestos es la necesidad de múltiples eventos anestésicos. Se realizaría una tomografía computarizada inicial para obtener las dimensiones de la nasofaringe, un segundo procedimiento para la dilatación de la estenosis y la colocación del stent una vez producido, y un tercero para la extracción del stent. De manera similar, los stents de nitinol también requieren múltiples eventos anestésicos para su medición, colocación y posiblemente un tercer evento para su extracción (20). Por el contrario, la colocación de catéteres modificados como stents temporales es la más eficiente, ya que la tomografía computarizada, la dilatación y colocación de los stents se realizan bajo el mismo evento anestésico y la extracción no requiere anestesia (3).
En general, este estudio describió el desarrollo, la modificación y la colocación de stents nasofaríngeos específicos del paciente utilizando moldes impresos en 3D. Estos stents tienen propiedades mecánicas comparables a las de los stents comerciales y se desarrollan con un método específico para cada paciente.
Declaración de disponibilidad de datos
Los datos brutos que respaldan las conclusiones de este artículo serán puestos a disposición por los autores, sin reservas indebidas.
Declaración ética
No se requirió aprobación ética para el estudio con animales de acuerdo con la legislación local y los requisitos institucionales debido a la naturaleza del estudio como un estudio cadavérico.
Contribuciones de los autores
CS: Curación de datos, Análisis formal, Investigación, Metodología, Redacción: borrador original, Redacción: revisión y edición. BH: Conceptualización, Análisis formal, Obtención de fondos, Investigación, Metodología, Supervisión, Redacción, revisión y edición. SL: Conceptualización, Metodología, Recursos, Redacción – revisión y edición. LJ: Redacción – revisión y edición. WC: Conceptualización, Recursos, Escritura – revisión y edición.
Financiación
El/los autor/es declara(n) haber recibido apoyo financiero para la investigación, autoría y/o publicación de este artículo. Los autores desean agradecer al Centro para la Salud de los Animales de Compañía de UC Davis por financiar este estudio (CCAH 2019-2-f).
Reconocimientos
Los autores desean agradecer a Tanya García-Nolen, BS, MS, por realizar las pruebas biomecánicas. Los autores desean agradecer a la Dra. Rebecca Woodworth por proporcionar las especificaciones de la TC y al servicio de Radiología de Pequeños Animales de UC Davis por su asistencia en la captura de imágenes.
Conflicto de intereses
Los autores declaran que la investigación se llevó a cabo en ausencia de relaciones comerciales o financieras que pudieran interpretarse como un posible conflicto de intereses.
Nota del editor
Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, ni las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo, o afirmación que pueda hacer su fabricante, no está garantizado ni respaldado por el editor.
Notas
1. ^Skulls Unlimited, Oklahoma City, OK, EE. UU.
2. ^Olympus BF-P180, San José, CA, EE. UU.
3. ^Alambre de comadreja médica Infiniti de 0,035 pulgadas × 150 cm; Infiniti Medical, 334 Redwood City, CA, EE. UU.
4. ^Introductor de vaina percutánea de flecha 8 Fr; Teleflex, Wayne, Pensilvania, Estados Unidos.
5. ^ Pinzas de copa desechables de Endoscopy Support Services Inc; Servicios de apoyo en endoscopia, Brewster, NY, EE. UU.
6. ^Sutura de seda de mano permanente Ethicon; Johnson and Johnson, Nuevo Brunswick, Nueva Jersey, Estados Unidos.
7. ^Tráquea de stent veterinario médico de Infiniti; Infiniti Medical, Redwood City, CA, EE. UU.
8. ^Infiniti Medical Vet Stent-Uretra; Infiniti Medical, Redwood City, CA, EE. UU.
9. ^Tubo torácico MILA 24 Fr; Patterson Veterinary, Loveland, CO, EE. UU.
10. ^Sonda de alimentación y catéter uretral Patterson Sovereign; Patterson Veterinary, Loveland CO, EE. UU.
Referencias
1. Berent, A. Diagnóstico y tratamiento de la estenosis nasofaríngea. Vet Clin N Am Pequeño Anim Pract. (2016) 46:677–89. doi: 10.1016/j.cvsm.2016.01.005
2. Budrick, S, Berent, A, Weisse, C, Palma, D, Asprea, L, Lamb, K, et al. Tratamiento intervencionista de la estenosis nasofaríngea benigna y la nasofaringe imperforada en perros y gatos: 46 casos (2005-2013). JAVMA. (2018) 253:1300–8. doi: 10.2460/javma.253.10.1300
3. De Lorenzi, D, Bertoncello, D, Comastri, S, y Bottero, E. Tratamiento de la estenosis nasofaríngea adquirida mediante un stent de silicona removible. J Feline Med Surg. (2015) 17:117–24. doi: 10.1177/1098612X14533692
Resumen de PubMed | Texto completo de Crossref | Google Académico
4. Berent, A, Weisse, C, Todd, K, Rondeau, M y Reiter, A. Uso de un stent metálico expandible con balón para el tratamiento de la estenosis nasofaríngea en perros y gatos: seis casos (2005-2007). JAVMA. (2008) 233:1432–40. doi: 10.2460/javma.233.9.1432
Resumen de PubMed | Texto completo de Crossref | Google Académico
5. Bird, L, Nelissen, P, White, R, y Tappin, S. Tratamiento de la estenosis nasofaríngea canina mediante stents metálicos expandibles con balón: seguimiento a largo plazo de cuatro casos. JSAP. (2015) 57:265–70. doi: 10.1111/jsap.12430
6. Cook, A, Mankin, K, Saunders, A, Waugh, C, Cuddy, L, y Ellison, G. Erosión palatina y fistulación oronasal después de la colocación de un stent nasofaríngeo cubierto en dos perros. Ir Vet J. (2013) 66:8. doi: 10.1186/2046-0481-66-8
Resumen de PubMed | Texto completo de Crossref | Google Académico
7. Guibert, N, Mhanna, L, Didier, A, Moreno, B, Leyx, P, Plat, G, et al. Integración de la impresión 3D y la fabricación aditiva en la caja de herramientas del neumólogo intervencionista. Respir Med. (2018) 134:139–42. doi: 10.1016/j.rmed.2017.11.019
8. Tam, M, Laycock, S, Jayne, D, Babar, J y Noble, B. Impresiones 3D del árbol traqueobronquial generadas a partir de imágenes de TC como ayuda para el tratamiento en un caso de condromalacia traqueobronquial causada por policondritis recurrente. J Radiol Caso Rep. (2013) 7:34–43. doi: 10.3941/jrcr.v7i8.1390
9. Ntiamoah, P, Gildea, TR y Baiera, A. Determinación del ajuste del stent de la vía aérea específico del paciente mediante nuevas técnicas de medición de reconstrucción 3D: un seguimiento de 4 años de un paciente. Ther adv respir dis. (Enero-Diciembre de 2023) 17:17534666221137999. doi: 10.1177/17534666221137999
Resumen de PubMed | Texto completo de Crossref | Google Académico
10. Schweiger, T, Gildea, T, Prosch, H, Lang, G, Klepetko, W, Hoetzenecker, K, et al. Stents en Y de silicona diseñados en 3 dimensiones específicos para cada paciente en la traqueobroncomalacia: experiencia clínica con un nuevo tipo de stent de vía aérea. J Cirugía Cardiovasca Torácica. (2018) 156:2019–21. doi: 10.1016/j.jtcvs.2018.06.049
Resumen de PubMed | Texto completo de Crossref | Google Académico
11. Ojima, T, y Kitamura, N. Tratamiento de la estenosis de la vía aérea con un stent bronquial personalizado utilizando una impresora tridimensional y filamentos flexibles. Respirol Case Rep. (2019) 7:E00491. DOI: 10.1002/RCR2.491
Resumen de PubMed | Texto completo de Crossref | Google Académico
12. Gildea, T, Young, B y Machuzak, M. Aplicación de la impresión 3D para stents de silicona específicos del paciente: seguimiento de 1 año en dos pacientes. Respiración. (2018) 96:488–94. doi: 10.1159/000489669
Resumen de PubMed | Texto completo de Crossref | Google Académico
13. Mejía, S, Stewart, N, Miller, A, Savicky, R, Monarski, C, Moore, G, et al. Precisión de las mediciones externas de biomodelos impresos en 3D en 3D del radio canino utilizados en un entorno hospitalario. Can J Vet Res. (2019) 83:181–6.
14. Larguier, L, Hespel, A, Jamet, N, Mercier, E, Jouan, D, Jardel, N, et al. Exactitud y precisión de las mediciones realizadas en pelvis impresas tridimensionales en comparación con las mediciones de tomografía computarizada. J Vet Sci. (2019) 20:E22. doi: 10.4142/jvs.2019.20.e22
Resumen de PubMed | Texto completo de Crossref | Google Académico
15. Thatcher, GP, y Soukup, JW. Planificación quirúrgica virtual e impresión 3D en odontología veterinaria y cirugía oromaxilofacial. Veterinario Clin North Am Small Anim Pract. (2022) 52:221–34. doi: 10.1016/j.cvsm.2021.09.009
Resumen de PubMed | Texto completo de Crossref | Google Académico
16. Klasen, JRS, Thatcher, GP, Bleedorn, JA, y Soukup, JW. Planificación quirúrgica virtual e impresión 3D: metodología y aplicaciones en cirugía oromaxilofacial veterinaria. Frente Vet Sci. (2022) 9:971318. doi: 10.3389/fvets.2022.971318
17. Huang, YH, Lee, B, Chuy, JA y Goldschmidt, impresión SL. 3D para la planificación quirúrgica de cirugías orales y maxilofaciales caninas. Impresión 3D Med. (2022) 8:17. doi: 10.1186/s41205-022-00142-y
Resumen de PubMed | Texto completo de Crossref | Google Académico
18. Nikanorov, A, Smouse, HB, Osman, K, Bialas, M, Shrivastava, S, y Schwartz, LB. Fractura de stents de nitinol autoexpandibles estresados in vitro en condiciones intravasculares simuladas. J Vasc Surg. (2008) 48:435–40. doi: 10.1016/j.jvs.2008.02.029
Resumen de PubMed | Texto completo de Crossref | Google Académico
19. Popilevsky, F, Al-Ajam, MR, Ly, V, Sánchez, LD y Cutaia, M. Fracturas dinámicas de stent Y en traqueobroncomalacia semilunar. J Bronchol Interv Pulmonol. (2012) 19:206–10. doi: 10.1097/LBR.0b013e31825c6f57
Resumen de PubMed | Texto completo de Crossref | Google Académico
Palabras clave: stents impresos en 3D, nasofaringe, estenosis nasofaríngea, pruebas mecánicas, nasofaringe imperforada
Cita: Sutter C, Hardy B, Lucero S, Johnson L y Culp W (2024) Stent nasofaríngeos impresos en 3D específicos del paciente en perros: un estudio piloto cadavérico. Frente. Vet. Sci. 11:1461657. doi: 10.3389/fvets.2024.1461657
Recibido: 08 de julio de 2024; Aceptado: 06 de noviembre de 2024;
Publicado: 20 de noviembre de 2024.
Editado por:
Rocío Fernández-Parra, Universidad Católica de Valencia San Vicente Mártir, España
Revisado por:
Adeline Decambron, Clínica Veterinaria Hopia, Francia
Carolina Serrano Casorran, Universidad de Zaragoza, España
Derechos de autor © 2024 Sutter, Hardy, Lucero, Johnson y Culp. Este es un artículo de acceso abierto distribuido bajo los términos de la Licencia Creative Commons Attribution License (CC BY).
*Correspondencia: Craig Sutter, Craig.m.sutter@gmail.com
†Direcciones actuales: Craig Sutter, Sala de Emergencias y Centro de Especialidades para Mascotas del Noroeste del Pacífico, Vancouver, WA, Estados Unidos; Brian Hardy, Departamento de Ciencias Clínicas, Universidad Estatal de Oregón, Corvallis, Oregón, Estados Unidos
Renuncia: Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente a las de sus organizaciones afiliadas, o las del editor, de los editores y de los revisores. Cualquier producto que puede ser evaluada en este artículo o afirmación que puede ser hecha por su El fabricante no está garantizado ni respaldado por el editor.
Date de alta y recibe nuestro 👉🏼 Diario Digital AXÓN INFORMAVET ONE HEALTH
Date de alta y recibe nuestro 👉🏼 Boletín Digital de Foro Agro Ganadero
Noticias animales de compañía
Noticias animales de producción
Trabajos técnicos animales de producción
Trabajos técnicos animales de compañía