Tratamiento de trematodos hepáticos en bovinos y ovinos

Tratamiento de trematodos hepáticos en bovinos y ovinos
Sarah Hewitt discute el ciclo de vida de esta enfermedad parasitaria, los métodos para detectar infecciones, las opciones de tratamiento y las medidas para su control.
- Este artículo se publicó originalmente en Vet Times 49.17 (29 de abril de 2019).
El trematodo hepático es una infección zoonótica que puede afectar significativamente el rendimiento del ganado vacuno y ovino. Teniendo en cuenta el ciclo de vida del huésped intermedio, el caracol de barro es vital para diseñar e implementar protocolos de control efectivos. Los niveles de infección por Fasciola están fuertemente influenciados por el clima y el medio ambiente, por lo que, para ser más efectivos, los protocolos de control deben ser específicos de la granja, el clima y el medio ambiente, y, por lo tanto, pueden variar de año en año y de granja a granja.
Se puede considerar el uso estratégico de los fluquicidas y las opciones de manejo, y con la creciente preocupación por la resistencia a los fluquicidas, se deben considerar métodos alternativos de control de los trematodos. Además, es necesario tener en cuenta los períodos de espera de los fluquicidas, particularmente en vacas lecheras lactantes.
Se pueden utilizar varios diagnósticos para identificar la infección por trematodos y monitorear el efecto de cualquier plan de control implementado. Estos se pueden llevar a cabo de forma rutinaria, lo que permite un monitoreo continuo de la infección por trematodos en la granja y el ajuste de las medidas de control según sea necesario.
Las infecciones por trematodo hepático (Fasciola hepatica) en bovinos y ovinos pueden tener un efecto importante en la producción, y comprender el ciclo de vida y la distribución del parásito es crucial para diseñar e implementar planes de control efectivos.
El trematodo hepático es un trematodo que parasibiliza a moluscos (como huéspedes intermedios) y vertebrados (como huéspedes definitivos). El ganado vacuno y las ovejas son los principales huéspedes definitivos del trematodo hepático, aunque los ciervos, conejos y humanos también pueden actuar como huéspedes definitivos, mientras que el huésped intermedio es el caracol barro (Galba truncatula). Esto significa que la prevalencia de la infección aumenta cuando el ganado vacuno y el ganado ovino se encuentran con caracoles de barro infectados, es decir, en pastos húmedos, y tiende a variar con los entornos y climas cambiantes.
Como su nombre indica, la trematodo hepático daña el hígado. Esto da lugar a una variedad de signos clínicos, incluyendo tasas de crecimiento y calidad de canal reducidas, pérdida de peso, reducción de la producción y calidad de la leche, reducción de la fertilidad y muerte (Mazeri et al, 2017; Howell et al, 2015; Beesley et al, 2017; Charlier et al, 2014; Sargison y Scott, 2011). Las pérdidas de producción aumentan aún más por las condenas hepáticas en el sacrificio.
La infección por fasciola también puede conducir a la modulación inmune, haciendo que el ganado sea más propenso a otras enfermedades, como la bTB, y afectando el diagnóstico de enfermedades y, posiblemente, la eficacia de la vacuna (Charlier et al, 2014; Flynn et al, 2009).
Las cifras sobre el verdadero costo financiero de la infección por trematodo son difíciles de estimar debido a estos diversos efectos en la producción. Los costos anuales para la industria ganadera del Reino Unido se han estimado entre 40,4 millones de libras esterlinas (Control de Worms Sustainably, 2018) y 23 millones de libras esterlinas (Scott, 2016), mientras que, a nivel de animal individual, las estimaciones son de 25 a 30 libras esterlinas por oveja y 200 libras esterlinas por vaca lechera/carne de res (Skuce y Zadoks, 2017). Además de los costos económicos, es evidente que existe un costo de bienestar para las infecciones por trematodos hepáticos.
Ciclo de vida
El huésped intermedio del caracol de barro es crucial para que el trematodo complete su ciclo de vida, por lo que la presencia de este organismo dicta el tiempo del tratamiento y los protocolos de control.
Un solo trematodo adulto puede desprender hasta 50.000 huevos al día, lo que lleva a una contaminación rápida y pesada de los pastos. Estos huevos eclosionan de manera dependiente de la temperatura para liberar la primera etapa larvaria: los milagros, que infectan al caracol de barro al enterrar a través del pie hasta la cavidad abdominal.
Dentro del caracol de barro, se produce la reproducción asexual, produciendo la segunda etapa larvaria, las cercarias. Como la reproducción es asexual en esta etapa, existe el potencial de una rápida expansión de cualquier población resistente a los medicamentos. Estas cercarias se liberan de los caracoles después de unas seis semanas y forman quistes (metacercariae), que luego son ingeridos por huéspedes definitivos como bovinos, ovejas, humanos y muchos otros vertebrados. Cuando se ingieren, los jóvenes se exquiste la trematodo y migran desde el intestino a través del hígado, causando daño a medida que van a los conductos biliares, donde maduran y ponen huevos. El período total de prepatente es de 10 a 12 semanas (Figura 1).
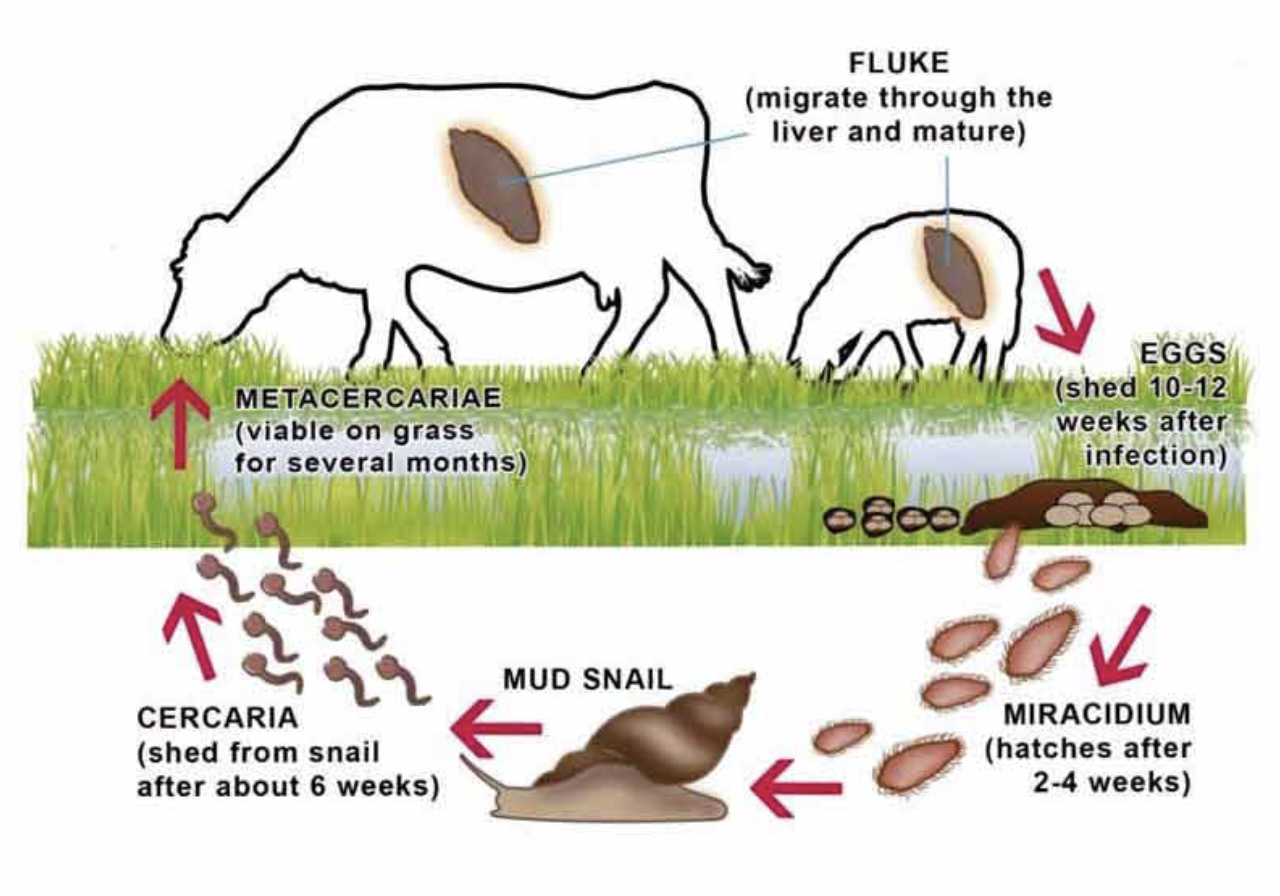
Los caracoles de barro son parte integral de este ciclo de vida, por lo que evitar el contacto con ellos y romper el ciclo es un aspecto importante del control. Los caracoles de barro tienden a encontrarse en terreno húmedo y pantanoso y se pueden encontrar poblaciones particularmente grandes después del clima húmedo (Figura 2). Esto conduce a una variación estacional en las infecciones por trematodos, con caracoles que tienden a infectarse en primavera, pastos contaminados durante el verano, ganado infectado en otoño y signos clínicos que se ven en invierno.

La actividad de fasciola depende mucho del clima, lo que significa que los inviernos suaves/húmedos pueden provocar que los animales se infecten en primavera. Esto influye cuando se producen períodos de alto riesgo y, por lo tanto, cuando se debe tratar a los animales. El Servicio Nacional de Información sobre Enfermedades Animales proporciona pronósticos de trematodos para diferentes regiones del Reino Unido basados en el clima y los patrones de infección anteriores, y se puede utilizar para informar las decisiones de calendario del tratamiento. Sin embargo, la geografía y el manejo individual de la granja también deben tenerse en cuenta al desarrollar protocolos de control, ya que estos pueden variar localmente (McCann et al, 2010; Knubben-Schweizer y Torgerson, 2015).
Diagnóstico
Hay varios métodos de diagnóstico disponibles para la detección de trematodos. Para el monitoreo a largo plazo, se pueden usar informes de matadero de condenas hepáticas, o muestreo regular de leche a granel para anticuerpos contra la gripe en rebaños lecheros. Para grupos individuales o pequeños de animales, se puede realizar un muestreo de sangre o fecal. Las muestras de sangre se pueden utilizar para detectar anticuerpos creados contra un desafío de trematodo, que dura entre dos y cuatro semanas (Salimi-Bejestani et al, 2005). Sin embargo, estos anticuerpos pueden persistir con la detección 18 meses después de la denuncia de la infección (Hutchinson y Macarthur, 2003), lo que significa que no se puede confiar en los resultados para indicar la infección reciente o actual. El análisis de enzimas hepáticas en muestras de sangre también se puede utilizar para identificar el daño hepático o evaluar la función; sin embargo, esto no es específico del trematodo y lo bien que se correlaciona con el pronóstico puede ser difícil de determinar (Skuce y Zadoks, 2013).
Las pruebas fecales suelen detectar huevos de trematodo, por lo que solo detectarán la infección después del período de prepatente (10 a 12 semanas). El recuento de óvulos fecales también puede producir resultados falsos negativos debido a la baja sensibilidad (aunque se ha demostrado que las pruebas repetidas mejoran esto) y el almacenamiento de óvulos dentro de la vesícula biliar con desprendimiento intermitente (Charlier et al, 2014; Sargison y Scott, 2011).
El coproantígeno ELISA es una prueba más reciente que detecta antígenos de trematodo en las heces, por lo que puede detectar la infección antes del final del período de prepatente. Sin embargo, los ensayos de campo a veces han tenido dificultades para replicar las tasas de detección alcanzadas experimentalmente, particularmente en el ganado (Skuce y Zadoks, 2013). En la infección aguda, donde la muerte súbita es un signo común de presentación, una autopsia es a menudo el mejor método de diagnóstico.
Claramente, todos los diagnósticos tienen sus limitaciones, y estas deben tenerse en cuenta al investigar los patrones de infección por trematodos en la granja y utilizar los resultados para informar las decisiones de gestión. La identificación de grupos particulares de animales con infección por trematodos (o la etapa de producción en la que los animales se están infectando) se puede utilizar para ayudar a informar estas decisiones y para identificar áreas de alto riesgo de pastos, épocas del año y grupos de animales (Knubben-Schweizer y Torgerson, 2015). Repetir regularmente los diagnósticos y revisar el control de la corriente, con respecto a los resultados y el clima reciente, puede ayudar a adaptar las estrategias de control a las granjas individuales cada año.
Tratamiento
Las infecciones por trematodo hepático pueden ser crónicas (Figura 3) o agudas (Figura 4), dependiendo de la dosis infecciosa ingerida, y el tipo de infección determina las opciones de tratamiento más adecuadas.
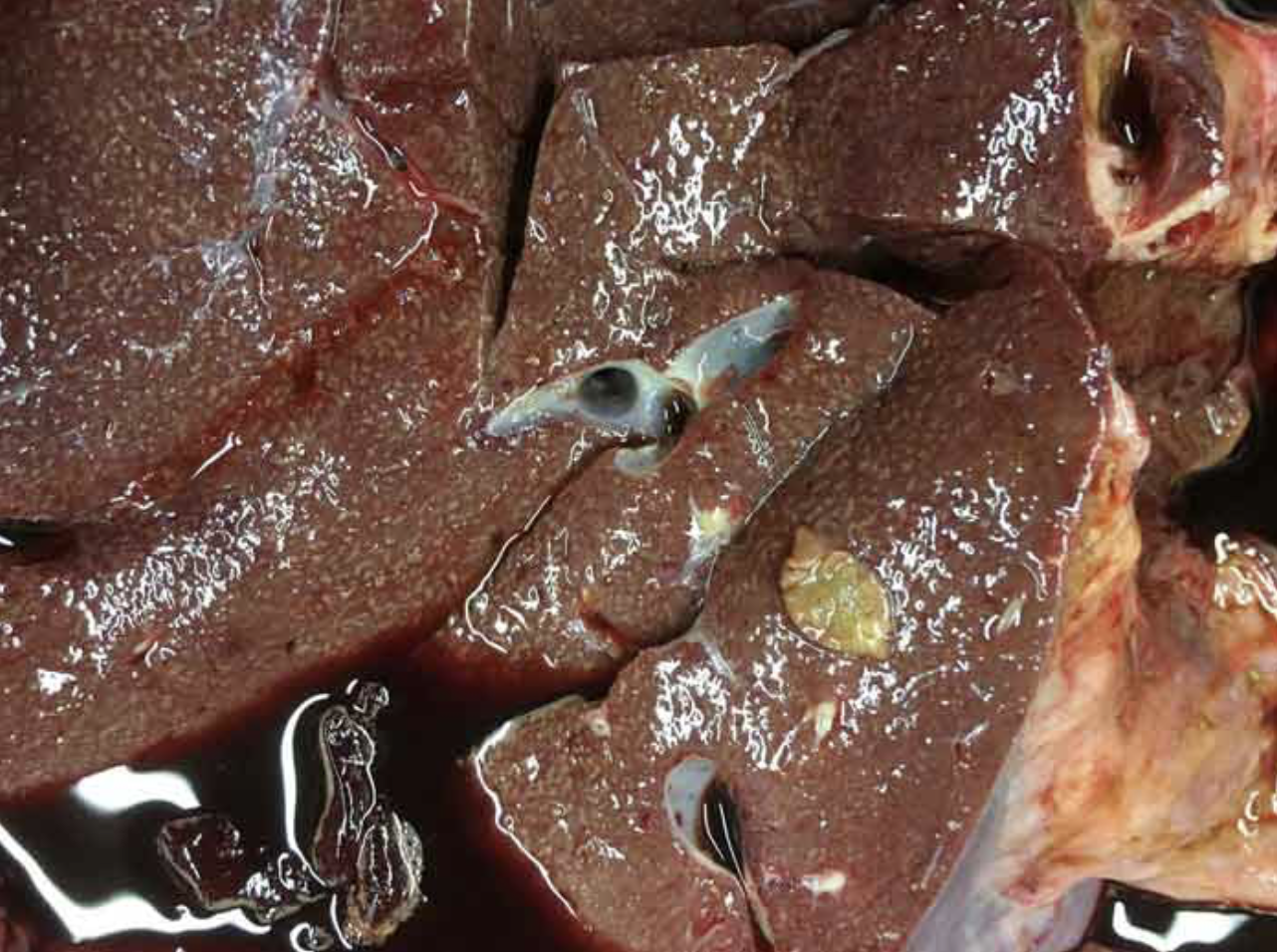
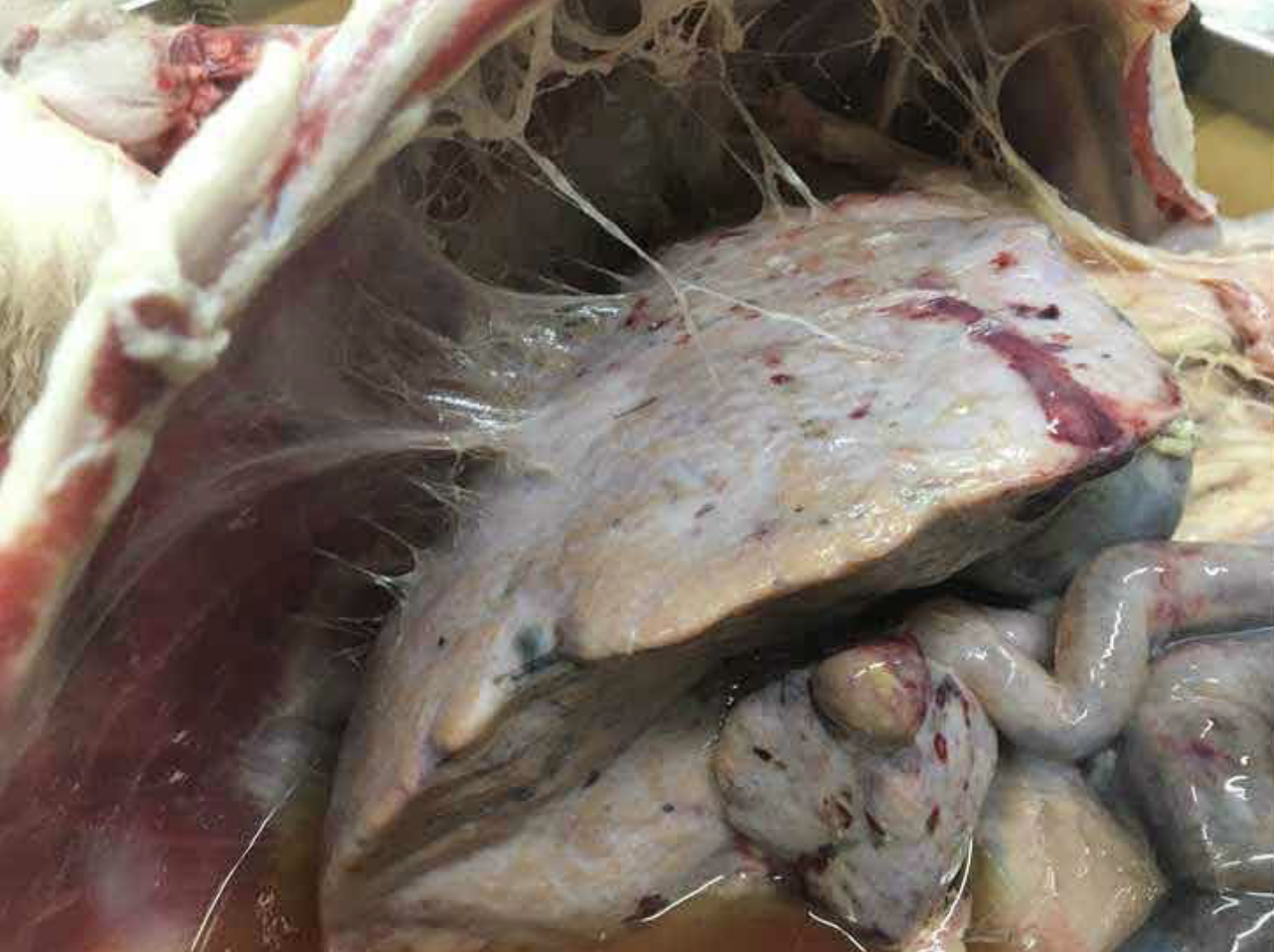
Las ovejas son más propensas a mostrar signos de infección aguda (daño hepático grave, anemia y muerte súbita) después de ingerir grandes cantidades de quistes infecciosos, a menudo en otoño. Las muertes pueden ocurrir antes de que el trematodo inmaduro se haya convertido en adultos ponedores de huevos (es decir, durante el período prepatente), lo que significa que los huevos de trematodo no se pueden detectar en las heces. Las infecciones crónicas por trematodo se observan tanto en ovejas como en bovinos, generalmente en invierno/principios de primavera después de la ingesta prolongada de un bajo número de quistes infecciosos. Los signos de infecciones crónicas por trematodos incluyen pérdida de peso, mandíbula del biberón y mala fertilidad.
Teniendo en cuenta el espectro de actividad del fluquicida, es decir, las etapas del ciclo de vida del trematodo al que se dirige con respecto al tipo de infección presente, es importante al seleccionar los tratamientos. Otros aspectos a considerar incluyen las condiciones climáticas recientes, la época del año, el pastoreo de tierras, las probables presiones de infección y las extracciones de leche/carne. Es poco probable que seguir el mismo protocolo en cada granja, o incluso en la misma granja en los años posteriores, sea la mejor opción. Las estrategias de control deben adaptarse a las granjas individuales y revisarse regularmente. Esto es particularmente pertinente con respecto al uso de triclabendazol, ya que se han reportado casos de resistencia a este fluquicida en ovejas y bovinos (Sargison y Scott, 2011; Skuce y Zadoks, 2013).
El triclabendazol se utiliza a menudo como tratamiento y control de primera línea para el trematodo hepático, ya que mata la más amplia gama de etapas del ciclo de vida del trematodo. Sin embargo, no siempre es necesario, por ejemplo, si el ganado ha sido alojado durante un período y solo es probable que haya trematodos adultos. De hecho, se ha sugerido que el triclabendazol no debe usarse en el ganado en absoluto, y debe reservarse para tratar ovejas donde la infección aguda por trematodos y, por lo tanto, la focalización de las etapas inmaduras del parásito, es más común (Skuce y Zadoks, 2013).
Otras opciones de tratamiento incluyen tratamientos secuenciales con un medicamento que mata solo el trematodo adulto, aunque esto solo será efectivo si los animales no se reinfectan posteriormente. A diferencia de los desparasitantes, los fluquicidas no tienen actividad persistente, por lo que las vacas y ovejas pueden volver a infectarse de pastos infectados si se les devuelven después del tratamiento. Además, a diferencia de los nematodos, el ganado vacuno y el ovino no generan inmunidad efectiva al trematodo, por lo que no se puede presumir que las cepas más antiguas que previamente han estado expuestas al trematodo sean inmunes.
Cuando co-pastorean ganado vacuno y ovino, es importante recordar que el mismo parásito puede infectar a ambas especies, y los protocolos de tratamiento/control deben incluir tanto bovinos como ovinos. Los reservorios de infección de vida silvestre también pueden significar que las poblaciones de trematodos se pueden mantener en ausencia de ganado. El uso de productos combinados, que a menudo combinan fluquicidas con otros desparasimbantes, debe considerarse cuidadosamente para garantizar que se minimicen los riesgos de promover la resistencia a otros productos.
Los períodos de espera deben tenerse en cuenta al seleccionar las opciones de tratamiento, y esto puede ser particularmente problemático al tratar vacas lecheras. Dos ingredientes activos están autorizados para tratar vacas lecheras – albendazol y oxiclozanida – y ambos matan el trematodo adulto (10 semanas después de la infección en adelante), lo que significa que pueden ser necesarios tratamientos repetidos. Esto puede ser difícil de implementar, ya que se requerirán extracciones de leche después de cada tratamiento. Otra alternativa es tratar a las vacas al secarse con un producto apropiado (Tabla 1).
| Ingrediente activo | Ruta de administración | Edad de la dilasión dirigida | ¿Vonado u oveja? | Uso en ganado lechero |
| Triclabendazol | Oral | Dos semanas después (algunos productos a partir de unos pocos días de edad) | Ganado y oveja | Algunos productos se pueden usar durante el período seco (se aplican períodos de espera) |
| Verter | De seis a ocho semanas en adelante | Ganado | Ninguno | |
| Closantel | Inyección SC (en combinación con ivermectina) | De siete a nueve semanas en adelante | Ganado y oveja | Ninguno |
| Verter (en combinación con ivermectina) | Siete semanas después | Ganado | Ninguno | |
| Oral | Cinco semanas en adelante (actividad a partir de tres semanas con algunos productos) | Ovejas | N/D | |
| Nitroxinil | Inyección SC | De siete a ocho semanas en adelante | Ganado y oveja | Ninguno |
| Clorsulón | Inyección SC (en combinación con ivermectina) | Diez semanas después | Ganado | Ninguno |
| Oxiclozanida | Oral | Diez semanas después | Ganado y oveja | Extracción de leche 108 horas |
| Albendazol | Oral | Diez semanas después | Ganado y oveja | Extracción de leche de 60 a 72 horas |
| Adaptado del Control de Gusanos Productos Flukicidas sostenibles para ganado y utilizando información del Compendio NOAH. Correcto a partir de noviembre de 2018. Para obtener la información más reciente, consulte la base de datos de información de productos VMD | ||||
Tabla 1. Fluquicidas para bovinos y ovinos en el Reino Unido
Monitoreo del éxito del tratamiento
Al monitorear el éxito del tratamiento, es importante diferenciar entre resistencia a los medicamentos y fracaso del tratamiento (Skuce y Zadoks, 2013). El fracaso del tratamiento puede deberse a una dosificación incorrecta del ganado o al almacenamiento del producto, en lugar de a poblaciones resistentes a los trematodos. La reinfección inmediata de los animales también puede imitar el aparente fracaso del tratamiento.
También vale la pena considerar que los productos con licencia para atacar diferentes etapas del trematodo a menudo no informan del 100% de eficacia en estas etapas (particularmente las etapas inmaduras). La resistencia a los medicamentos se puede detectar mediante pruebas de reducción del recuento de huevos fecales (FECRT). Sin embargo, el riesgo de resultados falsos negativos con las FECRT a veces puede indicar un éxito aparente del tratamiento en ausencia de una eficacia completa, por lo que los resultados deben interpretarse a la luz de esto. Se ha demostrado que las FECRT se correlacionan mal con los niveles de infección por trematodo identificados en el examen post mortem, aunque el coproantígeno ELISA se ha sugerido como una prueba alternativa para el éxito del tratamiento (Skuce y Zadoks, 2013; Beesley et al, 2017). Las pruebas moleculares en desarrollo pueden ofrecer una identificación más confiable de la resistencia a los medicamentos en las poblaciones de trematodos en el futuro (Beesley et al, 2017; Skuce y Zadoks, 2013).
Otras medidas de control
Romper el ciclo de vida del trematodo, es decir, prevenir el contacto entre el ganado y los caracoles, es clave para implementar una estrategia de control; por lo tanto, el manejo de pastos puede desempeñar un papel integral. Aunque el clima influye claramente en los niveles de trematodos temporal y geográficamente, se ha demostrado que los factores de manejo están asociados con los niveles de trematodos en casi el mismo grado (Howell et al, 2015), por ejemplo, cercar o drenar los pastos pantanosos y evitar que el ganado pasta hábitats de trematodos. Es cierto que esto a veces es un desafío; estas áreas pueden ser difíciles de identificar, con los caracoles, de solo 5 mm a 6 mm de largo, a menudo difíciles de encontrar.
Las áreas de hábitat de trematodos también pueden cambiar durante todo el año o entre años, y los trematodos pueden viajar fuera de su «hábitat» (Knubben-Schweizer y Torgerson, 2015). El drenaje de pastos pantanosos para reducir las poblaciones de caracoles puede ser una opción; sin embargo, esto a veces entra en conflicto con los esquemas de conservación ambiental. La rotación del pastoreo para limitar la contaminación por pastos/caracoles puede ser una opción, y se puede utilizar la dosificación estratégica con el objetivo de reducir los niveles de infección por caracoles y pastos, por ejemplo, tratar a los animales en primavera antes de la participación para prevenir la infección por caracoles (aunque la presencia de reservorios de vida silvestre puede comprometer este enfoque). Poner en cuarentena a los animales comprados, incluso si se sabe que el trematodo está presente en la granja, es importante para evitar atraer poblaciones de trematodos resistentes.
Dos tratamientos de un producto dirigido a etapas de trematodo adultas o intermedias, utilizados con 6 a 10 semanas de diferencia, dependiendo del producto utilizado, pueden lograr esto sin la necesidad de triclabendazol. Otros posibles métodos de control incluyen el desarrollo de una vacuna, y aunque se están haciendo progresos en esta área, no es una opción disponible para nosotros (Molina-Hernández et al, 2015; Beesley et al, 2017).
Conclusión
El control de Fasciola es complejo debido a los muchos factores variados que pueden influir en las presiones de infección y los niveles de enfermedad en la granja (Tabla 2). Los diagnósticos imperfectos significan que los resultados deben interpretarse con cuidado, y el desarrollo de resistencia a los medicamentos y restricciones de licencia significa que no se debe confiar en los medicamentos por sí solos.
| Desafíos | Opciones |
| No específico del huésped: existe el potencial de infección cruzada entre bovinos y ovinos, y de embalses de vida silvestre. | Incluya todo el ganado en los protocolos de control y considere el impacto potencial de los embalses de vida silvestre. |
| Los niveles de infección están influenciados por el clima y la geografía, por lo que varían de año en año y de granja a granja. Los niveles generales están aumentando y las áreas que antes no se veían afectadas ahora están detectando infecciones por trematodos. | Aunque están fuertemente influenciados por factores climáticos y ambientales, se pueden tomar medidas de gestión: • Reducir la contaminación de los pastos, por ejemplo, tratar en primavera antes de la participación. • Reducir la población de caracoles, por ejemplo, mediante drenaje cuando sea apropiado. • Evite el contacto entre el ganado y los caracoles: cercar / evite pastar pastar de alto riesgo en momentos de alto riesgo (generalmente en otoño). • Repita los diagnósticos y revise los protocolos de tratamiento regularmente, dependiendo de los patrones de infección actuales. |
| El hábitat y los caracoles pueden ser difíciles de identificar. | Considere la posibilidad de realizar pruebas a diferentes grupos de animales para identificar cuándo y dónde se produce la infección. |
| Resistencia a los medicamentos (y detectándola). | • Supervisar el éxito del tratamiento y diferenciar entre el fracaso del tratamiento y la resistencia a los medicamentos. • Considere el tipo de infección presente (aguda/crónica) y use un producto apropiado. • Reserva de triclabendazol para infecciones agudas por trematodos, siempre que sea posible. • Tratar y poner en cuarentena las existencias aportadas para evitar atraer poblaciones resistentes a los trematodos. |
| No hay persistencia de fluquicidas. | Se debe suponer que los animales están en riesgo de reinfección después del tratamiento. Considere alojar/evitar el contacto con caracoles después del tratamiento. |
| El ganado vacuno y las ovejas no parecen desarrollar ninguna inmunidad protectora a la infección por trematodos. | Se debe suponer que todas las edades del ganado están en riesgo de infección al desarrollar protocolos de control. |
| Modulación inmune: puede afectar las respuestas de los animales a otras enfermedades y a las pruebas para estas enfermedades. | Este es un área que se está investigando, con avances hacia una mejor definición de los efectos del parásito en la respuesta inmune del huésped y hacia el desarrollo de una vacuna. |
Tabla 2. Control Fasciola hepática: desafíos y opciones
El manejo de pastos puede desempeñar claramente un papel en el control de la trematodo, pero puede ser difícil de implementar debido a los aspectos prácticos a nivel de granja. Es probable que los protocolos de control varíen de granja a granja y de año en año, y es probable que colaborar con los agricultores para revisarlos regularmente, y desarrollar estrategias de control dinámicas y holísticas, sea beneficioso para limitar las pérdidas de producción.
Referencias
- Beesley NJ, Caminade C, Charlier J, Flynn RJ, Hodgkinson JE, Martinez-Moreno A, Martinez-Valladares M, Perez J, Rinaldi L y Williams DJL (2017). Fasciola y fasciolosis en rumiantes en Europa: identificación de las necesidades de investigación, Enfermedades Transfronterizas y Emergentes 65 (Suplemento 1): 199-216.
- Charlier J, Vercruysse J, Morgan E, van Dijk J y Williams DJ (2014). Avances recientes en el diagnóstico, impacto en la producción y predicción de Fasciola hepatica en bovinos, Parasitología 141(3): 326-335.
- Control de gusanos de manera sostenible (2018). Fluke de hígado y rumen,https://bit.ly/2XjciWs
- Flynn RJ, Mulcahy G, Welsh M, Cassidy JP, Corbett D, Milligan C, Andersen P, Strain S y McNair J (2009). Coinfección de ganado con Fasciola hepatica y Mycobacterium bovis – consecuencias inmunológicas, enfermedades transfronterizas y emergentes 56(6-7): 269-274.
- Howell A, Baylis M, Smith R, Pinchbeck G y Williams D (2015). Epidemiología e impacto de la exposición a Fasciola hepatica en rebaños lecheros de alto rendimiento, Medicina Veterinaria Preventiva 121(1-2): 41-48.
- Hutchinson G y Macarthur E (2003). Validación del anticuerpo francés ELISA para el trematodo hepático, informe final, Meat and Livestock Australia, https://www.mla.com.au/download/finalreports? itemId=54
- Knubben-Schweizer G y Torgerson PR (2015). Fasciolosis bovina: Estrategias de control basadas en la ubicación de los hábitats de la trunctula de Galba en granjas, Parasitología Veterinaria 208(1-2), 77-83.
- Mazeri S, Rydevik G, Handel I, Bronsvoort bmd y Sargison N (2017). Estimación del impacto de la infección por Fasciola hepatica en el tiempo que tarda el ganado vacuno del Reino Unido en alcanzar el peso del sacrificio, Informes científicos 7(1): 7.319.
- McCann CM, Baylis M y Williams DJL (2010). El desarrollo de modelos de regresión lineal utilizando variables ambientales para explicar la distribución espacial de la infección por Fasciola hepatica en rebaños lecheros en Inglaterra y Gales, International Journal for Parasitology 40(9): 1.021-1,028.
- Molina-Hernández V, Mulcahy G, Pérez J, Martínez-Moreno á, Donnelly S, O’Neill SM, Dalton JP y Cwiklinski K (2015). Vacuna contra la Fasciola hepatica: puede que todavía no estemos allí, pero estamos en el camino correcto, Parasitología Veterinaria 208(1-2): 101-111.
- Salimi-Bejestani MR, McGarry JW, Felstead S, Ortiz P, Akca A y Williams DJL (2005). Desarrollo de una ELISA de detección de anticuerpos para Fasciola hepatica y su evaluación contra una prueba disponible comercialmente, Research in Veterinary Science 78(2): 177-181.
- Sargison ND y Scott PR (2011). Diagnóstico y consecuencias económicas de la resistencia al triclabendazol en Fasciola hepatica en una manada de ovejas en el sureste de Escocia, Registro Veterinario 168(6): 159.
- Scott P (2016). Control de la gripe hepática en bovinos, Servicio Nacional de Información sobre Enfermedades Animales, www.nadis.org.uk/disease-a-z/cattle/liver-fluke-control-in-cattle
- Skuce P y Zadoks R (2013). Fluke hepático: una amenaza creciente para la producción ganadera del Reino Unido, Cattle Practice 21: 138-149.
- Skuce P y Zadoks R (2017). Lucha contra la casualidad en ovejas y bovinos, Hoja de prensa, The Moredun Foundation 6(16).
Fuente VetTimes
Date de alta y recibe nuestro 👉🏼 Diario Digital AXÓN INFORMAVET ONE HEALTH
Date de alta y recibe nuestro 👉🏼 Boletín Digital de Foro Agro Ganadero
Noticias animales de compañía
Noticias animales de producción
Trabajos técnicos animales de producción
Trabajos técnicos animales de compañía
