En busca del mejor análisis sobre el tratamiento de la meningoencefalitis de origen desconocido en perros
En busca del mejor análisis sobre el tratamiento de la meningoencefalitis de origen desconocido en perros
 Mark Lowrie*
Mark Lowrie*- Hospital Veterinario Dovecote, Derby, Reino Unido
1. Introducción
El tratamiento de la meningoencefalitis de origen desconocido (MUO) sigue recibiendo una enorme cantidad de atención científica cada año. Con el fin de proporcionar a sus pacientes las mejores opciones de tratamiento, los profesionales deben estar al día de los últimos resultados de la investigación. Los veterinarios se encargan de criticar la literatura médica para mantenerse actualizados sobre los desarrollos más recientes en la gestión. Para facilitar el cuidado de un paciente, el profesional debe aportar la mejor evidencia disponible a la consulta y presentarla en términos claros para educar al propietario y capacitarlo para tomar la mejor decisión para su mascota. Los últimos estudios se entregan en revistas de investigación a la profesión veterinaria después de haber sido sometidos a una extensa revisión por pares para garantizar que transmitan un contenido de alto nivel y científicamente relevante. Sigue siendo responsabilidad del profesional examinar las ofertas de estas revistas para garantizar la ausencia de sesgos y la calidad esté asegurada. En la búsqueda del mejor manejo de la MUO, se han publicado numerosos estudios con tiempos de supervivencia y conclusiones muy variadas. La realidad de todos estos artículos de investigación es que la calidad de la base de evidencia es deficiente, compuesta predominantemente por estudios retrospectivos y análisis prospectivos ocasionales, con poca frecuencia controlados (1). Este artículo revisará el principio de intención de tratar (ITT) y su análisis inverso, por protocolo, para demostrar cómo el uso del método de análisis incorrecto en los ensayos de tratamiento con MUO puede conducir a una evaluación significativamente sesgada de la efectividad de una intervención.
2. Ensayos controlados aleatorizados
Los ensayos controlados aleatorizados (ECA) son la mejor manera de establecer relaciones causales entre las intervenciones y los resultados (2, 3). Son estos ensayos los que carecen por completo en el tratamiento de la MUO. El objetivo principal de la aleatorización es evitar el sesgo de selección y generar grupos que sean comparables entre sí. Cuando la aleatorización se realiza correctamente, se obtienen grupos con variables pronósticas equilibradas (variables que influyen en el desarrollo del resultado en estudio). Esto permite a los veterinarios argumentar de forma precisa y convincente que una diferencia en el resultado entre dos (o más) grupos pronosticados equilibrados, excluyendo la intervención, puede atribuirse a la intervención.
En general, se considera que el método de referencia para establecer relaciones causales entre las intervenciones y los resultados es la aleatorización. Sin embargo, este método no garantiza la ausencia total de sesgos. Cuando los datos se analizan incorrectamente, el sesgo puede ocurrir incluso cuando se implementa una secuencia de asignación aleatoria válida (por ejemplo, utilizando una tabla de números aleatorios o un software informático que genera una secuencia aleatoria). Con el fin de garantizar que la aleatorización siga siendo precisa durante el estudio y el análisis, es imperativo mantener su integridad. Cuando el veterinario no da a los pacientes la evaluación adecuada basada en su asignación original, los resultados pueden interpretarse incorrectamente y estar sesgados.
Cuando se interrumpe la aleatorización, el sesgo puede alterar inadvertidamente el análisis y el resultado. Esto significa que el objetivo de un investigador debe ser mantener el equilibrio pronóstico entre los grupos en todo momento durante el estudio, desde el ingreso, la asignación, la intervención, el seguimiento hasta el análisis. Un método para evaluar a los pacientes en función de su asignación inicial se denomina ITT (4). En este artículo se detalla una hipótesis estándar de MUO y se describe el diseño y la interpretación del estudio asociado, lo que ilustra cómo puede ser engañoso interpretar los resultados de los ECA sin aplicar el concepto de ITT.
2.1. ¿Por qué utilizar la intención de tratar en un ECA?
Para responder a esta pregunta consideraremos un ejemplo. Queremos evaluar la efectividad de la adición de medicación inmunosupresora adyuvante (intervención) a la prednisolona (el tratamiento convencional) en la prevención de la muerte (resultado) en pacientes con MUO (Figura 1). En nuestro ejemplo, logramos reclutar 200 perros para nuestro ECA y estos pacientes se dividen en partes iguales en dos grupos; el grupo A recibirá la intervención (prednisolona + adjunto) y el grupo B es nuestro control activo (prednisolona sola). Evaluaremos el resultado después de 3 meses.
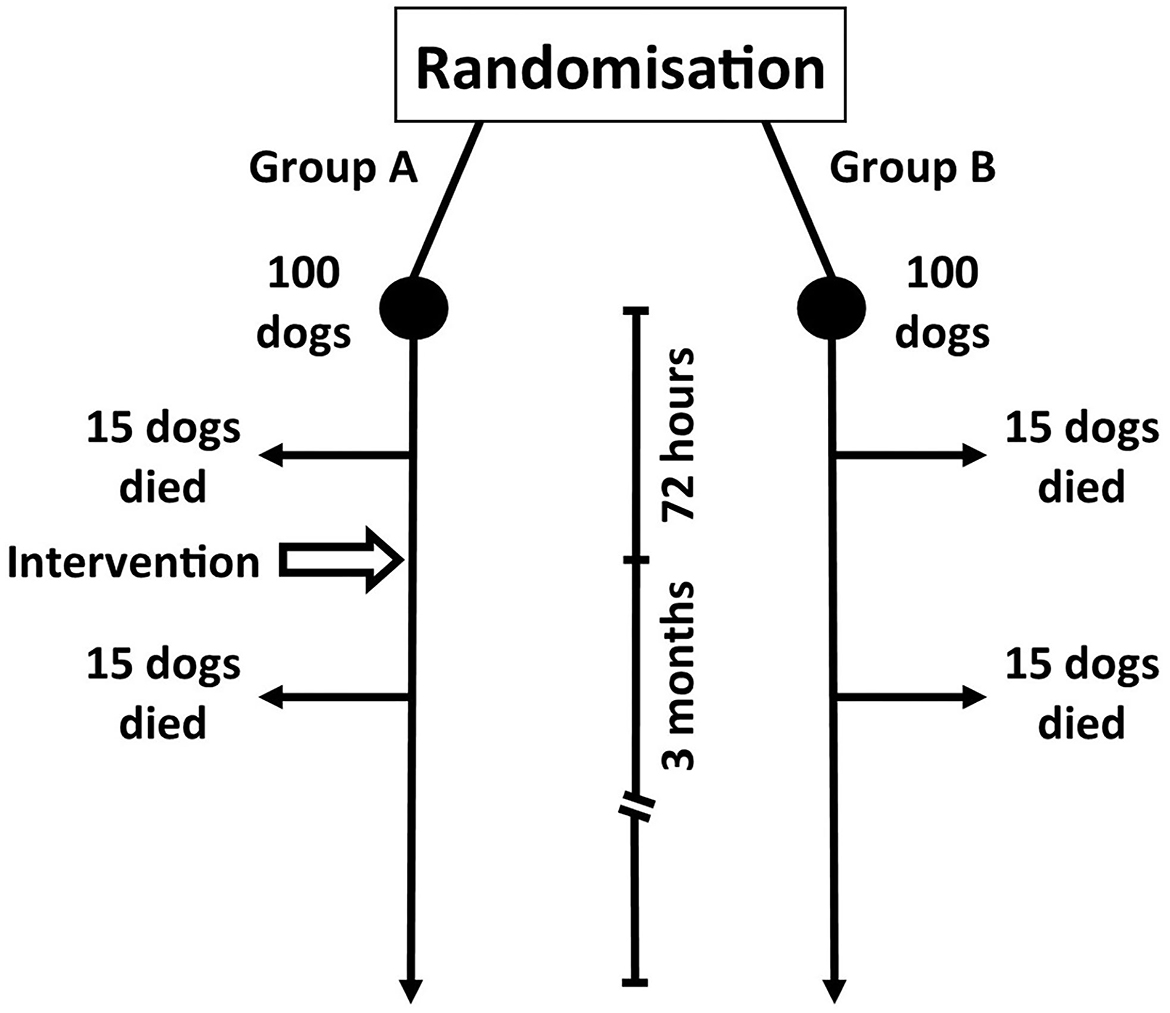 Figura 1. Estudio prospectivo hipotético que evalúa la eficacia de una intervención (Grupo A; manejo médico más complemento inmunosupresor) vs. control (Grupo B; manejo médico solamente) en perros con meningoencefalitis de origen desconocido.
Figura 1. Estudio prospectivo hipotético que evalúa la eficacia de una intervención (Grupo A; manejo médico más complemento inmunosupresor) vs. control (Grupo B; manejo médico solamente) en perros con meningoencefalitis de origen desconocido.
Es importante tener en cuenta que la naturaleza del diseño de nuestro estudio es que tenemos un período corto de 72 h entre la aleatorización (es decir, el punto de diagnóstico) y la intervención. En el seguimiento de 3 meses, 30 perros del grupo A han muerto (la principal medida de resultado del estudio). Quince de estos perros murieron dentro de las 72 h posteriores a la inscripción, mientras que los otros 15 perros murieron entre 72 h y 3 meses después. Un resultado similar se observa con el grupo B (Figura 1).
Ahora considere que agregar este medicamento inmunosupresor (intervención) no previene nuestro resultado primario (muerte). Podemos considerar esto como la «verdad». Por lo tanto, nuestro trabajo debería consistir en realizar ensayos aleatorios para determinar esta «verdad». La forma en que elijamos analizar los datos determinará si podemos llegar a una conclusión imparcial (encontrar la verdad). Utilizando el análisis correcto, deberíamos determinar que la inmunosupresión adyuvante no tiene éxito, mientras que en el análisis incorrecto, llegaremos a una suposición falsa y sesgada de que la inmunosupresión adicional mejora la mortalidad.
2.2. Análisis mediante un método por protocolo
El primer paso en nuestro análisis es considerar qué perro recibió la intervención asignada por el protocolo. Este es un método conocido como análisis por protocolo (5). Esto puede parecer algo extraño, ya que se podría suponer que todos los perros del grupo de intervención han recibido la intervención. La realidad, sin embargo, es que solo 85 perros del grupo A recibieron la intervención; 15 perros murieron antes de que pudiera ser administrado. Según este método de análisis, la tasa de mortalidad es del 0,18 o 18% (15/85), mientras que el riesgo de muerte para nuestro grupo control es del 0,3 o 30% (30/100).
El riesgo relativo de muerte se refiere a la relación entre el riesgo de muerte del grupo de intervención y el riesgo de muerte del grupo de control. En este caso, el cociente de riesgo es de 0,59 (0,18 dividido por 0,3). Para determinar la reducción del riesgo relativo de muerte debemos restar este valor de 1 para obtener un 0,41 o un 41%. En otras palabras, el análisis de datos utilizando un método por protocolo puede significar que un veterinario concluiría que la inmunosupresión adyuvante reduce el riesgo de muerte de un perro en un 41%.
Sabemos, sin embargo, que el complemento no tiene ningún efecto en la reducción de la mortalidad. Analizar la intervención de esta manera sería malinterpretar groseramente y tergiversar incorrectamente los resultados. La práctica clínica basada en una interpretación tan inexacta no beneficiaría a los pacientes que sufren por recibir una medicación inmunosupresora adicional.
Existe otro método para analizar estos datos que considera a los perros en función del tratamiento que les habían administrado en lugar del grupo al que se les designó originalmente. Este método, llamado análisis de tratamiento (3), también adolece de la introducción de sesgos de selección y, por lo tanto, elimina cualquier ventaja obtenida por la aleatorización.
Con esta estrategia, los perros que reciben el complemento dentro de la muestra de control (cualquiera que sea el motivo) se consideran participantes del grupo de intervención, y los asignados dentro del grupo de tratamiento adyuvante que no reciben el complemento se consideran participantes del grupo de control. Al evaluar los hallazgos de un ECA, el uso de métodos tratados y por protocolo aumenta la posibilidad de sesgo. Para evitar esta trampa, existe una estrategia para analizar los datos de un ECA que no dará lugar a este tipo de conclusiones erróneas. El análisis por intención de tratar (ITT, por sus siglas en inglés) es el nombre de esta técnica.
2.3. ¿Qué es el análisis por intención de tratar?
Independientemente de todos los percances que pueden ocurrir durante un estudio, ITT significa que se debe analizar a todos los perros asignados aleatoriamente a uno de los tratamientos colectivamente como representativos de ese tratamiento, ya sea que hayan recibido solo algunos o incluso ninguno de los tratamientos. De este modo, se garantiza que la aleatorización permanezca intacta y que se reduzcan las variables de confusión, preservando el equilibrio pronóstico. Por lo tanto, el uso del principio ITT en nuestro estudio requiere un seguimiento uniforme y completo de todos los perros (en la medida de lo posible) y asigna crédito por todos los eventos y resultados positivos o negativos al grupo de tratamiento aleatorio, independientemente de los cambios en el tratamiento realmente recibidos por esos perros.
Mirando hacia atrás en nuestro estudio, un perro en el grupo de intervención se enfrenta a un 30% de posibilidades de morir. Este cálculo incluye los 15 perros que murieron (el resultado primario del estudio) antes de que se administrara el medicamento adyuvante. Los perros control tienen una mortalidad del 30% (0,3 o 30/100). En comparación con el grupo control, los perros que reciben la intervención tienen un riesgo relativo de muerte de 1 (0,3/0,3) y la reducción del riesgo relativo es cero.
En consecuencia, el principio ITT es correcto al concluir que el complemento inmunosupresor es ineficaz. Se puede negar que no es razonable incluir a los 15 perros que murieron antes de que se les administrara el agente inmunosupresor. Sin embargo, esta es una práctica totalmente razonable. Altera el equilibrio pronóstico logrado por la aleatorización para eliminar a los perros de un brazo o del otro. Un ECA que excluye a los perros tiene más probabilidades de estar sesgado (6).
Los estudios que investigan los protocolos de tratamiento en MUO a menudo fracasan en este primer obstáculo. Es bien sabido que la MUO conlleva un alto riesgo de muerte dentro de las primeras 72 h (7-9). Los pacientes aleatorizados después de este período de tiempo tendrán un mejor pronóstico. El período entre la aleatorización y la asignación del tratamiento grupal también debe incluirse siempre en el análisis. Es muy frecuente que los pacientes con MUO mueran en estas primeras horas antes de la administración del tratamiento y los investigadores los excluyen del análisis; Este es un problema particular cuando los estudios retrospectivos recopilan información sobre los resultados (10, 11). El momento de la adhesión y la aleatorización en los estudios de MUO afectarán directamente a la eficacia percibida del tratamiento en cuestión. Los pacientes perdidos antes de la aleatorización no serán pronósticos idénticos a los que quedan. La omisión de pacientes que mueren antes de que se administre el tratamiento adyuvante haría que se contaran menos muertes y, en consecuencia, el análisis de los tratados estaría sesgado a favor de la inmunosupresión adyuvante. Un ejemplo de ello se muestra en un estudio retrospectivo en el que se evaluó la procarbazina como terapia adyuvante para la MUO (12). La mediana del tiempo de supervivencia reportado en 21 perros fue de 14 meses según un análisis de los tratados. Sin embargo, este estudio es digno de elogio, ya que informa que 11 perros no lograron sobrevivir para recibir tratamiento, lo que le da al estudio una tasa de mortalidad del 34% (11/32). La inclusión de estas muertes en un análisis ITT disminuiría significativamente la mediana de supervivencia general. El hecho de no reconocer estas muertes sienta un precedente peligroso. Los estudios que informan sobre el análisis de la MUO tratada a menudo brillan por su mediana de supervivencia relativamente más larga que los publicados en informes prospectivos. Una vez que se ha realizado la aleatorización, los perros (o específicamente los dueños) que no se adhieren al protocolo del grupo pueden variar en muchos aspectos, no solo en el hecho de no recibir el tratamiento asignado. Es bien sabido que los dueños adherentes tienden a tener perros que tienen un mejor resultado que los dueños de perros que no son adherentes. A este fenómeno se le denomina efecto «adherente sano» (13). Un análisis ITT mantiene el equilibrio pronóstico logrado a partir de la aleatorización, minimizando así el riesgo de que se introduzca un sesgo al crear y comparar involuntariamente grupos con variables potencialmente confusas.
La aplicación de ITT nos permite obtener una evaluación sin prejuicios de la eficacia de un tratamiento en la prevención del resultado del estudio (muerte). Cuando una intervención disminuye la probabilidad de muerte pero se reduce la adherencia al protocolo del estudio, un análisis ITT subestima el beneficio que la medicación dará a aquellos perros que se adhieran al programa de tratamiento. Al igual que con un análisis por protocolo o según el tratamiento, la ITT produce una eficacia más precisa e imparcial, aunque la magnitud de su efecto puede estar subestimada.
3. Conclusión
Los ensayos clínicos aleatorizados a gran escala para la MUO se enfrentan a una serie de desafíos, sobre todo la naturaleza variable de la afección, lo que dificulta la definición de criterios de entrada y resultados sólidos. En segundo lugar, la MUO a menudo resulta en la eutanasia de los afectados. Sin embargo, el momento y la naturaleza de esta decisión pueden diferir dadas las circunstancias individuales del propietario y del médico tratante, lo que a su vez reducirá la validez de la muerte como un marcador sólido en la eficacia del tratamiento. El camino a seguir es difícil, pero todos los estudios futuros de MUO deben considerar el nivel de evidencia presentado antes de formular observaciones finales.
Contribuciones de los autores
El autor confirma ser el único colaborador de este trabajo y lo ha aprobado para su publicación.
Conflicto de intereses
El autor declara que la investigación se llevó a cabo en ausencia de relaciones comerciales o financieras que pudieran interpretarse como un posible conflicto de intereses.
Nota del editor
Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, ni las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo, o afirmación que pueda ser hecha por su fabricante, no está garantizado ni respaldado por el editor.
Referencias
1. Granger N, Smith PM, Jeffery ND. Hallazgos clínicos y tratamiento de la meningoencefalomielitis no infecciosa en perros: una revisión sistemática de 457 casos publicados desde 1962 hasta 2008. Veterinario J. (2010) 184:290–7. doi: 10.1016/j.tvjl.2009.03.031
Resumen de PubMed | Texto completo de CrossRef | Google Académico
2. Brighton B, Bhandari M, Tornetta P, Felson DT. Jerarquía de la evidencia: desde informes de casos hasta ensayos controlados aleatorizados. Clin Orthop Relat Res. (2003) 413:19–24. doi: 10.1097/01.blo.0000079323.41006.12
Resumen de PubMed | Texto completo de CrossRef | Google Académico
3. Lund EM, James KM, Neaton JD. Diseño de ensayos clínicos: perspectivas veterinarias. J Veterinario Pasante Med. (1994) 5:317–22. doi: 10.1111/j.1939-1676.1994.tb03243.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
4. Freise KJ, Lin TL, Fan TM, Recta V, Clark TP. Medicina basada en la evidencia: el diseño y la interpretación de ensayos clínicos de no inferioridad en medicina veterinaria. J Veterinario Pasante Med. (2013) 216:1305–17. doi: 10.1111/jvim.12211
Resumen de PubMed | Texto completo de CrossRef | Google Académico
6. Fergusson D, Aaron SD, Guyatt G, Hébert P. Exclusiones posteriores a la aleatorización: el principio de intención de tratar y la exclusión de pacientes del análisis. BMJ. (2002) 325:652–4. doi: 10.1136/bmj.325.7365.652
Resumen de PubMed | Texto completo de CrossRef | Google Académico
7. Lowrie M, Smith PM, Garosi L. Meningoencefalitis de origen desconocido: investigación de factores pronósticos y resultados mediante un protocolo de tratamiento estándar. Rec. Veterinario (2013) 172:527. doi: 10.1136/vr.101431
Resumen de PubMed | Texto completo de CrossRef | Google Académico
8. Lowrie M, Thomson S, Smith P, Garosi L. Efecto de una infusión de tasa constante de arabinósido de citosina sobre la mortalidad en perros con meningoencefalitis de origen desconocido. Veterinario J. (2016) 213:1–5. doi: 10.1016/j.tvjl.2016.03.026
Resumen de PubMed | Texto completo de CrossRef | Google Académico
9. Lawn RW, Harcourt-Brown TR. Factores de riesgo de muerte prematura o eutanasia dentro de los 100 días posteriores al diagnóstico en perros con meningoencefalitis de origen desconocido. Veterinario J. (2022) 287:105884. doi: 10.1016/j.tvjl.2022.105884
Resumen de PubMed | Texto completo de CrossRef | Google Académico
10. Zarfoss M, Schatzberg S, Venator K, Cutter-Schatzberg K, Cuddon P, Pintar J, et al. Terapia combinada de arabinósido de citosina y prednisona para la meningoencefalitis de etiología desconocida en 10 perros. JSAP. (2006) 47:588–95. doi: 10.1111/j.1748-5827.2006.00172.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
11. Menaut P, Landart J, Behr S, Lanore D, Trumel C. Tratamiento de 11 perros con meningoencefalomielitis de origen desconocido con una combinación de prednisolona y arabinósido de citosina. Rec. Veterinario (2008) 172:527. doi: 10.1136/vr.162.8.241
Resumen de PubMed | Texto completo de CrossRef | Google Académico
12. Coates JR, Barone G, Dewey CW, Vitale CL, Hollway-Azene NM, Sessions JK. Procarbazina como terapia adyuvante para el tratamiento de perros con diagnóstico presuntivo antemortem de meningoencefalomielitis granulomatosa: 21 casos (1998-2004). JVIM. (2007) 21:100–6. doi: 10.1111/j.1939-1676.2007.tb02934.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
13. Simpson SH, Eurich DT, Majumdar SR, Padwal RS, Tsuyuki RT, Varney J, et al. meta-análisis de la asociación entre la adherencia a la terapia farmacológica y la mortalidad. BMJ. (2006) 333:15–21. doi: 10.1136/bmj.38875.675486.55
Resumen de PubMed | Texto completo de CrossRef | Google Académico
Palabras clave: meningoencefalitis de origen desconocido (MUO), supervivencia, ensayo controlado aleatorizado, canino, muerte, análisis por protocolo, análisis por intención de tratar, inmunosupresión
Cita: Lowrie M (2023) En busca del mejor análisis respecto al tratamiento de la meningoencefalitis de origen desconocido en perros. Frente. Vet. Sci. 9:1062114. doi: 10.3389/fvets.2022.1062114
Recibido: 05 de octubre de 2022; Aceptado: 12 de diciembre de 2022;
Publicado: 04 Enero 2023.
Editado por:
Daisuke Hasegawa, Universidad Japonesa de Veterinaria y Ciencias de la Vida, Japón
Revisado por:
Marios Charalambous, Universidad de Medicina Veterinaria de Hannover, Alemania
Karen Munana, Universidad Estatal de Carolina del Norte, Estados Unidos
Derechos de autor © 2023 Lowrie. Este es un artículo de acceso abierto distribuido bajo los términos de la Licencia Creative Commons Attribution License (CC BY).
*Correspondencia: Mark Lowrie,  mark.lowrie@dovecoteveterinaryhospital.co.uk
mark.lowrie@dovecoteveterinaryhospital.co.uk
Renuncia: Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, ni las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo o afirmación que pueda hacer su fabricante no está garantizado ni respaldado por el editor.
Date de alta y recibe nuestro 👉🏼 Diario Digital AXÓN INFORMAVET ONE HEALTH
Date de alta y recibe nuestro 👉🏼 Boletín Digital de Foro Agro Ganadero
Noticias animales de compañía
Noticias animales de producción
Trabajos técnicos animales de producción
Trabajos técnicos animales de compañía

