Farmacocinética de esomeprazol en cabras (Capra aegagrus hircus)

Farmacocinética de esomeprazol en cabras (Capra aegagrus hircus) después de la administración intravenosa y subcutánea
 Rachel Fladung1
Rachel Fladung1  Joe S. Smith1,2*
Joe S. Smith1,2*  Melissa T. Hines1
Melissa T. Hines1  Windy Michelle Soto-González1
Windy Michelle Soto-González1  Bryanna Fayne1
Bryanna Fayne1  Rebecca R. Rahn1
Rebecca R. Rahn1  Olivia Grace Escher1
Olivia Grace Escher1  Lainey Harvill1
Lainey Harvill1  Joan Bergman3
Joan Bergman3  Jessica D. García1
Jessica D. García1  Amanda Jo Kreuder4
Amanda Jo Kreuder4  Jerez Cox3
Jerez Cox3- 1Large Animal Clinical Sciences, Facultad de Medicina Veterinaria, Universidad de Tennessee, Knoxville, Knoxville, TN, Estados Unidos
- 2Ciencias Biomédicas, Facultad de Medicina Veterinaria, Universidad Estatal de Iowa, Ames, IA, Estados Unidos
- 3Ciencias Biomédicas y de Diagnóstico, Facultad de Medicina Veterinaria, Universidad de Tennessee, Knoxville, Knoxville, TN, Estados Unidos
- 4Microbiología Veterinaria y Medicina Preventiva, Facultad de Medicina Veterinaria, Universidad Estatal de Iowa, Ames, IA, Estados Unidos
Fondo: Las cabras estresadas y hospitalizadas están en riesgo de desarrollar ulceración abomasal (gástrica), pero hay una escasez de estudios farmacocinéticos para los fármacos inhibidores de la bomba de protones, como el esomeprazol en cabras.
Objetivos: Los objetivos de este estudio fueron estimar los parámetros farmacocinéticos plasmáticos para esomeprazol en cabras adultas después de la administración intravenosa (IV) y subcutánea (SQ). Un objetivo secundario fue describir la cinética plasmática del metabolito esomeprazol sulfona después de la administración IV y SC en cabras.
Materiales y métodos: Se administró esomeprazol a 5 cabras adultas en un estudio cruzado a dosis de 1 mg/kg IV o 2 mg/kg SC. Las muestras de plasma se recogieron durante 36 h y se analizaron mediante HPLC de fase inversa para determinar las concentraciones de esomeprazol y esomeprazol sulfona. Los parámetros farmacocinéticos se derivaron mediante análisis no compartimental.
Resultados: Después de la administración IV, valores medios para el aclaramiento plasmático (Cl), la vida media de eliminación [T1/2 (λz)], C0 y volumen de distribución (Vz) de esomeprazol se estimaron en 24,9 mL/min/kg, 6 min, 2,324 μg/mL y 0,23 L/kg, respectivamente. Después de la vida media de eliminación de la administración SC, la concentración máxima (Cmax) y el tiempo hasta la concentración máxima (Tmax) de esomeprazol se estimaron en 29 min, 1.038 μg / ml y 22 minutos respectivamente. Las concentraciones máximas del metabolito sulfona fueron de 32 y 18 ng/ml después de la administración IV y SC.
Conclusión: Esomeprazol se eliminó rápidamente del plasma después de la inyección IV y SC en cabras. La vida media de eliminación en cabras parece ser más corta que la reportada en perros, así como menor que la reportada para pantoprazol en cabras. El metabolito sulfona se detectó y también se eliminó rápidamente del plasma después de la administración IV y SC. Se necesitan investigaciones farmacodinámicas adicionales para determinar la eficacia de esomeprazol en la supresión del ácido abomasal (gástrico) en cabras y podría incluir dosis mayores o vías de administración adicionales.
Introducción
La ulceración abomasal (gástrica) es una enfermedad multifactorial de muchas especies de rumiantes, así como una causa común de morbilidad y mortalidad. La prevalencia de úlceras abomasales varía sustancialmente debido a las diferencias en las poblaciones, pero las úlceras abomasales se pueden encontrar en rumiantes de todas las edades y sistemas de producción (1-4). Los signos clínicos varían de leves (anorexia/hiporexia) a graves (muerte aguda), pero a menudo son vagos y difíciles de interpretar definitivamente como indicadores de ulceración abomasal. Los factores que contribuyen a la ulceración incluyen factores como la edad, el clima, la vivienda, el estrés, el trauma, la nutrición, el crecimiento excesivo de bacterias y la administración de un medicamento antiinflamatorio no esteroideo (AINE) (5-7). Los pequeños rumiantes colocados en un nuevo entorno, como un hospital, pueden experimentar altos niveles de estrés fisiológico, y muchos de estos pacientes hospitalizados también reciben un AINE como parte de su protocolo de tratamiento. Los AINE inhiben la síntesis de prostaglandinas; Las prostaglandinas dentro del abomaso actúan de múltiples maneras para proteger el revestimiento de la mucosa (1). Una reducción en estos mecanismos de protección deja la superficie mucosa susceptible al daño por el ambiente ácido del abomaso. A pesar del riesgo de ulceración abomasal en estos pacientes, no existen tratamientos aprobados para esta afección en pequeños rumiantes.
Los inhibidores de la bomba de protones (IBP) como el pantoprazol y el omeprazol son utilizados rutinariamente por médicos de animales grandes para tratar la ulceración gástrica en caballos y muchas especies de rumiantes, incluyendo ovejas, cabras, camélidos y ganado (7–10). Sin embargo, los estudios farmacocinéticos y farmacodinámicos de los efectos de los IBP en pequeños rumiantes son limitados. Una investigación de pantoprazol administrado a cabras encontró que el aclaramiento plasmático del fármaco era menor para los pequeños rumiantes que para los miembros de otras especies, como potros, terneros y alpacas (6). Este estudio también informó que la vida media de eliminación fue menor que la reportada en otras especies, y que la concentración de pantoprazol administrado por vía intravenosa o subcutánea fue indetectable después de 4 h en todos los animales (6). Un estudio previo examinó las propiedades farmacocinéticas y farmacodinámicas del pantoprazol administrado por vía intravenosa (IV) y subcutánea (SC) en alpacas (8). En ese estudio, pantoprazol, administrado IV o SC, alcanzó concentraciones terapéuticas en el plasma y aumentó significativamente el pH del tercer compartimento. Sin embargo, la disponibilidad de pantoprazol y esomeprazol puede ser limitada, y otros IBP, como el esomeprazol, siguen sin investigarse en cabras.
Los estudios farmacocinéticos de esomeprazol, el S-enantiómero del omeprazol, administrados a pacientes humanos muestran que esomeprazol tiene un metabolismo hepático de primer paso reducido, un aclaramiento plasmático más lento y una mayor concentración plasmática de área bajo la curva (AUC) que la de omeprazol (11). Esomeprazol se acumulará en los canalículos secretores ácidos de las células parietales gástricas y se une irreversiblemente a las enzimas H+/K+ ATPasa (11). Un estudio mostró que el esomeprazol tiene resultados prometedores en el mantenimiento de un pH elevado del jugo gástrico de los caballos (12). En ese estudio, esomeprazol magnesio administrado por vía oral (60 u 80 mg) en caballos mantuvo un pH gástrico de 5 o más hasta 6 h después de la administración (12). No se encontraron reacciones adversas después de la administración del fármaco. También se demostró que esomeprazol eleva el pH gástrico a 4 o más después de administrarse por vía intravenosa en caballos (12).
A pesar del uso potencial de esomeprazol en rumiantes, actualmente ningún estudio informa de la farmacocinética en cabras. Esomeprazol se propone para la investigación como un tratamiento para utilizar en los hospitales para prevenir el desarrollo o la perpetuación de la ulceración abomasal. El esomeprazol se investiga como un medicamento que puede tener concentraciones terapéuticas prolongadas en cabras que otros medicamentos inhibidores de la bomba de protones. Sobre la base de trabajos previos con pantoprazol en alpacas y cabras, así como la dosificación comparativa, se propuso una dosis similar para la determinación farmacocinética en cabras. No se han asociado efectos secundarios a corto plazo con el uso de la clase de fármacos inhibidores de la bomba de protones en pequeños rumiantes como las cabras, pero se necesitan más estudios para confirmar esta observación. El objetivo principal de este estudio fue determinar la farmacocinética plasmática de esomeprazol en cabras adultas sanas después de la administración intravenosa (IV) y subcutánea (SC) única. Un objetivo secundario adicional de este estudio fue investigar la farmacocinética del metabolito sulfona después de la administración IV y SC de esomeprazol en cabras adultas sanas.
Materiales y métodos
Animales
El protocolo fue revisado y aprobado por el Comité Institucional de Cuidado y Uso de Animales (IACUC) de la Universidad de Tennessee, Knoxville (número de protocolo: 2825-0221). Cinco cabras adultas sanas fueron utilizadas para este estudio. Tres cabras eran pigmeas y dos eran cruces pigmeos. Los pesos fueron de 42,1 ± 6,1 kg y las edades de las cabras fueron de 3,2 ± 0,7 años. Dos cabras eran machos castrados y tres de las cabras eran hembras intactas. Las cabras se obtuvieron del rebaño de cabras de enseñanza mantenido en el Centro de Investigación y Educación Veterinaria de la Universidad de Tennessee. La dieta durante el estudio consistió en heno de hierba ad libitum. Ninguno de los animales había sido medicado dentro de las cuatro semanas anteriores al estudio y todos estaban al día con la vacunación contra Clostridium perfringens tipos C y D, así como contra el tétanos.
Administración y muestreo de medicamentos
Antes de la inscripción para el estudio, todas las cabras se consideraron sanas según el examen físico realizado por un especialista veterinario de animales grandes certificado por la junta. Antes de la administración intravenosa, todas las cabras tenían catéteres yugulares intravenosos colocados asépticamente como se informó anteriormente, (13) con un catéter designado para la recolección de sangre y otro designado para la administración de medicamentos. Esomeprazol se reconstituyó a una concentración de 8 mg/ml en el vial del fabricante con 5 ml de cloruro de sodio al 0,9% (inyección de cloruro de sodio, USP). Se administró una dosis de 1 mg/kg de esomeprazol (Esomeprazole Sodium, Mylan Int., USA) por vía intravenosa a cada cabra. Las muestras de sangre se recogieron a las 0, 5, 10, 20, 30 y 45 min y 1, 1,5, 2, 3, 4, 8, 12, 18, 24 y 36 h después de la administración del fármaco. Las muestras de sangre se colocaron en tubos de heparina de litio después de la recolección, se colocaron inmediatamente en hielo durante varios minutos y luego se hilaron inmediatamente y se transfirieron a viales criogénicos para su almacenamiento a -80 ° C hasta el análisis. Después de un período mínimo de lavado de 10 días, las cabras se cruzaron con un solo catéter intravenoso colocado y una dosis de 2 mg / kg de esomeprazol administrada por vía subcutánea en la región axilar izquierda caudal hasta el codo. Después de la administración, se recogieron muestras de sangre y se conservaron como se describe para la administración intravenosa.
Análisis de muestras
El análisis de esomeprazol y su metabolito en muestras de plasma se realizó utilizando el método de cromatografía líquida de alta resolución (HPLC) en fase inversa basado en un método previamente validado para pantoprazol en plasma de cabra (14). El sistema consistía en un módulo de 2.695 separaciones y un detector de absorbancia UV de 2.487 (Waters, Milford, MA, US). Los compuestos se separaron en una simetría C18 (4,6 x 150 mm, 5 μm) columna con una simetría C de 5 μm18 columna de guardia (Waters, Milford, MA, US). La fase móvil fue una mezcla de acetato de amonio de 20 mM y acetonitrilo (75:25). El caudal fue de 1 mL/min y la absorbancia se midió a 290 nm.
Esomeprazol y su metabolito se extrajeron de muestras de plasma utilizando un método de extracción líquido-líquido. Las muestras que se congelaron previamente se descongelaron, se mezclaron con vórtices y se transfirieron 100 μl de plasma a un tubo superior de rosca de 13 x 100 mm, seguido de 10 μl de tinidazol (patrón interno, 10 μg / ml) y 1 ml de cloroformo. Los tubos se agitaron durante 10 minutos y luego se centrifugaron durante 10 minutos a 1.000 x g. La capa orgánica se transfirió a un tubo de vidrio y se evaporó a sequedad con gas nitrógeno. Las muestras se reconstituyeron en 225 μL de fase móvil y se analizaron 100 μL.
La validación del método se realizó de acuerdo con las Directrices Bioanalíticas de la FDA (FDA) (15). Las curvas estándar para el análisis plasmático se prepararon fortificando el plasma combinado no tratado con esomeprazol y su metabolito, lo que produjo un rango de concentración lineal de 5-5000 ng / ml. La recuperación, exactitud y precisión se determinaron mediante el análisis de cinco réplicas a concentraciones bajas, medias y altas dentro del rango de concentración de la curva. La recuperación se calculó como el porcentaje de la respuesta del fármaco después de la extracción en comparación con la respuesta del fármaco en el estándar a una concentración conocida. Las concentraciones de control de calidad (QC) utilizadas fueron 15, 75, 300, 1.300 y 4.000 ng/mL. La recuperación para esomeprazol varió de 99% ± 2 a 101% ± 5, mientras que el rango para el metabolito fue 99% ± 2 a 103% ± 5 para 15, 75, 300, 1.300 y 4.000 ng/mL, respectivamente. La recuperación promedio para el estándar interno fue del 99% ± 2. La precisión del ensayo estuvo dentro de 100, 99, 102, 102 y 101% para esomeprazol y 106, 105, 105, 103 y 103% para el metabolito para las concentraciones de control de calidad utilizadas. La precisión del ensayo fue (expresada como CV%) 0,77, 4,09, 2,62, 7,32 y 7,93% para esomeprazol y 5,99, 8,55, 2,47, 3,61 y 7,58% para el metabolito para las concentraciones de control de calidad. El límite inferior de cuantificación para ambos fue de 5 ng/mL.
Análisis farmacocinético
Los parámetros farmacocinéticos para esomeprazol en cabras se determinaron a partir de los datos de tiempo plasmático frente a concentración descritos previamente para el análisis no compartimental (6, 9, 16). El análisis de la farmacocinética para cada individuo se realizó con un software de modelado comercial utilizando un enfoque de momentos estadísticos (PKanalix, Monolix Suite 2020R1, Lixoft, Francia).
Se generaron parámetros farmacocinéticos estándar para animales individuales, como se informó anteriormente (6, 9):
1. Concentración máxima extrapolada al tiempo cero, C0 (esomeprazol).
2. Área bajo curva de concentración-tiempo de esomeprazol, AUCúltimo y AUCInf.
3. Área bajo la curva de momento, AUMCInf.
4. Esomeprazol tiempo medio de residencia, MRT = AUMCInf/AUCInf.
5. Vida media terminal de esomeprazol, T1/2 (λ z)) = ln (2)/λz.
6. Aclaramiento sistémico de esomeprazol, CL = dosis/AUCInf.
7. También se informa: Volumen de distribución y Biodisponibilidad (F), con Biodisponibilidad calculada como, AUCSC/AUCIV x DosisIV/DosisSC. Se utilizó una regla trapezoidal logarítmica para el análisis de datos para estimar el área bajo las curvas de tiempo de esomeprazol. Posteriormente, se realizaron estadísticas resumidas sobre los parámetros farmacocinéticos individuales para derivar la media geométrica, la mediana y el rango (min-max). Los parámetros farmacocinéticos para el metabolito sulfona se determinaron a partir de los datos de tiempo plasmático frente a concentración descritos anteriormente (6, 17).
Resultados
Sanidad animal
Durante la duración del estudio no se observaron efectos adversos para la salud en ninguna de las cabras. De los animales incluidos en el estudio, ningún animal mostró inapetencia o actitud o mentalidad anormal. No hubo evidencia del desarrollo de edema, reacciones en el lugar de la inyección o reacciones en el sitio del catéter. No hubo evidencia de reacción anafiláctica o reacciones adversas a lo largo de este estudio.
Parámetros farmacocinéticos
La Tabla 1 muestra la media geométrica, la mediana, el mínimo y el máximo de los parámetros farmacocinéticos de esomeprazol en cabras después de la administración IV y SQ. La Tabla 2 muestra la media geométrica, mediana, mínimo y máximo de los parámetros farmacocinéticos de esomeprazol sulfona en cabras después de la administración IV y SQ. La biodisponibilidad de esomeprazol después de la administración SC fue del 116%.
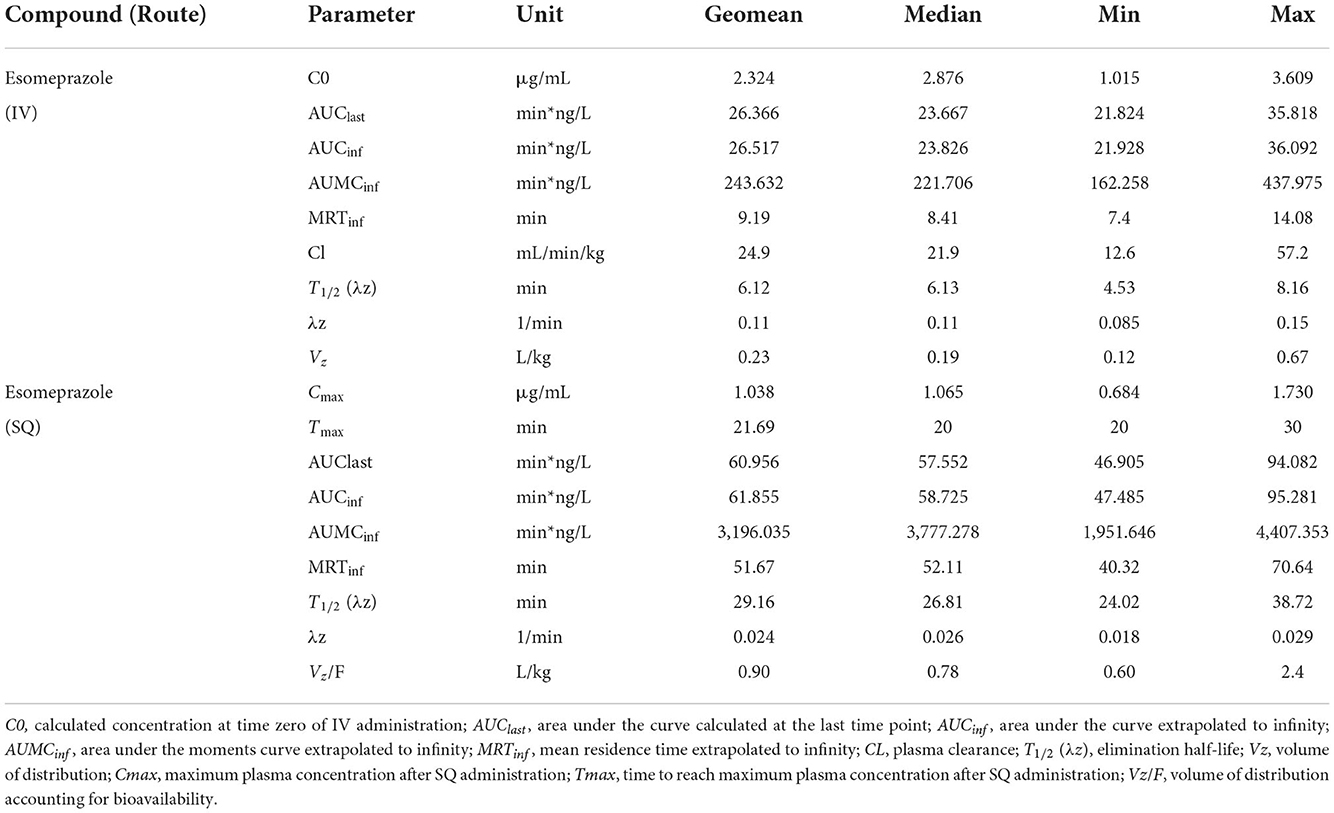 Tabla 1. Parámetros farmacocinéticos de esomeprazol después de la administración intravenosa (IV: 1 mg/kg) y subcutánea (SC: 2 mg/kg) en cabras (n = 5).
Tabla 1. Parámetros farmacocinéticos de esomeprazol después de la administración intravenosa (IV: 1 mg/kg) y subcutánea (SC: 2 mg/kg) en cabras (n = 5).
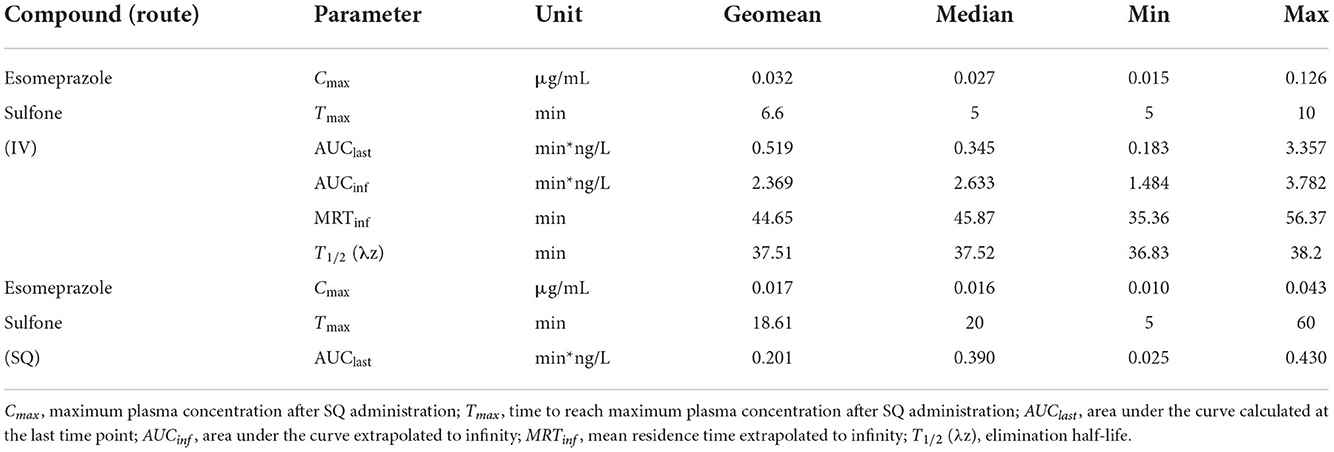 Tabla 2. Parámetros farmacocinéticos de esomeprazol sulfona después de la administración intravenosa (IV: 1 mg/kg) y subcutánea (SC: 2 mg/kg) de esomeprazol en cabras (n = 5).
Tabla 2. Parámetros farmacocinéticos de esomeprazol sulfona después de la administración intravenosa (IV: 1 mg/kg) y subcutánea (SC: 2 mg/kg) de esomeprazol en cabras (n = 5).
Las figuras 1, 2 muestran las curvas de tiempo vs. concentración para esomeprazol y esomeprazol sulfona, respectivamente.
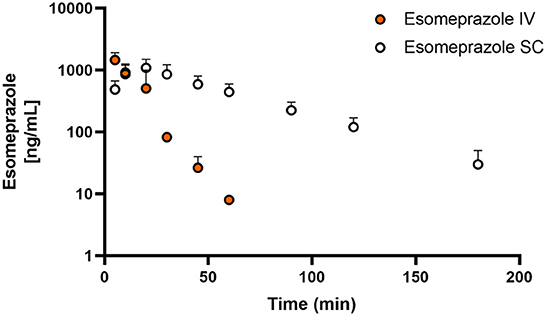 Figura 1. Concentración plasmática media de esomeprazol (escala logarítmica) frente a perfiles de tiempo (hr) para cabras adultas (n = 5) después de la administración intravenosa (IV) de dosis única de 1,0 mg/kg de esomeprazol (naranja) o subcutánea (SC) de dosis única de 2,0 mg/kg de esomeprazol (blanco). La media está representada por un círculo con barras de error estándar ascendentes.
Figura 1. Concentración plasmática media de esomeprazol (escala logarítmica) frente a perfiles de tiempo (hr) para cabras adultas (n = 5) después de la administración intravenosa (IV) de dosis única de 1,0 mg/kg de esomeprazol (naranja) o subcutánea (SC) de dosis única de 2,0 mg/kg de esomeprazol (blanco). La media está representada por un círculo con barras de error estándar ascendentes.
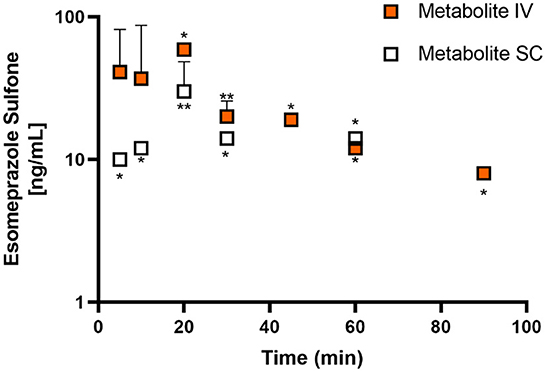 Figura 2. Concentración plasmática media de esomeprazol sulfona (escala logarítmica) frente a perfiles de tiempo (hr) para cabras adultas (n = 5) después de la administración intravenosa (IV) de dosis única de 1,0 mg/kg de esomeprazol (naranja) o subcutánea (SC) administración de dosis única de 2,0 mg/kg de esomeprazol (blanco). La media está representada por un círculo con barras de error estándar ascendentes. * indica n para el punto de tiempo si <5 animales (*: n = 1; **: n = 2).
Figura 2. Concentración plasmática media de esomeprazol sulfona (escala logarítmica) frente a perfiles de tiempo (hr) para cabras adultas (n = 5) después de la administración intravenosa (IV) de dosis única de 1,0 mg/kg de esomeprazol (naranja) o subcutánea (SC) administración de dosis única de 2,0 mg/kg de esomeprazol (blanco). La media está representada por un círculo con barras de error estándar ascendentes. * indica n para el punto de tiempo si <5 animales (*: n = 1; **: n = 2).
Discusión
El esomeprazol es el único isómero óptico del omeprazol utilizado en medicina veterinaria, y aunque muchos inhibidores de la bomba de protones se informan en la práctica clínica, no hay suficiente literatura sobre sus propiedades farmacocinéticas o farmacodinámicas, especialmente en cabras, para formular planes de tratamiento. En este estudio, las concentraciones de esomeprazol, cuando se administró IV y SC, no se detectaron después de 4 h en ningún animal. Cuando se administra una dosis única de esomeprazol (1 mg/kg) IV se caracteriza por una rápida eliminación en cabras en comparación con otras especies veterinarias, y en comparación, con otros inhibidores de la bomba de protones (6). La única especie con parámetros farmacocinéticos reportados para esomeprazol es la canina, que utilizamos para la comparación en este estudio (18, 19). Aunque hay muchos estudios farmacodinámicos equinos, no hay estudios farmacocinéticos equinos publicados. La Tabla 3 muestra los parámetros farmacocinéticos de esomeprazol en perros en comparación con este estudio. La vida media de eliminación de esomeprazol IV en las cabras de este estudio cuando se administró a 1 mg/kg fue de 6,12 min o 0,1 h. La vida media de esomeprazol SC en las cabras de nuestro estudio, cuando se administró a 2 mg/kg, fue de 29,16 min o 0,49 h. Esto es menor que la administración canina intravenosa y subcutánea de esomeprazol a 1 mg/kg, que fue de 0,73 y 0,9 h, respectivamente. La diferencia entre la mitad de vida de la administración IV vs. SC es más probable debido a la cinética del flip flop con la absorción de la administración extravascular que se superpone con la eliminación.
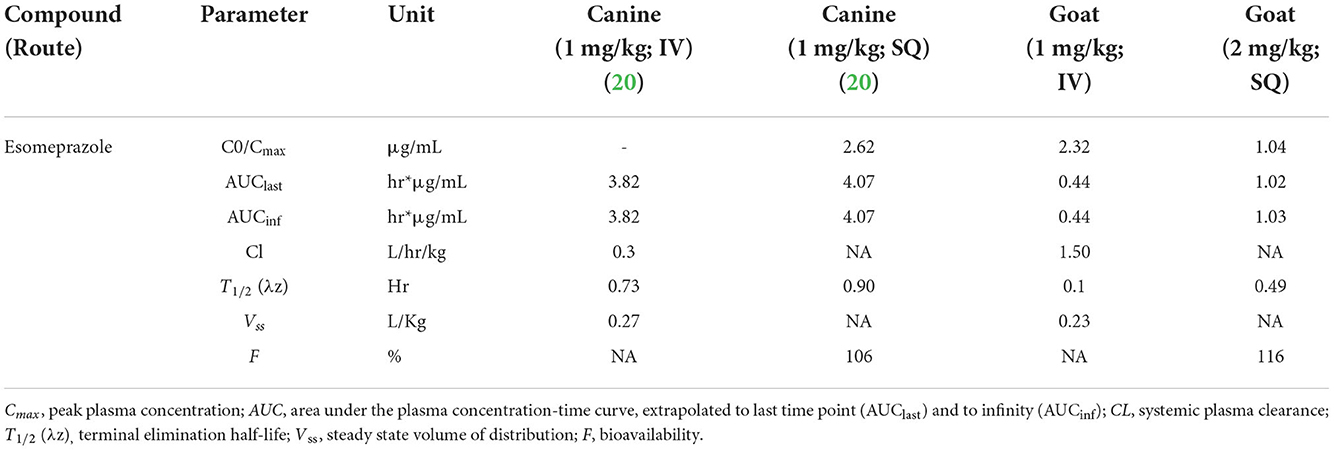 Tabla 3. Comparación de los parámetros farmacocinéticos reportados de la literatura canina y los sujetos caprinos de este estudio.
Tabla 3. Comparación de los parámetros farmacocinéticos reportados de la literatura canina y los sujetos caprinos de este estudio.
Este estudio utilizó la administración IV y SC para investigar cómo la vida media y la biodisponibilidad se ven afectadas por la vía de administración. En un entorno clínico, los inhibidores de la bomba de protones son muy utilizados, pero muy variables en la cantidad de tiempo que causan efectos terapéuticos. Debido a estudios previos de pantoprazol en pequeños rumiantes, se identificó que la administración SC tenía una vida media plasmática significativamente más larga que la administración IV (7). Los resultados de este estudio proporcionaron una línea de base para investigar múltiples vías de administración de esomeprazol. Si bien la administración IV es común en entornos hospitalarios, es más técnica que la administración SC y, como tal, la administración SC puede ser una ruta ideal para la administración en el campo por parte de los productores. Un hallazgo interesante de este estudio fue una biodisponibilidad SC del >100%. Si bien esto es inusual, podría deberse a la distribución, el programa de muestreo (posiblemente debido a que los puntos de tiempo de muestreo posteriores tienen más tiempo entre la recolección, lo que podría introducir artefactos en el área bajo el cálculo de la curva), y se ha identificado una observación similar en perros a los que se les administró esomeprazol por una ruta extravascular. El aclaramiento de esomeprazol de las cabras dentro de nuestro estudio fue de 1.050,31 ml / min (24,95 ml / min / kg), lo que es consistente con su vida media de eliminación extremadamente rápida. Debido a la falta de estudios farmacocinéticos de esomeprazol en medicina veterinaria, actualmente es difícil determinar la variabilidad de especies a especies del metabolismo, aclaramiento y efectos del esomeprazol. En los seres humanos, se cree que el esomeprazol se metaboliza en el hígado por CYP2C19 enzimas, y la mayoría del fármaco se excreta en la orina (21).
En humanos, los pacientes con enfermedad por reflujo gastroesofágico son de interés para la investigación del esomeprazol. Esomeprazol tiene una acción prolongada dentro del cuerpo y una rápida absorción en humanos, junto con una menor variabilidad entre pacientes en comparación con omeprazol. Los efectos secundarios más reportados de esomeprazol incluyen dolor de cabeza, enfermedad respiratoria, diarrea, dolor abdominal y náuseas (21). Se informa en humanos que el mantenimiento de la terapia con esomeprazol diariamente durante un máximo de 6 meses fue generalmente bien tolerado, y que un número significativamente mayor de personas fueron tratadas por enfermedad por reflujo gastroesofágico y ulceración después de 8 semanas de tratamiento (21). Sin embargo, en algunos casos, los medicamentos inhibidores de la bomba de protones, cuando se usan en hospitales veterinarios, pueden estar destinados a reducir el desarrollo de ulceración ruminal en lugar de tratar la ulceración activa. Estos hallazgos son consistentes con una investigación retrospectiva que estudia la seguridad del pantoprazol en especies de rumiantes hospitalizados (7), aunque se necesitan investigaciones de seguridad prospectivas adicionales para evaluar completamente el perfil de seguridad de este medicamento en cabras.
En un estudio en humanos, hay un grupo reportado de personas que muestran un metabolismo deficiente de esomeprazol, lo que resulta en una disminución del aclaramiento sistémico (21). Esta diferencia en la capacidad metabólica será similar para las cabras, ya que nuestro estudio identificó un animal sin metabolito de sulfona detectable después de la administración de esomeprazol SC. En los seres humanos, el metabolito sulfona no está activo dentro del cuerpo (21). La importancia del metabolito sulfona en cabras es actualmente desconocida.
Una limitación importante de esta investigación es el pequeño tamaño de la muestra de animales, pero muchos estudios farmacocinéticos de 4-6 animales son suficientes para describir los parámetros farmacocinéticos necesarios (22). Todas las cabras involucradas en el estudio no estaban relacionadas y mientras que 2 cabras eran cruces pigmeos, las otras cabras eran pigmeas, por lo que las razas utilizadas eran similares. Esomeprazol se elimina rápidamente en la cabra, tanto con administración intravenosa como subcutánea, lo que es una limitación para describir la fase de eliminación con precisión. Si bien este estudio había aumentado la frecuencia de muestreo en comparación con otros estudios farmacocinéticos de inhibidores de la bomba de protones en pequeños rumiantes, la eliminación rápida de esomeprazol puede requerir un programa de muestreo diferente o métodos más sensibles para caracterizar aún más la fase de eliminación. Actualmente se desconoce la importancia clínica de esta rápida eliminación. Debido a que esomeprazol se une irreversiblemente a la bomba de protones, los niveles sostenidos pueden ser innecesarios para cumplir con los objetivos del tratamiento. La administración de dosis más altas podría investigarse en estudios adicionales si se persigue para prolongar potencialmente la exposición al fármaco. Los estudios adicionales deben considerar una población más grande, así como modelos farmacocinéticos poblacionales (como efectos mixtos no lineales) (23) para dilucidar aún más la variabilidad entre las cabras a las que se les administró esomeprazol.
Se necesitarán más estudios sobre el metabolismo y los efectos farmacodinámicos del esomeprazol en cabras para comprender el esomeprazol y los efectos de sus metabolitos en especies de pequeños rumiantes. Actualmente no se sabe si hay una concentración específica de esomeprazol en circulación que debe alcanzarse durante un cierto período de tiempo para obtener los efectos deseados. Los estudios futuros deben investigar la eficacia de esomeprazol en cabras para determinar el potencial de diferencia en la capacidad metabólica de este fármaco en cabras, así como determinar los efectos del esomeprazol en el tracto gastrointestinal, el microbioma gastrointestinal de los rumiantes y los cambios en la acidez abomasal. El uso de esomeprazol en pequeños rumiantes se consideraría extramarcado, lo que indica que serían necesarios estudios futuros que incluyan la investigación y la determinación de los tiempos de retiro. Los estudios futuros también podrían investigar el efecto de la raza y el sexo sobre la farmacocinética de esomeprazol para determinar qué variación puede ser posible. Actualmente, también se desconoce si esomeprazol tiene algún potencial de efectos epigenéticos (24). También se justifica la investigación adicional de la administración múltiple de esomeprazol en pequeños rumiantes para estudios futuros.
En conclusión, esomeprazol administrado por vía intravenosa o subcutánea en cabras parece eliminarse muy rápidamente. Aunque se elimina rápidamente, la administración de este medicamento es bien tolerada. La vida media de eliminación y el aclaramiento plasmático parecen ser significativamente más rápidos que los reportados en los caninos. Esomeprazol sulfona, el metabolito de esomeprazol, fue detectable en plasma durante <4 h, independientemente de la vía de administración. Esomeprazol se metabolizó significativamente más rápido que el pantoprazol en pequeños rumiantes (6). En estudios futuros se debe considerar una población más grande de animales junto con estrategias de muestreo de tejidos para describir completamente la farmacocinética de esomeprazol en cabras. Se deben considerar estudios futuros que analicen la farmacodinámica del esomeprazol.
Declaración de disponibilidad de datos
Las contribuciones originales presentadas en el estudio se incluyen en el artículo / material complementario, las consultas adicionales pueden dirigirse al autor correspondiente.
Declaración ética
El estudio en animales fue revisado y aprobado por el Comité Institucional de Cuidado y Uso de Animales de la Universidad de Tennessee.
Contribuciones del autor
RF, JS, AK y SC desarrollaron el diseño experimental. RF, WS-G, RR, BF, OE, JG, JS y LH contribuyeron al apoyo logístico, la evaluación de la salud animal y la recopilación de datos. SC y JB desarrollaron el método analítico para la determinación de la concentración. JS realizó el análisis farmacocinético. Todos los autores contribuyeron a la construcción del manuscrito. Todos los autores contribuyeron al artículo y aprobaron la versión presentada.
Financiación
La autoría desea agradecer al fondo de investigación residente de Ciencias Clínicas de Grandes Animales en la Universidad de Tennessee, así como a la beca de investigación de pregrado de la Universidad de Tennessee.
Reconocimientos
Los autores desean agradecer a Laura Fischer por su ayuda con la recolección de muestras.
Conflicto de intereses
Los autores declaran que la investigación se llevó a cabo en ausencia de cualquier relación comercial o financiera que pudiera interpretarse como un posible conflicto de intereses.
Nota del editor
Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, o las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo, o reclamo que pueda ser hecho por su fabricante, no está garantizado ni respaldado por el editor.
Referencias
1. Hund A, Wittek T. Abomasal y úlceras del tercer compartimento en rumiantes y camélidos sudamericanos. Veterinario Clin North Am Food Anim Pract. (2018) 34:35–54. doi: 10.1016/j.cvfa.2017.10.003
Resumen de PubMed | Texto completo de CrossRef | Google Académico
2. Autobús JD, Stockhofe N, Webb LE. Revisión invitada: daño abomasal en terneros. J Dairy Sci. (2019) 102:943–60. DOI: 10.3168/JDS.2018-15292
Resumen de PubMed | Texto completo de CrossRef | Google Académico
3. Palmer MV, Waters WR, Whipple DL. Úlceras abomasales en ciervo cola blanca cautivo (Odocoileus virginianus). J Comp Pathol. (2001) 125:224–7. DOI: 10.1053/JCPA.2001.0496
Resumen de PubMed | Texto completo de CrossRef | Google Académico
4. Vatn S, Ulvund MJ. Hinchazón abomasal, hemorragia y úlceras en corderos noruegos jóvenes. Veterinario Rec. (2000) 146:35–9. DOI: 10.1136/VR.146.2.35
Resumen de PubMed | Texto completo de CrossRef | Google Académico
5. Mosichuk A, Smith J, Tatarniuk D, Kreuder A. Ulceración gastrointestinal en terneros presentados a un centro de referencia veterinaria de Iowa central: ¿una morbilidad subestimada? bioRxiv. (2021) 2020:2020.12.17.423269. doi: 10.1101/2020.12.17.423269
6. Smith JS, Mochel JP, Soto-Gonzalez WM, Rahn RR, Fayne BN, et al. Farmacocinética de pantoprazol y pantoprazol sulfona en cabras después de la administración intravenosa: un informe preliminar. Front Vet Sci. (2021) 8:744813. DOI: 10.3389/FVETS.2021.744813
Resumen de PubMed | Texto completo de CrossRef | Google Académico
7. Smith JS, Kosusnik AR, Mochel JP. Una investigación clínica retrospectiva de la seguridad y los efectos adversos del pantoprazol en rumiantes hospitalizados. Front Vet Sci. (2020) 7:97. DOI: 10.3389/FVETS.2020.00097
Resumen de PubMed | Texto completo de CrossRef | Google Académico
8. Smith GW, Davis JL, Smith S Smith GW, Davis JL, Smith SM, Gerard MP, Campbell NB, Foster DM. Eficacia y farmacocinética de pantoprazol en alpacas. J Vet Pasante Med. (2010) 24:949–55. doi: 10.1111/j.1939-1676.2010.0508.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
9. Olivarez JD, Kreuder AJ, Tatarniuk DM, Wulf LW, Dembek KA, Mochel JP, et al. Farmacocinética y niveles tisulares de pantoprazol en terneros neonatos después de la administración intravenosa. Front Vet Sci. (2020) 7:580735. doi: 10.3389/fvets.2020.580735
Resumen de PubMed | Texto completo de CrossRef | Google Académico
10. Poirier NC, Smith JS, Breuer RM, Farrell AM, Klostermann CA, Tseng CT, et al. Manejo de la hematometra en una cierva bóer. Clin Theriogenol. (2020) 12:39–45. Disponible en línea en: https://www.researchgate.net/publication/339390167_Management_of_hematometra_in_a_Boer_doe
11. Andersson T, Hassan-Alin M, Hasselgren G, Röhss K, Weidolf L, et al. Estudios farmacocinéticos con esomeprazol, el isómero (S)-del omeprazol. Clin Pharmacokinet. (2001) 40:411–26. DOI: 10.2165/00003088-200140060-00003
Resumen de PubMed | Texto completo de CrossRef | Google Académico
12. Videla R, Sommardahl CS, Elliott SB, Vasili A, Andrews FM. Efectos del esomeprazol sódico administrado por vía intravenosa sobre el pH del jugo gástrico en caballos hembras adultas. J Vet Pasante Med. (2011) 25:558–62. doi: 10.1111/j.1939-1676.2011.0716.x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
13. Smith JS, Borts DJ, Slagel CC, Rajewski SM, Bousquet-Melou A, Ferran AA, et al. Farmacocinética de ertapenem en ovejas (Ovis aries) con infección del tracto urinario inducida experimentalmente. Comp Med. (2019) 69:413–8. doi: 10.30802/AALAS-CM-18-000144
Resumen de PubMed | Texto completo de CrossRef | Google Académico
14. Cox S, Harvill L, Bullock S, Smith J, Bergman J. Validación de un método para pantoprazol y su metabolito de sulfona en plasma de cabra utilizando cromatografía líquida de alta resolución. J Chromatogr Abierto. (2022) 2:100038. doi: 10.1016/j.jcoa.2022.100038
15. FDA. Guía para la industria: validación de métodos bioanalíticos. (2021). Disponible en línea en: http://www.fda.gov/downloads/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/UCM070107.pdf (consultado el 28 de octubre de 2022).
16. Smith JS, Marmulak TL, Angelos JA, Lin Z, Rowe JD, Carlson JL, et al. Parámetros farmacocinéticos e intervalos estimados de retirada de leche para cabras domésticas (Capra Aegagrus Hircus) después de la administración de dosis intravenosas y subcutáneas únicas y múltiples de flunixina meglumina. Front Vet Sci. (2020) 7:213. DOI: 10.3389/FVETS.2020.00213
Resumen de PubMed | Texto completo de CrossRef | Google Académico
17. Smith JS, Coetzee JF, Fisher IW, Borts DJ, Mochel JP. Farmacocinética de citrato de fentanilo y norfentanilo en terneros Holstein y efecto de las prestaciones analíticas en la estimación de parámetros de fentanilo. J Vet Pharmacol Ther. (2018) 41:555–61. DOI: 10.1111/JVP.12501
Resumen de PubMed | Texto completo de CrossRef | Google Académico
18. Seo DH, Lee JB, Hwang JH, Jeong JW, Song GH, Koo TS, et al. Farmacocinética y farmacodinamia de esomeprazol intravenoso en 2 dosis diferentes en perros. J Vet Int Med. (2019) 33:531–5. DOI: 10.1111/JVIM.15383
Resumen de PubMed | Texto completo de CrossRef | Google Académico
19. Kuhl A, Odunayo A, Price J, Hecht S, Marshall K, Steiner J, et al. Análisis comparativo del efecto de los supresores de ácido administrados por vía intravenosa sobre el pH gástrico en perros. J Vet Int Med. (2020). DOI: 10.1111/JVIM.15718
Resumen de PubMed | Texto completo de CrossRef | Google Académico
20. Hwang JH, Jeong JW, Song GH, Koo TS, Seo KW. Farmacocinética y eficacia supresora de ácido de esomeprazol después de la administración intravenosa, oral y subcutánea a perros beagle sanos. J Vet Pasante Med. (2017) 31:743–50. DOI: 10.1111/JVIM.14713
Resumen de PubMed | Texto completo de CrossRef | Google Académico
21. Spencer CM, Faulds D. Esomeprazole. Drogas. (2000) 60:321–9. DOI: 10.2165/00003495-200060020-00006
Resumen de PubMed | Texto completo de CrossRef | Google Académico
22. Riviere JE. Pharmacokinetics comparativo: principios, técnicas y aplicaciones, 2 ed. John Wiley & Sons (2011). DOI: 10.1002/9780470959916
23. Bon C, Toutain PL, Concordet D, Gehring R, Martin-Jimenez T, Smith J, et al. Modelización y simulación matemática en sanidad animal. Parte III: uso de efectos mixtos no lineales para caracterizar y cuantificar la variabilidad en la farmacocinética farmacológica. J Vet Pharmacol therap. (2018) 41:171–83. DOI: 10.1111/JVP.12473
Resumen de PubMed | Texto completo de CrossRef | Google Académico
24. Anderson SJ, Feye KM, Schmidt-McCormack GR, et al. Efectos de fármacos fuera del objetivo que resultan en eventos de expresión génica alterados con orígenes epigenéticos y «cuasi-epigenéticos». Farmacol Res. (2016) 107:229–33. doi: 10.1016/j.phrs.2016.03.028
Resumen de PubMed | Texto completo de CrossRef | Google Académico
Palabras clave: inhibidor de la bomba de protones, úlcera, cabra (Capra aegagrus hircus), farmacocinética, esomeprazol, rumiante
Cita: Fladung R, Smith JS, Hines MT, Soto-Gonzalez WM, Fayne B, Rahn RR, Escher OG, Harvill L, Bergman J, Garcia JD, Kreuder AJ y Cox S (2022) Farmacocinética de esomeprazol en cabras (Capra aegagrus hircus) después de la administración intravenosa y subcutánea. Frente. Vet. Sci. 9:968973. doi: 10.3389/fvets.2022.968973
Recibido: 14 de junio de 2022; Aprobado: 09 Noviembre 2022;
Publicado: 15 diciembre 2022.
Editado por:
Nora Mestorino, Universidad Nacional de La Plata, Argentina
Revisado por:
Heather Knych, Universidad de California, Davis, Estados Unidos
Feray Altan, Universidad de Dicle, Turquía
Derechos de autor © 2022 Fladung, Smith, Hines, Soto-Gonzalez, Fayne, Rahn, Escher, Harvill, Bergman, Garcia, Kreuder y Cox. Este es un artículo de acceso abierto distribuido bajo los términos de la Licencia de Atribución Creative Commons (CC BY).
*Correspondencia: Joe S. Smith, jss303@iastate.edu; jsmit604@utk.edu
Renuncia: Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, o las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo o reclamo que pueda ser hecho por su fabricante no está garantizado ni respaldado por el editor.
Date de alta y recibe nuestro 👉🏼 Diario Digital AXÓN INFORMAVET ONE HEALTH
Date de alta y recibe nuestro 👉🏼 Boletín Digital de Foro Agro Ganadero
Noticias animales de compañía
Noticias animales de producción
Trabajos técnicos animales de producción
Trabajos técnicos animales de compañía
