Implementación de una vacunación eficaz contra las enfermedades respiratorias bovinas: el papel de la inmunidad de las mucosas
Implementación de una vacunación eficaz contra las enfermedades respiratorias bovinas: el papel de la inmunidad de las mucosas
Cuando un animal vacunado se expone a un desafío natural, el reconocimiento del antígeno desencadena una respuesta inmunitaria, lo que conduce a la expansión de las poblaciones de células T y células B de memoria específicas del patógeno.
Las células B continúan produciendo anticuerpos, que pueden neutralizar el patógeno o ayudar a eliminar el patógeno a través de la fagocitosis. Las células T coordinan la respuesta inmunitaria (grupo de células T colaboradoras de diferenciación [CD]4+) o reconocen y destruyen las células infectadas (células T citotóxicas CD8+). Esto permite que el animal elimine la infección antes de que el patógeno pueda causar la enfermedad.
Para que las vacunas brinden una protección óptima, deben:
- proteger a los animales a una edad en la que es más probable que el patógeno cause la enfermedad
- generar una respuesta inmune en el sitio de la infección
- generar una respuesta inmunitaria protectora adecuada
Como los virus de la enfermedad respiratoria bovina (BRD) inician la infección dentro del tracto respiratorio, la inducción de inmunidad en las superficies mucosas puede optimizar la protección contra la infección: los anticuerpos de la mucosa bloquean la entrada del virus en las células, mientras que las células T citotóxicas matan las células infectadas.
El sistema inmunitario mucoso es distinto del sistema inmunitario sistémico. Proporciona una defensa de primera línea contra la invasión de patógenos en las superficies mucosas, mediada por agregados de células inmunitarias ubicadas cerca de la mucosa. Esto se conoce como tejidos linfoides asociados a la mucosa (MALT).
La forma más eficaz de inducir respuestas inmunitarias en las mucosas es mediante la administración de vacunas en la superficie de las mucosas.
Inducción de respuestas inmunitarias mucosas específicas de antígeno 1
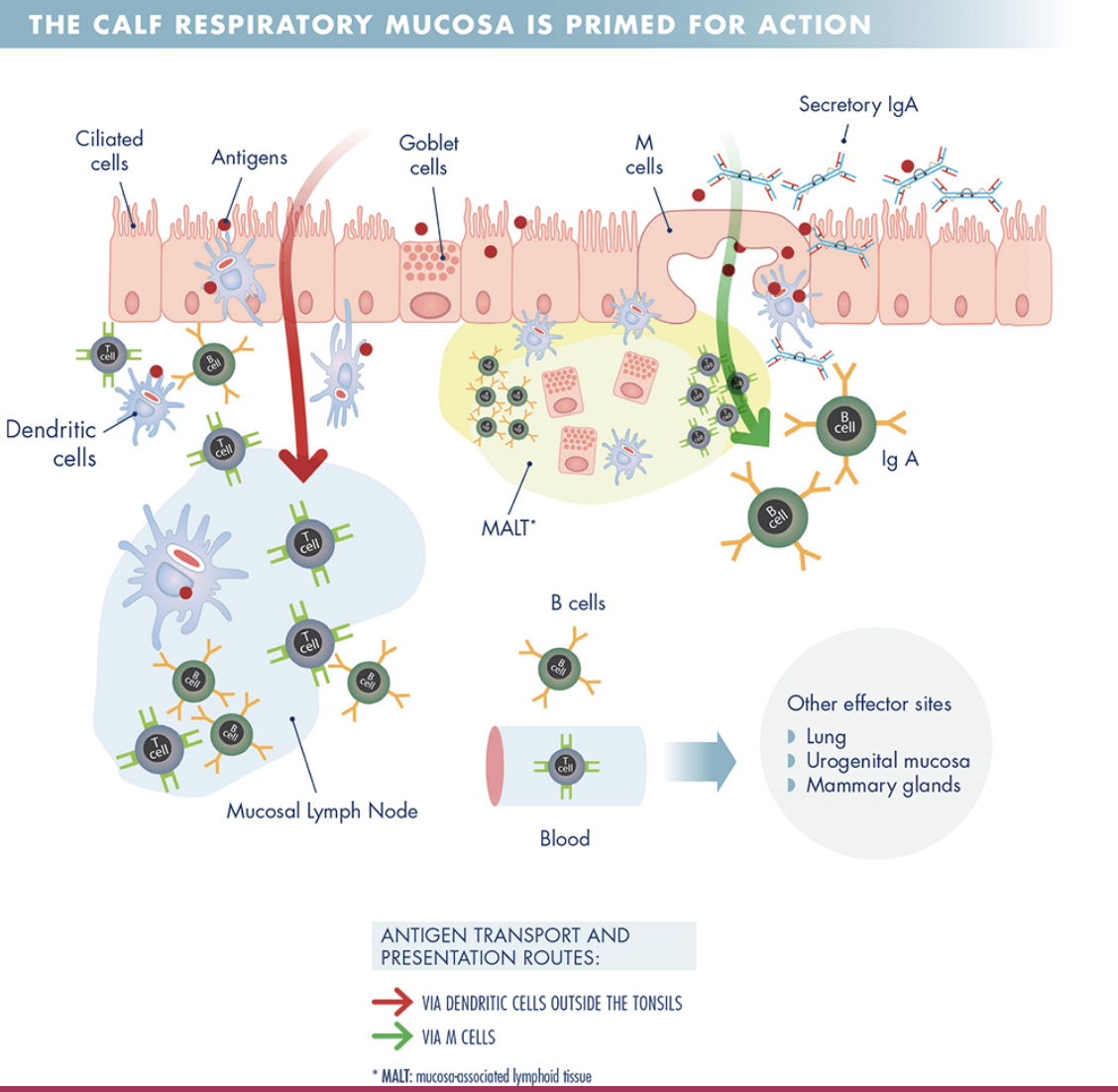
El antígeno que llega a la superficie de la mucosa es captado principalmente por las células M, o células caliciformes, y se entrega a las células dendríticas (DC) que subyacen al epitelio de la mucosa. Estas CD luego presentan este antígeno a las células T CD4+ y CD8+ en MALT o en los ganglios linfáticos de la mucosa.
El antígeno también viaja directamente al tejido linfoide, donde es reconocido por las células B específicas del antígeno.
Un subconjunto de células T auxiliares CD4+ migran a los folículos de células B dentro del tejido linfoide para ayudar a las células B a producir anticuerpos de alta afinidad. Los linfocitos B y los linfocitos T luego salen de los tejidos linfoides de las mucosas y recirculan a través de la sangre antes de volver a entrar en los tejidos de las mucosas 7 a 10 días después como resultado de los receptores de búsqueda específicos en sus superficies.
Una vez allí, las células T y las células B ejercen sus respuestas efectoras; Las células B se diferencian en células plasmáticas y producen IgA, que se secreta en la superficie de la mucosa y puede bloquear la entrada de patógenos, y las células T citotóxicas CD8+ destruyen las células infectadas. Este proceso se muestra en la Figura 1 .
Impacto de los anticuerpos maternos en las vacunas BRD
Debido a que las infecciones virales severas de BRD tienden a ocurrir en terneros jóvenes, es deseable que las vacunas funcionen frente a los anticuerpos derivados de la madre (MDA) y proporcionen una inmunidad rápida.
La unión de los anticuerpos maternos a los antígenos de la vacuna puede interferir con la respuesta a las vacunas sistémicas (inyectables). Esto inhibe la activación de las células B y atenúa la respuesta inicial de anticuerpos a la vacunación, aunque se puede inducir una respuesta de memoria de las células B, y aún ocurrirá el cebado de las células T 2 .
Los estudios han demostrado que las vacunas virales vivas atenuadas administradas por vía mucosa (intranasal) son más efectivas para inducir la protección frente a la MDA que las vacunas inactivadas o vivas administradas por inyección 3 . Un estudio reciente demostró que los terneros positivos para MDA vacunados con Bovalto® Respi Intranasal estaban protegidos contra la infección por desafío con parainfluenza-3 o virus cincitial respiratorio bovino a las 12 semanas después de la vacunación inicial 4 .
La eficacia de las vacunas mucosas frente a la MDA se debe a la presencia de niveles más bajos de anticuerpos maternos específicos del virus en la superficie mucosa en comparación con los sitios de inyección SC o IM. La inducción de inmunidad innata mediada por citocinas no específicas y la preparación eficaz de las respuestas inmunitarias celulares dentro del tracto respiratorio mejoran su efecto.
La inmunidad de las mucosas se desarrolla rápidamente, pero por lo general proporciona una duración más corta de la inmunidad que la conferida por la administración sistémica de vacunas inyectables. La vacunación de seguimiento puede extender la duración de la inmunidad contra los patógenos BRD y proporcionar una protección adecuada antes de los períodos de alto riesgo 5 .
Conclusiones
Las vacunas contra el virus BRD deben generar respuestas inmunitarias eficaces en el tracto respiratorio. Las vacunas vivas atenuadas administradas en el tracto respiratorio proporcionan un medio eficaz para lograrlo. Estas vacunas inducen respuestas inmunitarias tanto innatas como adaptativas que contribuyen a la protección contra los virus BRD y, lo que es más importante, pueden funcionar frente a la MDA, lo que permite su uso en terneros jóvenes.
Bovalto® Respi Intranasal, spray nasal, liofilizado y disolvente para suspensión contiene virus parainfluenza-3 bovino, virus vivo modificado, cepa Bio 23/A 105,0 – 107,5 TCID50 y virus respiratorio sincitial bovino, virus vivo modificado, cepa Bio 24/A 104,0 – 106.0 TCID50. Bovalto® Respi 3 Suspensión para inyección y Bovalto® Respi 4 Suspensión para inyección contienen virus respiratorio sincitial bovino inactivado, cepa BIO-24, virus de parainfluenza-3 bovina inactivado, cepa BIO-23 y Mannheimia haemolytica inactivada , serotipo A1, cepa DSM 5283. Bovalto ® Respi 4 también contiene virus de la diarrea viral bovina inactivado, cepa BIO-25. Reino Unido: POM-V. Se debe buscar el consejo del prescriptor.
Más información disponible en los SPC o en Boehringer Ingelheim Animal Health UK Ltd, RG12 8YS, Tel: 01344 746957. Correo electrónico: vetenquiries@boehringer-ingelheim.com
Bovalto® es una marca registrada del Grupo Boehringer Ingelheim. ©2020 Boehringer Ingelheim Animal Health UK Ltd. Todos los derechos reservados. Fecha de elaboración: Oct 2020. BOV-007-2021. Use los medicamentos de manera responsable.
Referencias
- Chase C y Kaushik RS (2019). Sistema inmunitario de la mucosa del ganado: todas las respuestas inmunitarias comienzan aquí, Clínicas Veterinarias de América del Norte: Práctica Animal Alimentaria 35 (3): 431-451.
- Windeyer MC y Gamsjäger L (2019). Vacunación de terneros frente a los anticuerpos maternos, Clínicas Veterinarias de América del Norte: Práctica Animal Alimentaria 35 (3): 557-573.
- Kimman TG, Westenbrink F y Straver PJ (1989). Cebado para respuestas de memoria de anticuerpos locales y sistémicos al virus sincitial respiratorio bovino: efecto de la cantidad de virus, replicación del virus, vía de administración y anticuerpos maternos, Inmunología e inmunopatología veterinaria 22 (2): 145-160.
- Metcalfe L, Chevalier M, Tiberghien MP, Jolivet E, Huňady M, Timothy S y Phillippe-Reversat C (2020). Eficacia de una vacuna intranasal viva contra la parainfluenza tipo 3 y el virus sincitial respiratorio bovino en terneros jóvenes con anticuerpos derivados de la madre, Vet Record Open 7 (1): e000429.
- Ellis J, Gow S, Berenik A, Lacoste S y Erickson N (2018). Eficacia comparativa de vacunas vivas modificadas e inactivadas para impulsar las respuestas al virus respiratorio sincitial bovino después de la preparación de la mucosa neonatal de terneros, The Canadian Veterinary Journal 59 (12): 1,311-1,319.
Date de alta y recibe nuestro 👉🏼 Diario Digital AXÓN INFORMAVET ONE HEALTH
Date de alta y recibe nuestro 👉🏼 Boletín Digital de Foro Agro Ganadero
Noticias animales de compañía
Noticias animales de producción
Trabajos técnicos animales de producción
Trabajos técnicos animales de compañía
