Uso de vacunas en rebaños canadienses de vacas y terneros y oportunidades de mejora

Uso de vacunas en rebaños canadienses de vacas y terneros y oportunidades de mejora
 Madelana M. Lazurko1
Madelana M. Lazurko1  Nathan E.N. Erickson1
Nathan E.N. Erickson1  John R. Campbell1
John R. Campbell1  Sheryl Gow2
Sheryl Gow2  Cheryl L. Waldner1*
Cheryl L. Waldner1*- 1Departamento de Ciencias Clínicas de Grandes Animales, Western College of Veterinary Medicine, Universidad de Saskatchewan, Saskatoon, SK, Canadá
- 2Agencia de Salud Pública de Canadá, Saskatoon, SK, Canadá
Las vacunas son una de las herramientas más impactantes disponibles para que los productores de vacas y terneros controlen la enfermedad dentro del rebaño y más tarde, en los corrales de engorde. Si bien el uso de vacunas se ha estudiado en todo Canadá, los datos regionales inconsistentes y variables dificultan el análisis y la interpretación. El objetivo de este estudio fue describir los protocolos de vacunación y los factores asociados con el uso de vacunas en rebaños canadienses de vacas y terneros y definir las asociaciones entre el uso de la vacuna y los resultados de productividad. Las encuestas que describen el uso de vacunas en 2020 se recolectaron de 131 rebaños de vacas y terneros (40 orientales, 91 occidentales), reclutados a través de un programa nacional de vigilancia de ganado de carne. El noventa y dos por ciento de las vacas y novillas de reemplazo, y el 72% de los toros fueron vacunados con rinotraqueítis infecciosa bovina (IBR), virus de la diarrea viral bovina (BVDV), virus Parainfluenza3 (PI3) y virus sincitial respiratorio bovino (BRSV). Al menos la mitad de las vacas y toros fueron vacunados contra patógenos clostridiales y vacas y novillas para diarreas virales de terneros. Las vacunas clostridiales tenían significativamente más probabilidades de usarse en el oeste de Canadá en comparación con el este de Canadá. Mientras que el 92% de los productores vacunaron a los terneros lactantes contra IBR/BRSV/PI3, solo el 47% proporcionó una segunda vacuna antes del destete; El 78% de los terneros también fueron vacunados al menos una vez contra el BVDV antes del destete. Los productores que vacunaron a los terneros contra IBR/BRSV/PI3 antes de los 3 meses de edad proporcionaron una segunda dosis antes del destete con más frecuencia que los productores que administraron la primera vacuna IBR/BRSV/PI3 más tarde. El uso de vacunas ha aumentado en todo Canadá, particularmente en terneros, antes del destete. En relación con las recomendaciones de la etiqueta para la vacunación anual, las vacunas clostridiales generalmente fueron subutilizadas en vacas y toros, y por los productores en el este de Canadá en comparación con el oeste de Canadá. También existen oportunidades para mejorar el cumplimiento de las recomendaciones de la etiqueta para la dosis de refuerzo de la vacuna contra los residuos cuando se usa en novillas de reemplazo criadas. Los protocolos que incluyen la elección de productos, el momento y el impulso de las vacunas respiratorias en terneros lactantes varían ampliamente entre los rebaños. El uso de vacunas intranasales en terneros neonatales de menos de 2 semanas de edad ha aumentado en el oeste de Canadá en comparación con informes anteriores. Es necesario comprender mejor cómo el momento de la vacunación en terneros lactantes contribuye a la efectividad, para la enfermedad respiratoria en terneros lactantes y destetados.
1. Introducción
La vacunación del ganado vacuno de carne ha demostrado ser eficaz para estimular la respuesta inmunitaria y reducir la carga de la enfermedad en una variedad de diseños de estudio (1-8). Sin embargo, otros estudios sobre el uso de vacunas en rebaños de vacas y terneros y en la entrada en el corral de engorde han demostrado una efectividad más variable (9-18). El cumplimiento de los protocolos de vacunación basados en la evidencia puede mejorar la salud animal y aumentar la eficiencia de la producción a través del control y la prevención de enfermedades económicamente importantes. Por ejemplo, dos metaanálisis recientes resumieron la evidencia de la mitigación del riesgo de aborto y otras consecuencias negativas para la reproducción de la rinotraqueítis infecciosa bovina (IBR) y el virus de la diarrea viral bovina (BVDV) (2, 7).
La vacunación contra enfermedades reproductivas y clostridiales es comúnmente recomendada por los veterinarios (19). La Asociación Americana de Profesionales Bovinos (AABP) identificó los siguientes objetivos como vacunas básicas para todo el ganado de carne: IBR, BVDV, Virus Parainfluenza3 (PI3), Virus Respiratorio Sincitial Bovino (BRSV) y enfermedades clostridiales con la etiqueta para todos los productos autorizados que requieren o recomiendan la revacunación anual (20). La AABP recomienda vacunas virales vivas modificadas (MLV) para IBR y BVDV debido a la mayor eficacia en comparación con las vacunas muertas o inactivadas (20).
Los veterinarios deben recomendar otras vacunas sobre una base de rebaño individual, en función de factores de riesgo específicos y ubicación geográfica (20). Varios estudios han documentado causas de morbilidad y razones para el uso de antimicrobianos en rebaños de terneros. Por ejemplo, una encuesta de 2015/2016 de productores de terneros de Ontario y una encuesta de 2017 de productores de terneros de vaca del oeste de Canadá encontraron que los criadores neonatales de terneros (13-52%) y la enfermedad respiratoria de terneros antes del destete (15-16%) fueron causas importantes de mortalidad total antes del destete (21, 22). La enfermedad respiratoria es la razón más reportada para el uso de antimicrobianos tanto en rebaños de vacas y terneros como en corrales de engorde (23, 24). Las vacunas comerciales etiquetadas para ayudar en el control de los desechos y las enfermedades respiratorias están disponibles y se usan comúnmente en rebaños de vacas y terneros (25), aunque los resultados de los ensayos de campo publicados son variables tanto para los criaderos de terneros como para el predestete de enfermedades respiratorias (10, 12).
El momento de la administración de la vacuna debe considerarse para optimizar la eficacia, particularmente para el control de la enfermedad respiratoria. Si bien se ha demostrado que la vacunación antes del destete reduce el tratamiento de la enfermedad respiratoria en relación con la vacunación en o después del destete y nuevamente en la llegada al corral de engorde (26, 27), no se observó un mejor rendimiento durante todo el período de alimentación en estos estudios para los terneros vacunados antes del destete. La evidencia que apoya los efectos beneficiosos de la administración de vacunas respiratorias a la llegada al corral de engorde es aún más limitada, ya que muchos estudios muestran asociaciones negativas o nulas con la vacunación (26, 28-31). La falta de incentivos económicos actuales para que los productores de vacas y terneros vacunen completamente a los terneros antes de la venta para prevenir enfermedades respiratorias en los corrales de engorde limita la participación de los productores de vacas y terneros.
La literatura sobre la adopción y el uso nacional de vacunas en la industria canadiense de terneros es escasa. Sin embargo, informes recientes de la industria que utilizan datos de encuestas de productores de vacas y terneros han demostrado el uso regional de vacunas dentro de Canadá. Los estudios del oeste de Canadá han descrito previamente los protocolos de vacunación para los siguientes años: 2016/2017 (21), 2010 (5) y 2001/2002 (6). Los productores de vacas y terneros del este de Canadá han sido encuestados sobre el uso de vacunas en las provincias atlánticas (2017) (32), Ontario (2015/2016) (33, 34) y el norte de Quebec (2015) (34).
Una encuesta anterior del oeste de Canadá encontró que los productores de terneros utilizaron al menos una vacuna en vacas, novillas, terneros no destetados, terneros destetados y toros en 97, 97, 96, 57 y 72% de los rebaños, respectivamente (25). Los objetivos de vacunación más comunes para los terneros fueron las enfermedades clostridiales, y las vacunas respiratorias y reproductivas fueron las vacunas más comunes para toros, vacas y novillas de reemplazo (25). Los productores del este de Canadá habían reportado previamente el uso de vacunas entre vacas, novillas, terneros y toros en Ontario de 70, 72, 88 y 59% y en el norte de Quebec de 72, 78, 94 y 68%, respectivamente (33, 34). No se informaron datos similares para los rebaños del Atlántico, pero el 73% de los productores informaron haber vacunado al ganado y el 45% vacunó a las hembras antes de la reproducción (32).
El objetivo principal de este estudio fue describir la adopción de vacunas en rebaños de vacas y terneros en todo Canadá y proporcionar una mejor comprensión de los tipos de vacunas utilizadas y el momento de administración. Los resultados se utilizarán para investigar las diferencias regionales y las oportunidades de mejora en la aceptación de la vacunación y el cumplimiento de los protocolos recomendados. El objetivo secundario de este estudio fue examinar los factores asociados con el uso de vacunas y explorar posibles asociaciones entre el uso de vacunas y los resultados de productividad del rebaño.
2. Materiales y métodos
Este estudio fue aprobado por la Junta de Ética de Investigación del Comportamiento de la Universidad de Saskatchewan (Beh-REB # 309).
2.1. Diseño y contenido de la encuesta
Se desarrolló una encuesta en papel basada en una herramienta probada y utilizada en rebaños del oeste de Canadá en 2016 (25). La encuesta solicitó datos de rebaño desde el 1 de enero de 2020 hasta el 31 de diciembre de 2020, y se dividió en dos partes: la Parte A preguntó sobre las características del rebaño, las prácticas de manejo y la adopción de tecnología (datos informados en otros lugares), y la Parte B preguntó sobre protocolos específicos de vacunación del rebaño. Los productores describieron el uso de la vacuna completando una serie de tablas de texto abiertas para cada grupo de producción: toros, vacas, novillas de reemplazo, terneros destetados y terneros lactantes. Cada tabla se dividió en filas, según el objetivo de la vacuna (por ejemplo, toros: reproductivos, clostridiales, respiratorios, podredumbre del pie, ántrax y otros) con espacio para permitir múltiples vacunas por objetivo. Se registraron los nombres de las vacunas comerciales y se seleccionó el tiempo de administración en relación con otras actividades de manejo del rebaño de una lista (por ejemplo, toros: antes de la reproducción, después de la reproducción u otra) junto con un indicador de si fue la primera o posterior administración de una vacuna. También se pidió a los productores que identificaran los principales factores considerados al decidir vacunar a los terneros lactantes y seleccionar los protocolos de vacunación del rebaño. Una copia de la encuesta está disponible del autor correspondiente a petición.
Para facilitar la finalización de la encuesta, se alentó a los productores a consultar sus registros, recibos de gastos y veterinarios, si es necesario, para obtener más detalles. Además, se les proporcionó un manual que enumeraba y describía las vacunas bovinas, con fotografías en color asociadas del empaque de productos para vacunas actualmente aprobadas para su uso en ganado de carne en Canadá como ayuda para el retiro. El manual fue desarrollado en consulta con veterinarios de ganado de carne en ejercicio.
Los atributos del rebaño, incluidos los datos de parto, salud y productividad para la temporada de reproducción hasta el destete de 2020, se recopilaron en junio y diciembre de 2020 utilizando una encuesta adaptada de una encuesta de productividad previamente probada y probada con productores canadienses de terneros (35). Los datos de esta encuesta se extrajeron y se integraron con los resultados de la encuesta sobre el uso de vacunas.
2.2. Reclutamiento de participantes y distribución de encuestas
Todos los productores de vacas y terneros que participan en la Red Canadiense de Vigilancia de Vacas y Terneros (C3SN), una red nacional de vigilancia de la salud y la productividad del ganado establecida en 2018, recibieron la encuesta. Los requisitos de elegibilidad para C3SN incluyeron: un tamaño de rebaño de cría de ≥40 animales, mantenimiento de registros de parto, pruebas de embarazo de rutina y acceso al correo electrónico. Los rebaños fueron reclutados a través de veterinarios, grupos provinciales de productores y redes sociales (36). En julio de 2021, se enviaron encuestas de vacunación por correo a 162 rebaños participantes en todo Canadá.
2.3. Gestión de datos y análisis estadístico
Las respuestas se ingresaron en un programa comercial de hoja de cálculo y se verificó su precisión haciendo que una segunda persona revisara la entrada de datos y a través de verificaciones lógicas. Los nombres comerciales de las vacunas notificados por los productores estaban vinculados a una lista de vacunas autorizadas para su uso en ganado vacuno canadiense de acuerdo con el Compendio de Productos Veterinarios (37) para determinar cada uno de los componentes objetivo de la vacuna. Se obtuvieron detalles adicionales del producto, si fue necesario, directamente del embalaje y las etiquetas del producto. Los datos de la encuesta sobre el uso de vacunas se combinaron con los datos de atributos del productor y los registros de producción (Microsoft Access; Microsoft, St. Louis, Missouri, Estados Unidos).
Los factores potencialmente asociados con el uso de la vacuna, incluido el tamaño del rebaño de vacas (pequeño: <100 animales, mediano: 100-300 animales, grande: >300 animales), la edad del productor (<40 años) y el nivel de educación del productor (postsecundaria vs. escuela secundaria), se investigaron en una serie de análisis incondicionales (univariados) utilizando regresión logística (StataCorp LP, College Station, Texas).
El análisis de las asociaciones de interés entre el uso de vacunas y los datos de productividad se investigó utilizando ecuaciones de estimación generalizadas para tener en cuenta la agrupación de resultados dentro del rebaño, una función de enlace logit, distribución binomial y estructura de covarianza intercambiable (SAS para Windows versión 9.4, SAS Institute, Cary NC). Los recuentos de los resultados de interés para cada rebaño se incluyeron como numerador y el número total de animales en riesgo en cada rebaño como denominador ajustando el tamaño del rebaño de vacas, el mes de parto y la ubicación geográfica como posibles factores de confusión basados en datos recientes de esta región (35). Las asociaciones se informaron como odds ratios (OR) con intervalos de confianza del 95%; p < 0,05 fue considerado estadísticamente significativo.
3. Resultados
3.1. Población de estudio
Los rebaños inscritos en Columbia Británica (6), Alberta (38), Saskatchewan (27) y Manitoba (18) fueron identificados como del oeste de Canadá (69% (91/131)), mientras que los rebaños de Ontario (20), Quebec (16), Nueva Escocia (2) y Nuevo Brunswick (2) fueron identificados como del este de Canadá (31% (40/131)). Los rebaños se describieron como principalmente comerciales (60%, 79/131), principalmente de raza pura / semilla (4%, 5/131) y mixtos comerciales / de raza pura (36%, 47/131).
El número medio de vacas reproductoras por rebaño fue de 193 (mediana 130, percentil 5 y 95 40, 527). El número medio de vacas reproductoras por rebaño en las operaciones occidentales fue de 244 (mediana 190, percentil 5 y 95 64, 644) y 76 (mediana 65, percentil 5 y 95 33, 162) en los rebaños orientales. En promedio, las operaciones tuvieron 34 novillas criadas (mediana 20, 5º y 95º percentil 1, 105) y productores comprados en 7 hembras reproductoras de reemplazo (mediana 0, 5º y 95º percentil 0, 30) durante el año calendario 2020.
El veintidós por ciento de los rebaños (28/130) fueron manejados por al menos una persona menor de treinta años y el 47% (61/130) menores de cuarenta años. El treinta por ciento (38/128) de los administradores de rebaños informaron un título universitario, el 21% (27/128) un diploma universitario, el 18% (23/128) un oficio profesional, el 15% (19/128) un título de posgrado y el 16% (21/128) un diploma de escuela secundaria. Los denominadores diferían según las características del productor, ya que algunos productores se negaron a responder preguntas específicas.
Muchas operaciones se diversificaron con otras operaciones de producción de carne de vacuno; El 55% (72/131) reportó terneros en segundo plano, el 25% (33/131) mantuvo ganaderos o pastos, y el 15% (13/131) operó un corral de engorde. El treinta y cuatro por ciento (44/131) de las operaciones fueron estrictamente vaca-ternero. Más de la mitad de la cosecha de terneros de 2020 se retuvo durante al menos 2 meses después del destete en el 53% (69/131) de los rebaños. Cuarenta y cinco (31/69) por ciento de los rebaños que retuvieron terneros tenían algunas semillas. Las fechas de inicio del parto variaron e incluyeron enero (24%, 31/131), febrero (14%, 18/131), marzo (25%, 33/131) y abril (24%, 31/131). Las instalaciones de parto primario reportadas incluyeron pastizales (53%, 69/131), corrales o lotes secos (40%, 53/131) y graneros o cobertizos cubiertos (27%, 36/131). Los pastos comunitarios fueron utilizados por el 21% (27/131) de los rebaños.
3.2. Uso de vacunas en toros, vacas y novillas de reemplazo
La mayoría de los productores vacunaron toros (83%), vacas (97%) y novillas de reemplazo (95%) con al menos una vacuna entre el 1 de enero y el 31 de diciembre de 2020 (Tabla 1). Las vacas y novillas de reemplazo del 92% de los rebaños fueron vacunadas contra BVDV, IBR, BRSV y PI3, y al menos la mitad de los rebaños también vacunaron a ambos grupos contra las diarreas virales de terneros (coronavirus, rotavirus) (Tabla 1). Sin embargo, el 8% de los productores no administraron vacunas BVDV/IBR/BRSV/PI3 a hembras reproductoras y solo el 17% de los productores proporcionó una segunda vacuna contra las novillas (Tabla 1). El porcentaje de rebaños que vacunaron toros para BVDV, IBR, BRSV y PI3 fue menor que para las vacas. Las vacunas para otras enfermedades reproductivas se notificaron con menos frecuencia para los reproductores, con novillas de reemplazo más vacunadas contra Leptospira spp. (36%) y Campylobacter fetus (23%).
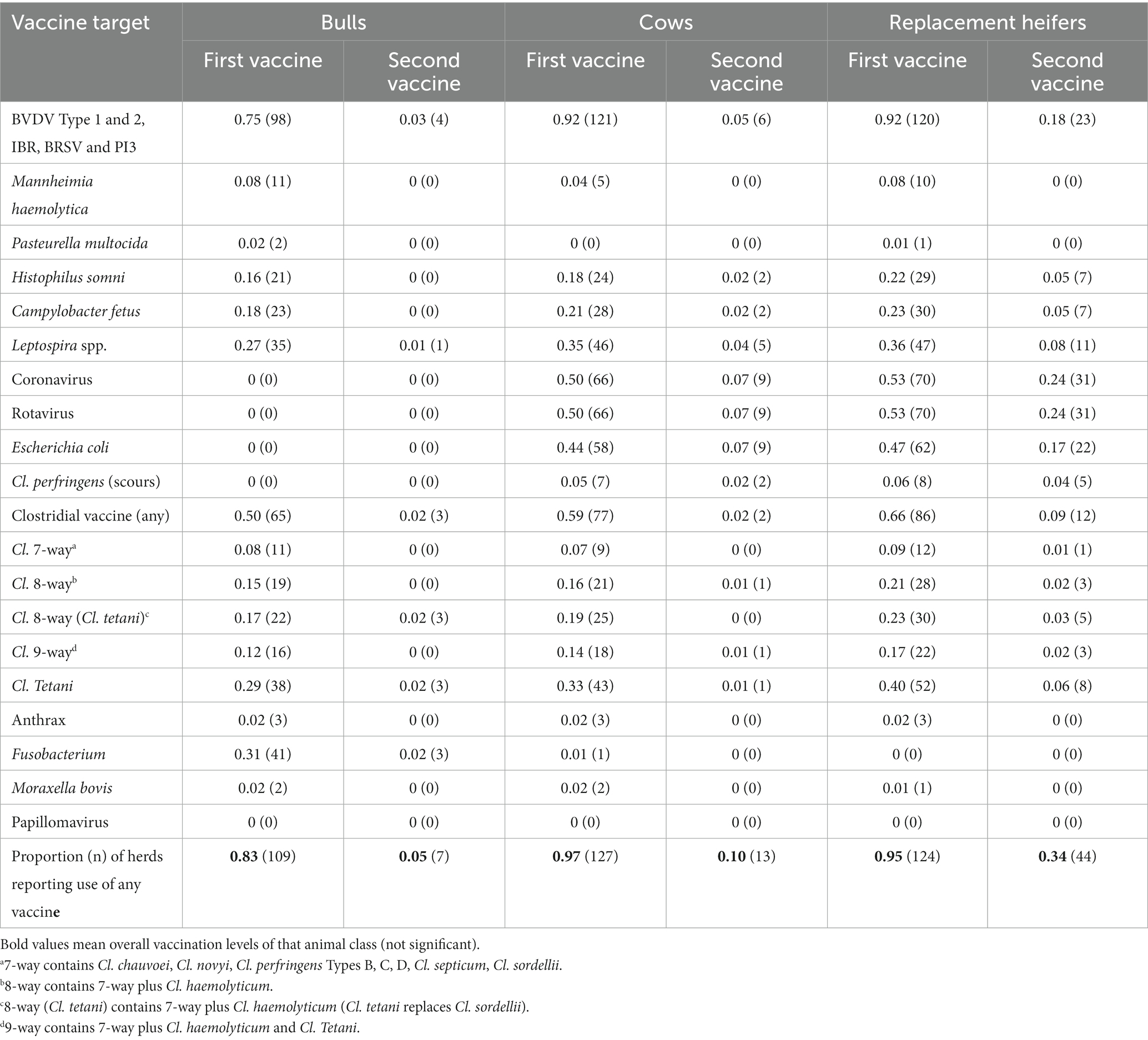 Tabla 1. Resumen de vacunas y dosis de refuerzo administradas a toros, vacas y novillas de reemplazo del 1 de enero al 31 de diciembre de 2020 en rebaños canadienses de vacas y terneros informados como proporción de rebaños (y número de rebaños) (n = 131 rebaños).
Tabla 1. Resumen de vacunas y dosis de refuerzo administradas a toros, vacas y novillas de reemplazo del 1 de enero al 31 de diciembre de 2020 en rebaños canadienses de vacas y terneros informados como proporción de rebaños (y número de rebaños) (n = 131 rebaños).
Dos tercios de los productores vacunaron a sus novillas de reemplazo contra la enfermedad clostridial, mientras que solo la mitad vacunó a sus vacas y toros durante el año (Tabla 1). Los productos de ocho vías fueron las vacunas clostridiales más comunes reportadas para toros, vacas y novillas de reemplazo (Tabla 1). La vacuna Footrot (Fusobacterium) se administró a toros en 31% de los rebaños; mientras que sólo un rebaño vacó vacas (Tabla 1).
El momento de vacunación en toros, vacas y novillas de reemplazo dependió del tipo de vacuna (Tabla 2). Más de la mitad de los productores vacunaron a las vacas y a la mayoría de las novillas de reemplazo vacunadas contra patógenos virales antes de la reproducción utilizando un producto MLV (Tabla 2). Las vacunas virales vivas modificadas se administraron con mayor frecuencia antes de la reproducción, y las vacunas inactivadas se administraron con mayor frecuencia en las pruebas de embarazo. Veinte de los 22 rebaños (91%) que administraron una vacuna MLV IBR/BVDV a novillas de reemplazo en el control del embarazo habían administrado previamente dos dosis de una vacuna MLV IBR/BVDV, y los otros dos rebaños administraron una vacuna MLV IBR/BVDV anterior. Aparte de las vacunas contra el ántrax (cultivo vivo no encapsulado), todas las demás vacunas bacterianas administradas a vacas y novillas de reemplazo fueron inactivadas. Las vacunas Campylobacter y Leptospira se administraron comúnmente antes de la reproducción (Tabla 2). Los productores que enviaron vacas a pastizales comunitarios fueron más propensos a administrar una vacuna contra Campylobacter (41%, 11/27), que aquellos que no usaron pastos comunitarios (16%, 17/104) (p < 0,01). Las vacas fueron vacunadas contra Clostridia spp. antes de la reproducción (21%), en el control de embarazo (22%) o antes del parto (15%). Las novillas fueron vacunadas contra la enfermedad clostridial antes de la reproducción en una mayor proporción de rebaños que en vacas (Tabla 2).
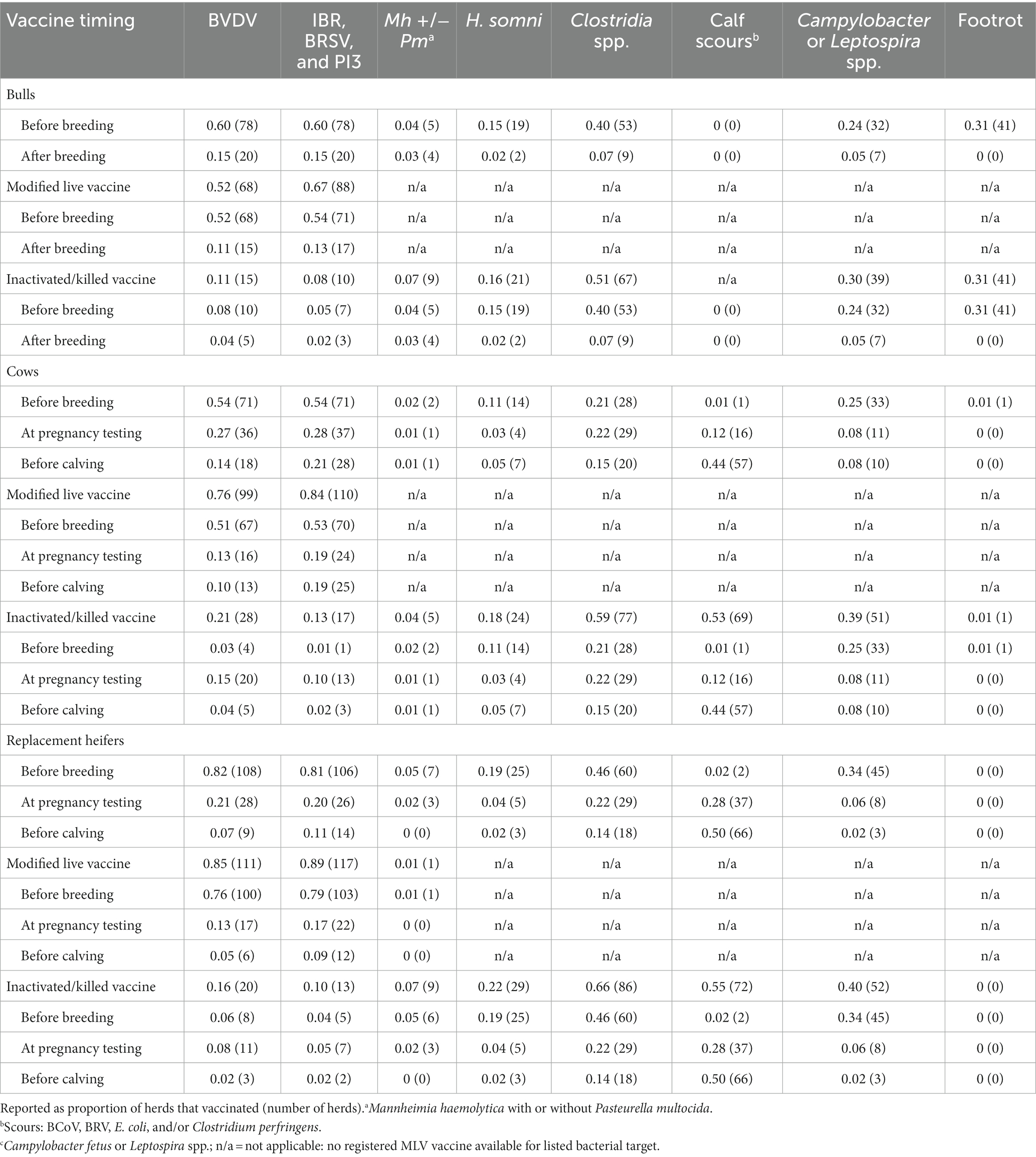 Tabla 2. Momento de vacunación y tipo de vacuna administrada a toros, vacas y novillas de reemplazo para objetivos comunes de vacunación utilizados en 131 rebaños canadienses de vacas y terneros.
Tabla 2. Momento de vacunación y tipo de vacuna administrada a toros, vacas y novillas de reemplazo para objetivos comunes de vacunación utilizados en 131 rebaños canadienses de vacas y terneros.
Los toros de la mayoría de los rebaños fueron vacunados antes de la reproducción (Tabla 2). Las vacunas vivas modificadas BVDV, IBR, BRSV, PI3 se usaron en toros más comúnmente que los productos inactivados. Dos productores administraron a sus toros una vacuna parenteral (SQ) disponible comercialmente que contenía P. multocida y M. haemolytica vivas avirulentas.
3.3. Uso de vacunas en terneros
Todos los terneros, lactantes y destetados considerados juntos, recibieron al menos una vacuna en el 99% de los rebaños y se les administró al menos una segunda dosis de un tipo de vacuna en el 82% de los rebaños (Tabla 3). Las dianas vacunales más comunes fueron IBR, BRSV, PI3, BVDV, Clostridia spp. y M. haemolytica (Tabla 3). Las vacunas con mayor probabilidad de ser seguidas por una segunda administración de una vacuna al mismo objetivo en terneros, ya sea antes, en o después del destete fueron IBR, BRSV y PI3 (77%), BVDV (61%), vacunas clostridiales (46%) y M. haemolytica (28%) (Tabla 3). Las vacunas vivas modificadas se utilizaron casi exclusivamente en terneros para objetivos respiratorios virales. A los terneros se les administró al menos una vacuna IN IBR/BRSV/PI3 antes del destete en el 33% (43/131) de los rebaños. Se administraron vacunas respiratorias bacterianas, incluyendo M. haemolytica, H. somni y P. multocida, a terneros en 62, 43 y 19% de los rebaños, respectivamente. Treinta y cuatro por ciento de todos los terneros recibieron al menos una dosis de una vacuna clostridial que contenía tétanos (Tabla 3).
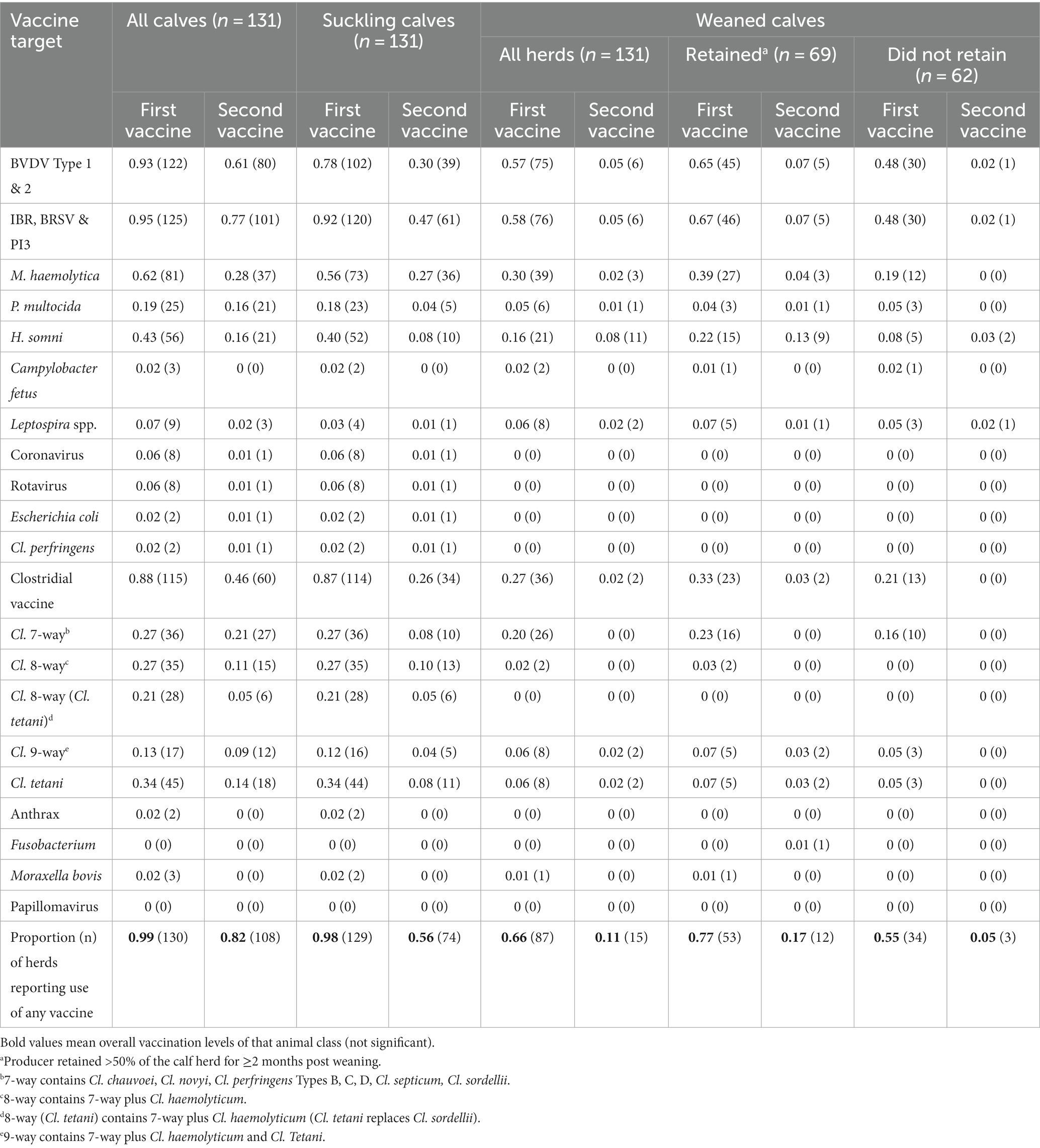 Tabla 3. Resumen de la dosis inicial de la vacuna y del tipo y dosis de refuerzo administradas a terneros lactantes y destetados del 1 de enero al 31 de diciembre de 2020 en rebaños canadienses de vacas y terneros informados como proporción de rebaños (y número de rebaños).
Tabla 3. Resumen de la dosis inicial de la vacuna y del tipo y dosis de refuerzo administradas a terneros lactantes y destetados del 1 de enero al 31 de diciembre de 2020 en rebaños canadienses de vacas y terneros informados como proporción de rebaños (y número de rebaños).
Los terneros lactantes recibieron al menos una vacuna en el 98% de los rebaños y los objetivos más comunes fueron IBR, BRSV y PI3 (92%), así como Clostridia spp. (87%), BVDV (78%) y M. haemolytica (56%) (Tabla 3). La mayoría de los terneros lactantes fueron vacunados después de las dos semanas de edad; sin embargo, los antígenos vacunales más comunes administrados antes de las 2 semanas de edad fueron para IBR/BRSV/PI3 (21%, 27/131) (Tabla 4).
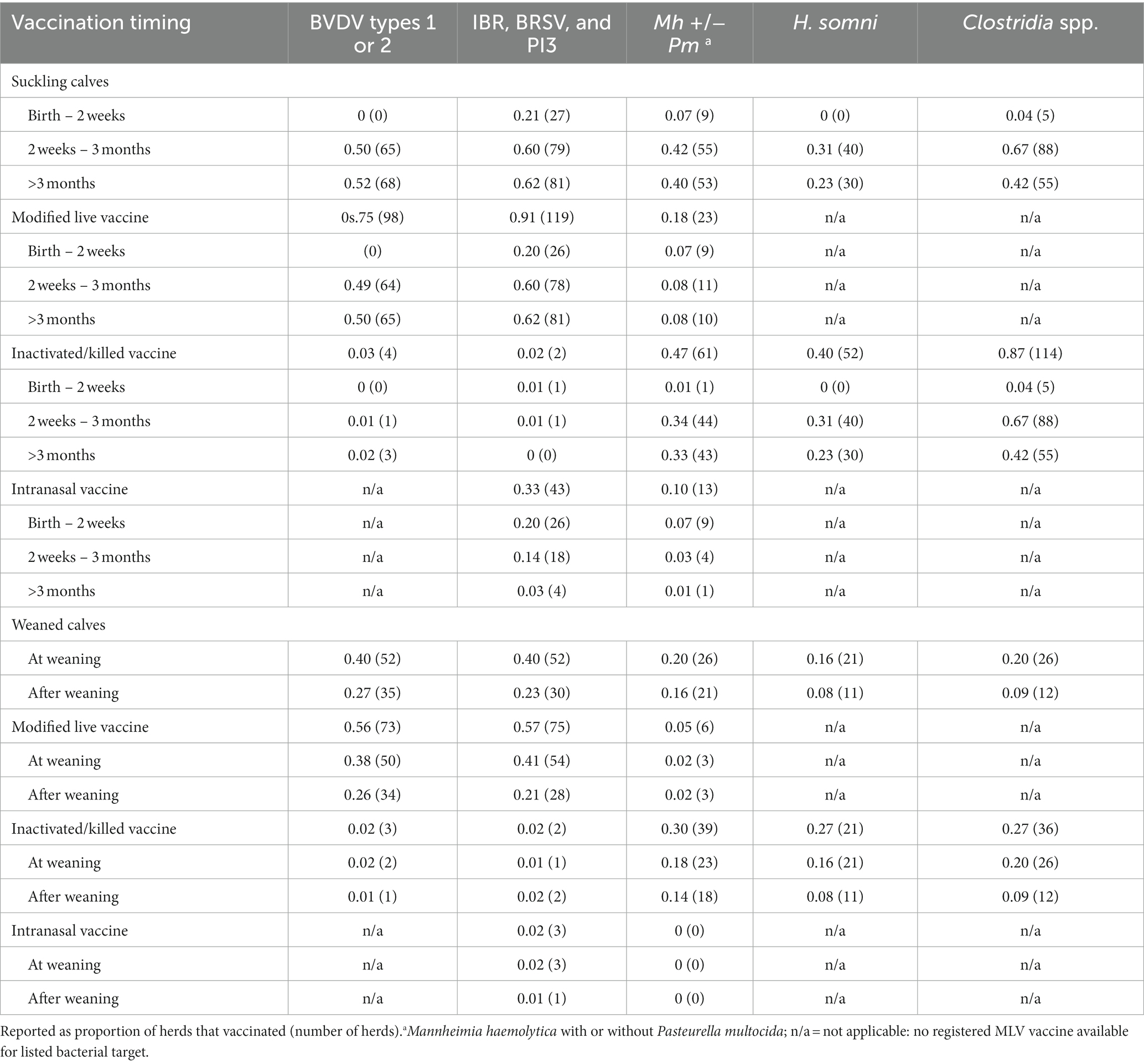 Tabla 4. Calendario de vacunación y tipo de vacuna para todas las dosis de vacuna administradas a terneros destetados y lactantes para objetivos comunes de vacunación utilizados en 131 rebaños canadienses de vacas y terneros.
Tabla 4. Calendario de vacunación y tipo de vacuna para todas las dosis de vacuna administradas a terneros destetados y lactantes para objetivos comunes de vacunación utilizados en 131 rebaños canadienses de vacas y terneros.
Sesenta y seis por ciento de los productores (87/131) vacunaron a los terneros en o después del destete, más comúnmente contra IBR / BRSV / PI3, BVDV y M. haemolytica (Tabla 3). Los productores que retuvieron el >50% de su cosecha de terneros durante ≥2 meses después del destete administraron vacunas IBR/BRSV/PI3 a los terneros en o después del destete (67%, 46/69) con más frecuencia que aquellos que no retuvieron terneros (48%, 30/62) (p < 0,05).
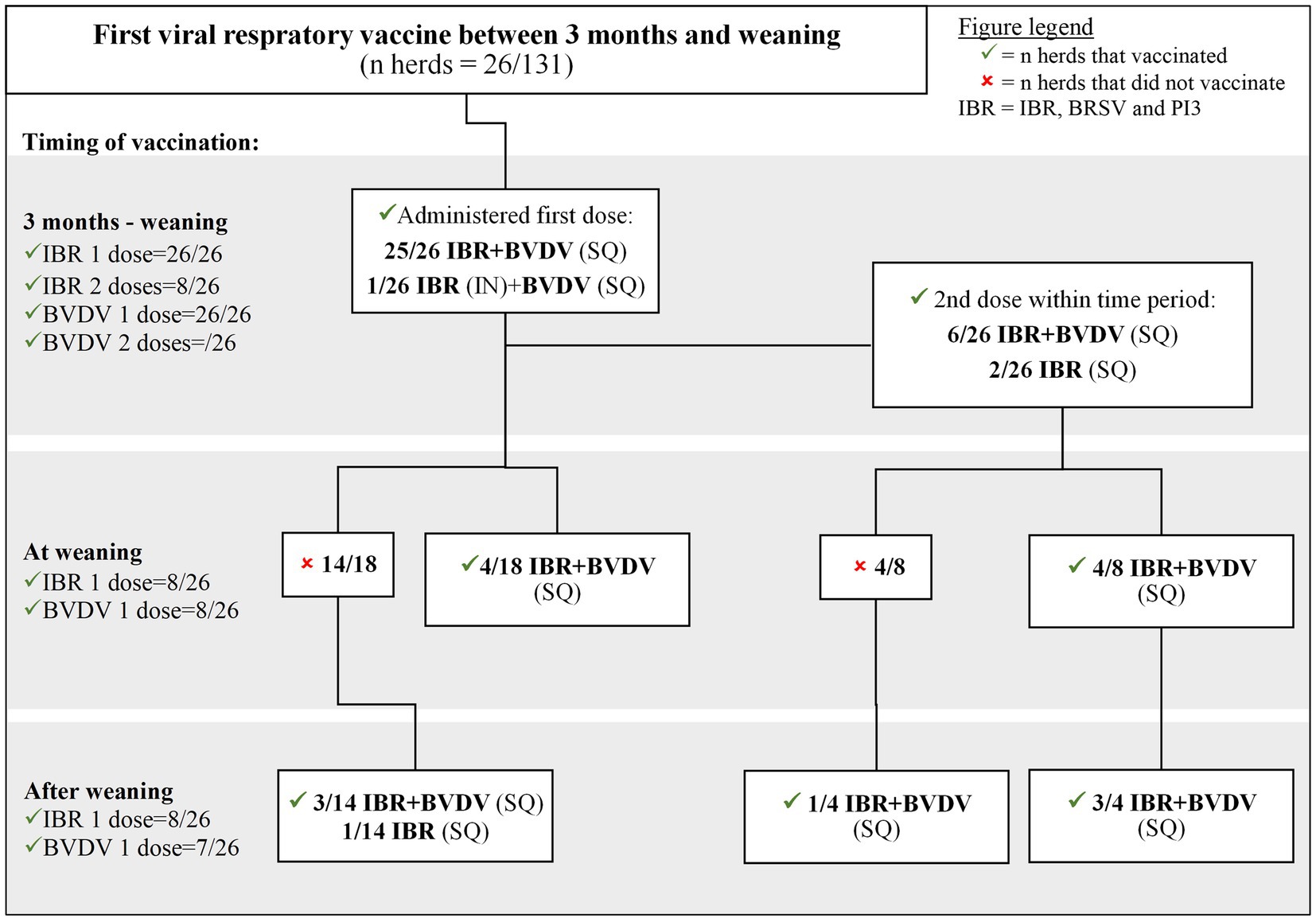
Los protocolos de vacunación para IBR/BRSV/PI3 y BVDV se agruparon en diagramas de flujo basados en el momento de la primera dosis administrada (Figuras 1-3). Veintiún (27/131) por ciento de los productores administraron vacunas IBR/BRSV/PI3 a terneros antes de las 2 semanas de edad (26 intranasales [IN], 1 subcutánea [SQ]) (Figura 1). Las vacunas contra el BVDV no se administraron antes de las 2 semanas de edad. Sesenta y siete por ciento (18/27) de los rebaños que vacunaron contra IBR / BRSV / PI3 antes de las 2 semanas de edad también recibieron una segunda dosis de IBR / BRSV / PI3 antes del destete. De los 27 rebaños vacunados contra IBR/BRSV/PI3 antes de las 2 semanas de edad, el 59% (16/27) vacunado contra BVDV y el 19% (5/27) proporcionaron una segunda dosis de BVDV antes del destete.
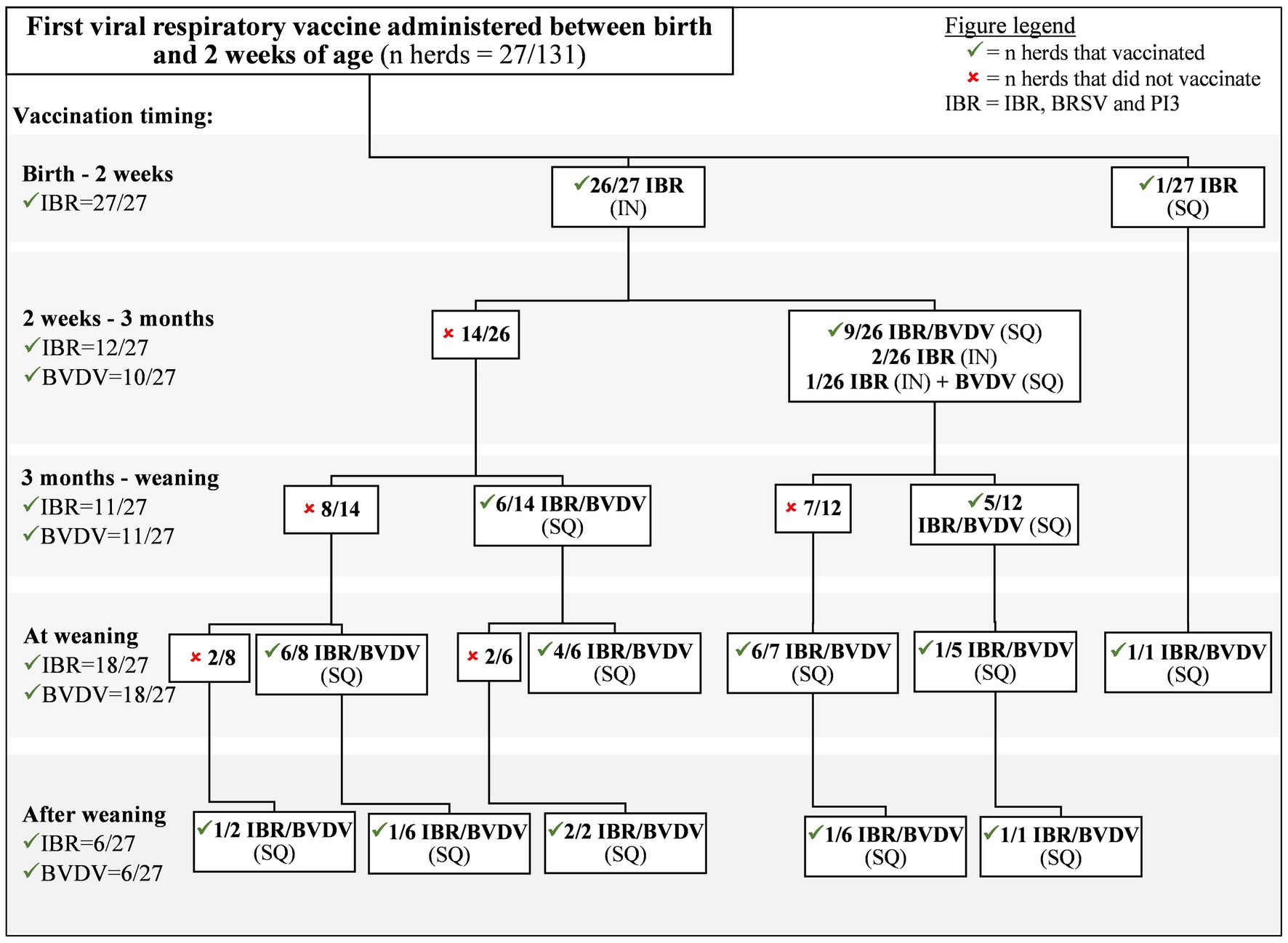 Figura 1. Protocolos de vacunas respiratorias virales de productores canadienses de vacas y terneros que vacunaron por primera vez a los terneros contra IBR, BVDV y PI3 entre el nacimiento y las 2 semanas de edad.
Figura 1. Protocolos de vacunas respiratorias virales de productores canadienses de vacas y terneros que vacunaron por primera vez a los terneros contra IBR, BVDV y PI3 entre el nacimiento y las 2 semanas de edad.
 Figura 2. Protocolos de vacunación respiratoria viral de productores canadienses de vacas-terneros que vacunaron por primera vez a terneros contra IBR, BVDV y PI3 entre las 2 semanas y los 3 meses de edad.
Figura 2. Protocolos de vacunación respiratoria viral de productores canadienses de vacas-terneros que vacunaron por primera vez a terneros contra IBR, BVDV y PI3 entre las 2 semanas y los 3 meses de edad.
Figura 3. Protocolos de vacunación respiratoria viral de productores canadienses de vacas y terneros que vacunaron por primera vez a los terneros contra IBR, BVDV y PI3 entre los 3 meses de edad y el destete.
Cincuenta y uno por ciento (67/131) de los productores administraron vacunas respiratorias virales iniciales entre las 2 semanas y los 3 meses de edad; 12 EN IBR/BRSV/PI3, 3 EN IBR/BRSV/PI3 con SQ BVDV y 52 SQ IBR/BRSV/PI3/BVDV (Figura 2). Cincuenta y dos por ciento (35/67) de los rebaños que recibieron vacunas IBR / BRSV / PI3 entre 2 semanas y 3 meses también recibieron una segunda vacuna IBR / BRSV / PI3 antes del destete. La mayoría de los rebaños administraron una vacuna contra el BVDV (88%, 59/67) y el 45% (30/67) administraron una segunda dosis de la vacuna contra el BVDV antes del destete.
No hubo diferencias significativas en si un rebaño recibiría una segunda dosis de la vacuna IBR/BRSV/PI3 (p = 0,25) antes del destete si los terneros fueron vacunados para IBR/BRSV/PI3 por primera vez entre el nacimiento y 2 semanas o 2 semanas y 3 meses. Sin embargo, los rebaños donde los terneros fueron vacunados con la vacuna IBR/BRSV/PI3 antes de las 2 semanas de edad fueron menos propensos (p = 0,04) que los vacunados de 2 semanas a 3 meses a administrar una segunda dosis de la vacuna contra el BVDV.
El veinte por ciento (26/131) de los terneros recibieron las vacunas iniciales SQ IBR/BRSV/PI3 y BVDV entre los 3 meses y el destete (Figura 3). De ellos, al 23% (6/26) se les administró una segunda vacuna SQ IBR/BRSV/PI3 y BVDV, y al 8% (2/26) se les administró una segunda vacuna SQ IBR/BRSV/PI3 antes del destete. Los terneros tenían más probabilidades de recibir una segunda dosis de la vacuna IBR/BRSV/PI3 (p = 0,03), pero no la vacuna contra el BVDV (p = 0,47), antes del destete si los terneros fueron vacunados para IBR/BRSV/PI3 por primera vez entre el nacimiento y los 3 meses que después de los 3 meses.
Las vacunas bacterianas incluyendo Clostridia spp., M. haemolytica, P. multocida y H. somni se administraron típicamente a terneros lactantes después de las 2 semanas de edad (Tabla 4). Pocos productores administraron una segunda dosis de vacuna contra M. haemolytica (27%) o Clostridia spp (26%) antes del destete (Tabla 3).
El setenta por ciento (92/131) de los productores vacunaron a los terneros contra la enfermedad clostridial antes de los 3 meses de edad, pero solo a un rebaño se le administró un refuerzo en ese período. El veinticinco por ciento (33/131) administró una segunda vacuna clostridial entre los 3 meses y el destete. El ochenta y siete por ciento (114/131) de los productores vacunaron a los terneros contra Clostridia spp. entre el nacimiento y el destete, pero solo el 26% (34/131) de los productores administraron una segunda vacuna clostridial antes del destete. Las vacunas de ocho vías con (21%, 28/131) y sin tétanos (27%, 35/131) fueron las opciones más comunes en los terneros lactantes. A los terneros lactantes se les administró al menos una vacuna que contenía Cl. tetani en 34% de los rebaños (Tabla 3). Las vacunas clostridiales de siete vías fueron la opción más común para los terneros destetados (Tabla 3).
Cuarenta y siete por ciento de los productores (61/131) administraron vacunas que contenían M. haemolytica (15%, 20/131 con P. multocida), antes de los 3 meses de edad, y cuatro productores también administraron una segunda dosis de M. haemolytica antes de los 3 meses. Treinta y cinco por ciento (46/131) vacunados contra M. haemolytica (7%, 9/131 con P. multocida) entre los 3 meses de edad y el destete. De esos 46 productores, uno administró una segunda dosis a los terneros nuevamente antes del destete, 7 impulsados al destete y 8 impulsados después del destete. Las vacunas intranasales contra M. haemolytica y P. multocida se administraron en el 10% (13/131) de los rebaños, y un rebaño proporcionó 2 dosis de una vacuna IN M. haemolytica y P. multocida antes del destete. Los 9 rebaños que vacunaron contra M. haemolytica y P. multocida entre el nacimiento y las 2 semanas usaron una vacuna intranasal.
3.4. Factores asociados al uso de vacunas
Se informaron razones de probabilidades incondicionales significativas a partir de la regresión logística donde el tamaño del rebaño de vacas, reteniendo el >50% de los terneros durante ≥ 2 meses después del destete y reportando solo ganado comercial vs. algunos de raza pura se asociaron con el uso de la vacuna (Tabla 5). Los rebaños grandes tenían más probabilidades de vacunar a las vacas y novillas contra la enfermedad clostridial, los terneros destetados contra M. haemolytica y la enfermedad clostridial, y los terneros lactantes contra H. somni en comparación con los rebaños pequeños. Los rebaños medianos también fueron más propensos a vacunar a las novillas y terneros lactantes contra la enfermedad clostridial, a los terneros destetados contra M. haemolytica y a los terneros lactantes contra H. somni que los rebaños pequeños (Tabla 5). Los terneros destetados tuvieron más probabilidades de ser vacunados contra BVDV, IBR, BRSV, PI3, M. haemolytica +/− P. multocida en rebaños que retuvieron la mayoría de sus terneros durante más de 2 meses (Tabla 5). Los rebaños que eran estrictamente comerciales tenían menos probabilidades de vacunar a los terneros destetados contra el BVDV y al ganado reproductor contra la campilobacteriosis genital bovina y la leptospirosis que los rebaños que contenían algunas semillas (Tabla 5).
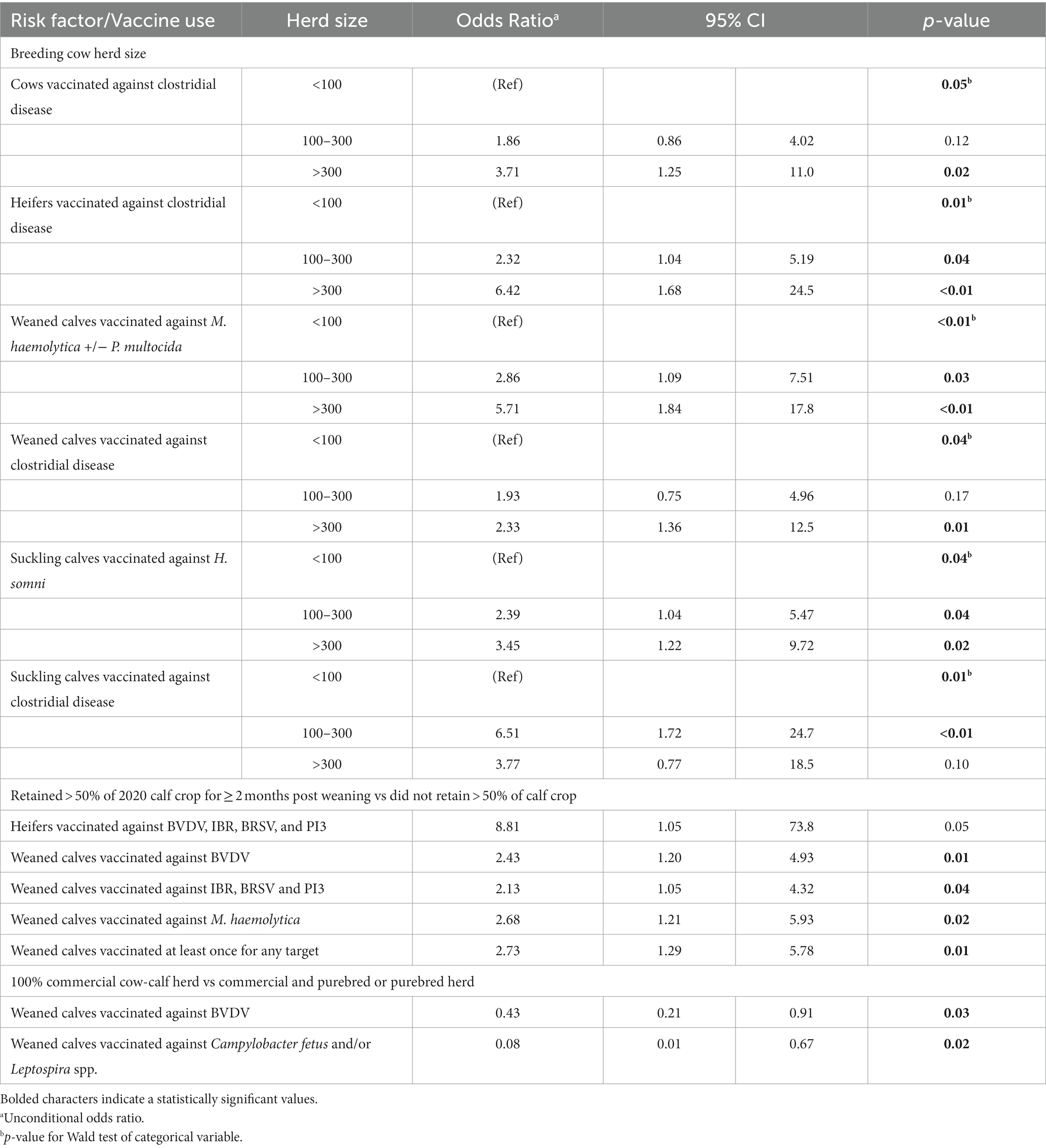 Tabla 5. Resumen de las asociaciones incondicionales entre el tamaño del rebaño de vacas reproductoras, la retención de terneros y el tipo de operación sobre el uso de vacunas en rebaños canadienses de vacas y terneros (n = 131).
Tabla 5. Resumen de las asociaciones incondicionales entre el tamaño del rebaño de vacas reproductoras, la retención de terneros y el tipo de operación sobre el uso de vacunas en rebaños canadienses de vacas y terneros (n = 131).
Los rebaños que comenzaron a parir en febrero y marzo tuvieron menos probabilidades de vacunar a los terneros destetados contra BVDV, IBR, BRSV y PI3 que los rebaños que comenzaron a parir en enero (Tabla 6). Los rebaños que parieron más tarde en la primavera (abril y mayo) tenían menos probabilidades de vacunar a las vacas contra los criadores de terneros en comparación con los que parieron en enero. Finalmente, los rebaños que parieron en marzo tenían más probabilidades de administrar vacunas IBR/BRSV/PI3 a los terneros lactantes, en comparación con los que parieron en enero (Tabla 6).
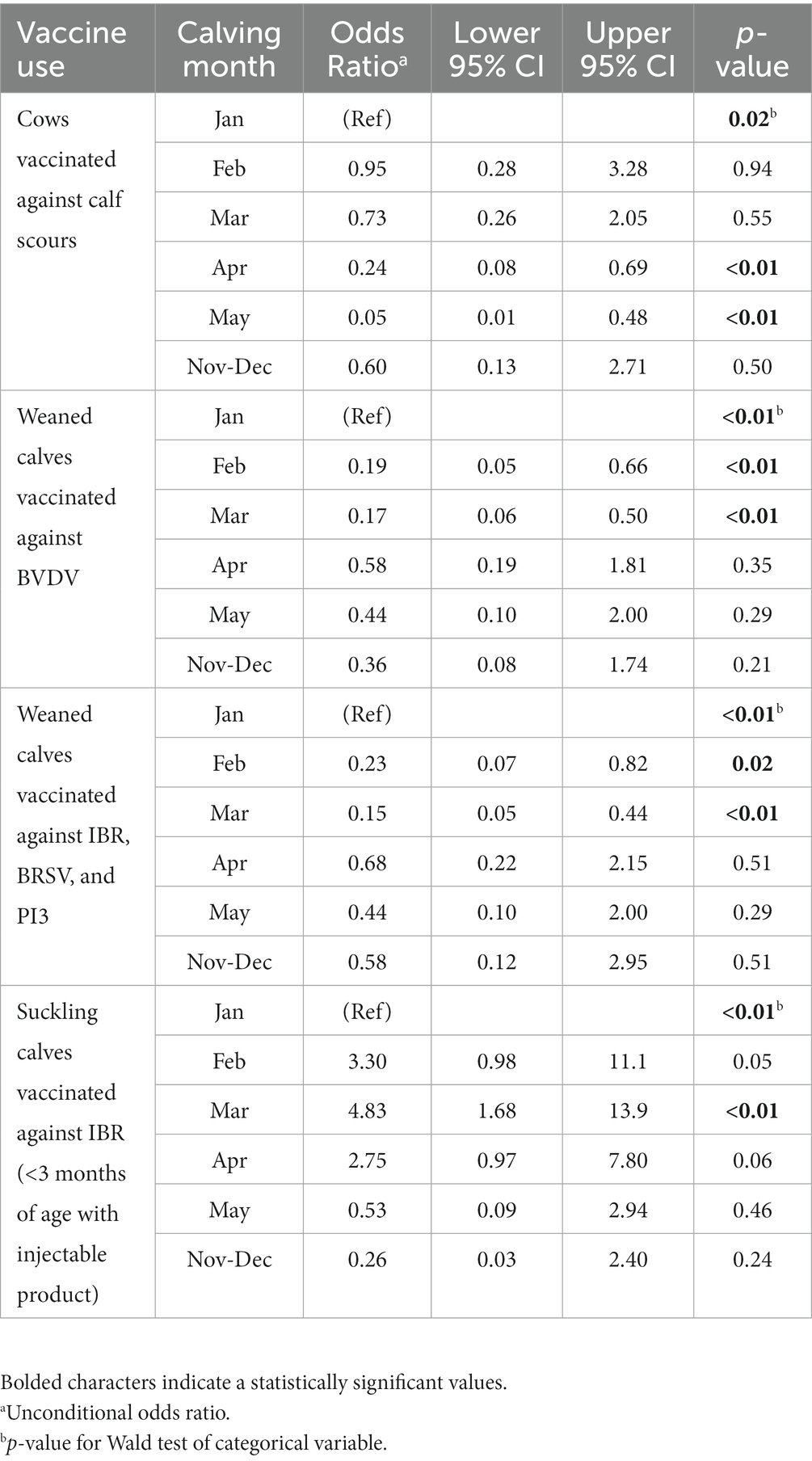 Tabla 6. Asociaciones incondicionales entre el mes de parto y el uso de la vacuna en rebaños canadienses de vacas y terneros (n = 131).
Tabla 6. Asociaciones incondicionales entre el mes de parto y el uso de la vacuna en rebaños canadienses de vacas y terneros (n = 131).
3.5. Tendencias regionales de vacunación
En general, las prácticas de vacunación informadas fueron consistentes entre los rebaños orientales y occidentales con algunas diferencias (Tabla 7). Los rebaños occidentales eran sustancialmente más propensos a administrar vacunas clostridiales a todas las clases de ganado. Los rebaños orientales tenían más probabilidades de vacunar a las vacas contra M. haemolytica +/− P. multocida, pero solo 1 rebaño occidental y 4 orientales informaron el uso de esta vacuna. Mientras que el 44% de los productores occidentales administraron vacunas contra la podredumbre a sus toros, los rebaños orientales no informaron el uso de esta vacuna. Los productores occidentales tenían más probabilidades de vacunar a los terneros antes o después del destete contra M. haemolytica y P. multocida, y a los terneros lactantes para H. somni que los productores orientales. El treinta y uno por ciento de los rebaños occidentales (28/91) y el 38% de los rebaños orientales (15/40) administraron al menos una vacuna IN IBR/BRSV/PI3 a los terneros antes del destete.
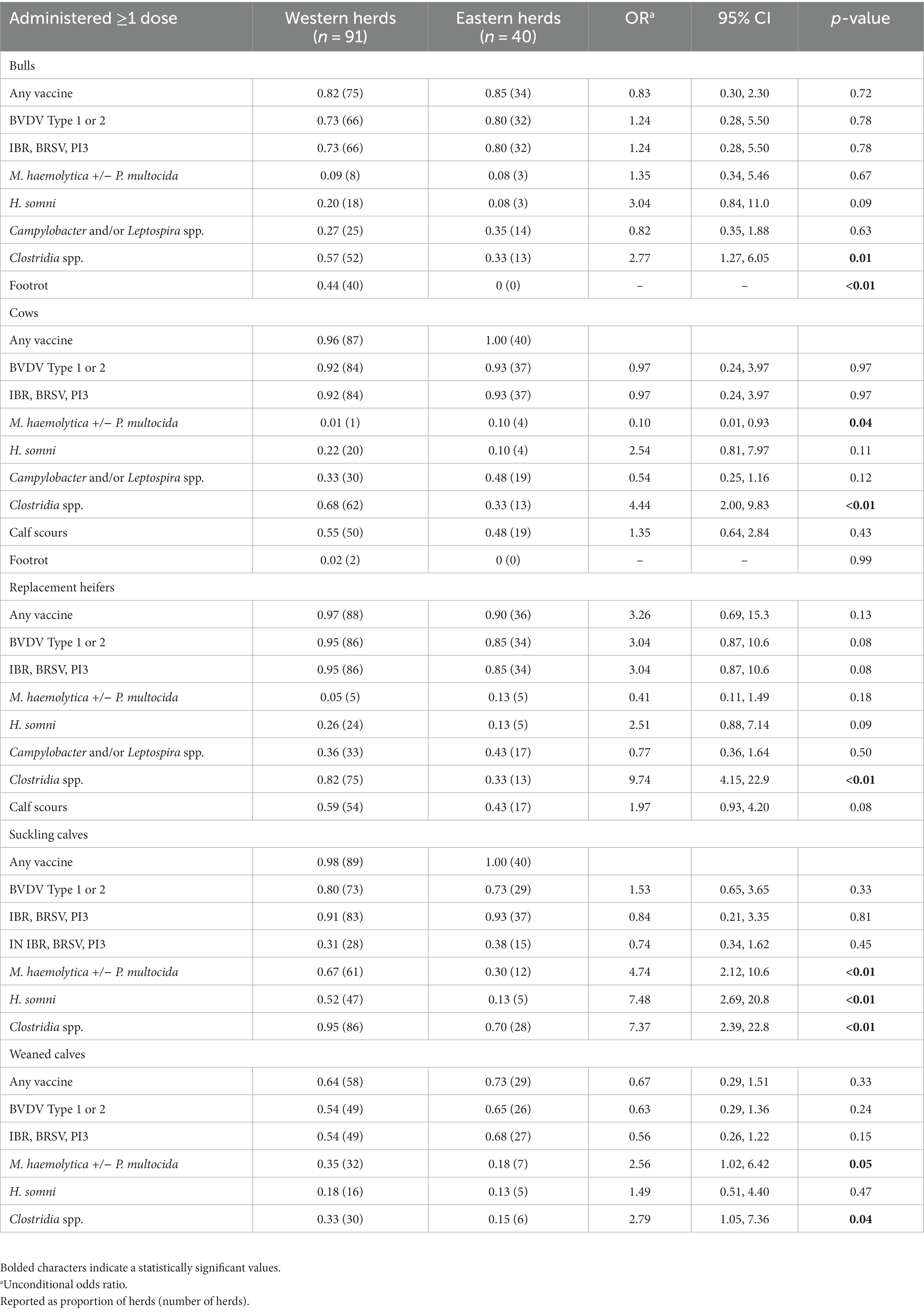 Tabla 7. Diferencia relativa entre las regiones occidental y oriental de Canadá y las vacunas utilizadas en los rebaños de vacas y terneros.
Tabla 7. Diferencia relativa entre las regiones occidental y oriental de Canadá y las vacunas utilizadas en los rebaños de vacas y terneros.
3.6. Motivaciones para el uso de la vacuna
Los tres factores principales que los productores consideraron al decidir qué vacunas usar en sus operaciones fueron la importancia de la enfermedad en el rebaño, los beneficios económicos del uso de la vacuna y el potencial para minimizar la tasa de tratamiento y el uso de antimicrobianos (Tabla 8). Dieciocho productores (14%) identificaron de forma independiente el consejo de su veterinario como uno de los principales factores influyentes en la elección de la vacuna. Las tres razones principales del productor para elegir si vacunar a los terneros lactantes fueron la conveniencia, la necesidad de mano de obra adecuada para manejar a los terneros y los antecedentes de problemas de salud de los terneros (Tabla 8).
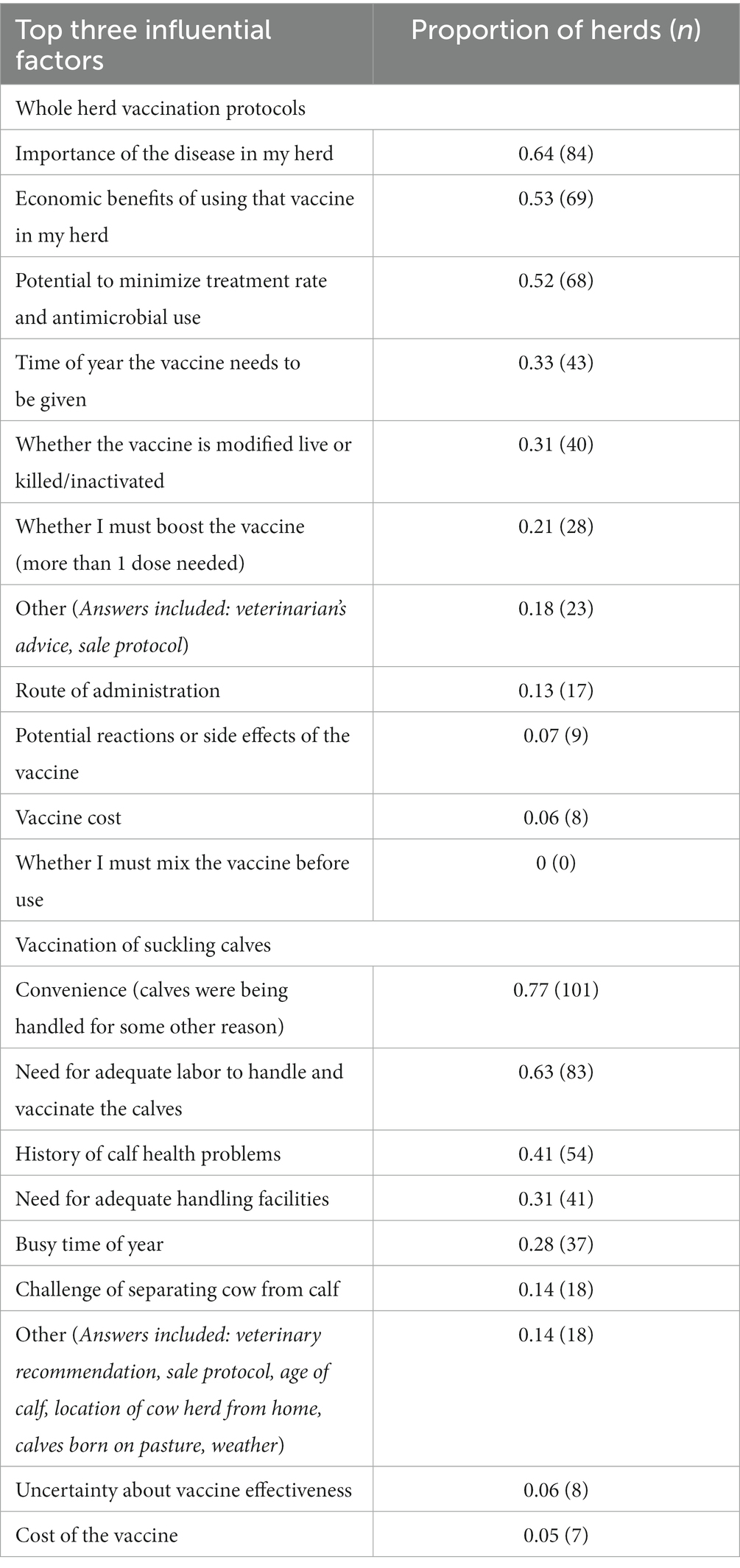 Tabla 8. Resumen de los tres principales factores de los productores canadienses de vacas y terneros que influyen en sus decisiones sobre los protocolos de vacunación de todo el rebaño y si vacunar a los terneros lactantes (n = 131).
Tabla 8. Resumen de los tres principales factores de los productores canadienses de vacas y terneros que influyen en sus decisiones sobre los protocolos de vacunación de todo el rebaño y si vacunar a los terneros lactantes (n = 131).
3.7. Uso de vacunas y asociaciones con la productividad de terneros y el embarazo en hembras reproductoras
Las tasas de morbilidad, tratamiento y mortalidad de terneros estaban disponibles para 124 de los 131 rebaños en esta cohorte y se examinó el uso de la vacuna para determinar su asociación con estos resultados (Tabla 9). Los rebaños que vacunaron a los terneros lactantes contra la enfermedad clostridial tuvieron un menor riesgo de mortalidad de terneros, y los rebaños que vacunaron contra BVDV y M. haemolytica (+/- P. multocida), tuvieron un mayor riesgo de neumonía en terneros. No se encontraron asociaciones entre el uso de la vacuna y el riesgo de diarrea de terneros o no embarazo en hembras reproductoras.
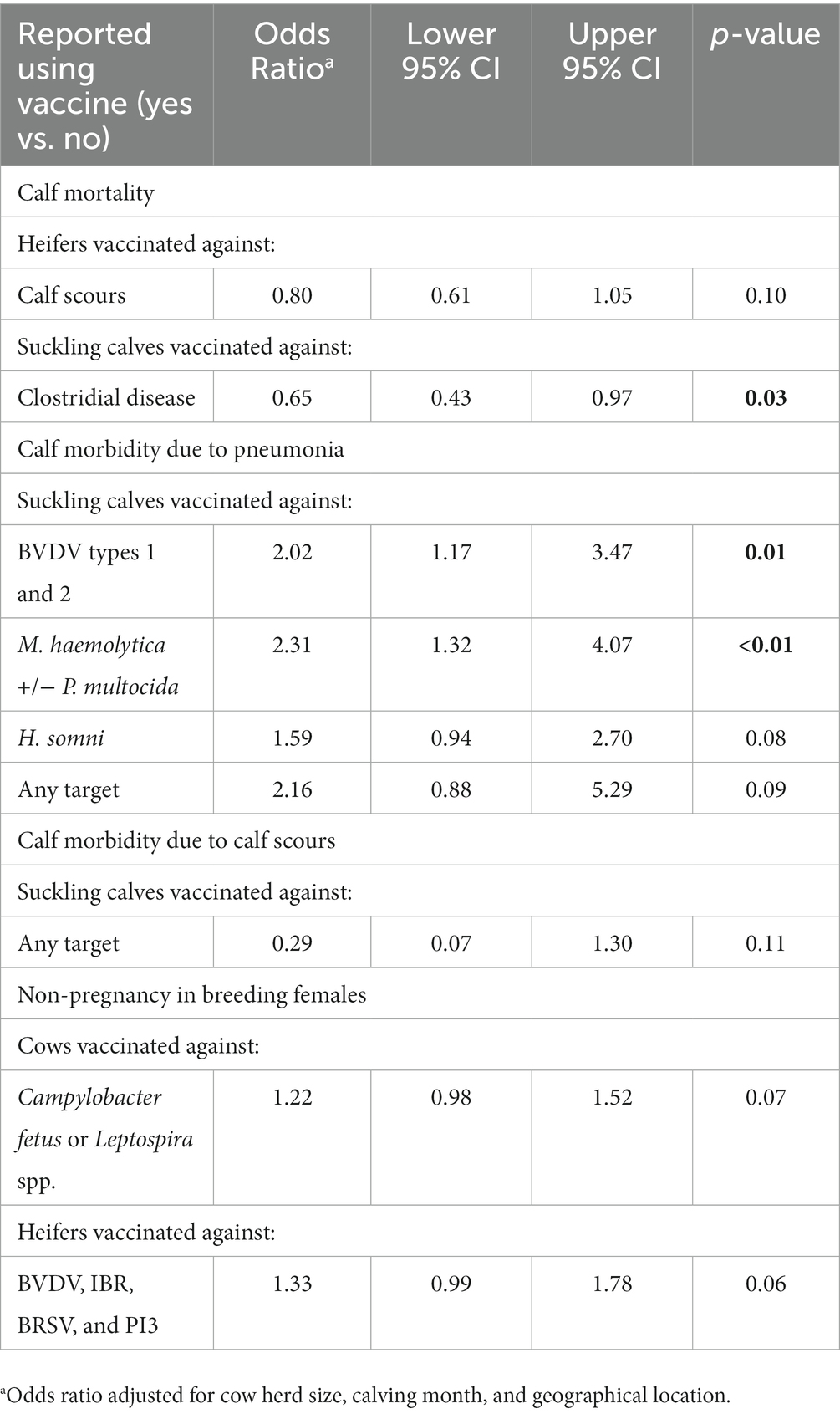 Tabla 9. Asociaciones (p < 0,20) entre el estado de vacunación y la mortalidad de terneros, la morbilidad de terneros y las hembras reproductoras no preñadas (n = 124).
Tabla 9. Asociaciones (p < 0,20) entre el estado de vacunación y la mortalidad de terneros, la morbilidad de terneros y las hembras reproductoras no preñadas (n = 124).
4. Discusión
Este documento presenta la primera imagen detallada de las prácticas de uso de vacunas en rebaños de vacas y terneros de todo Canadá. Las diferencias en el uso de vacunas entre los rebaños orientales y occidentales fueron limitadas. Las diferencias identificadas en la vacunación clostridial se hicieron eco de informes anteriores en los que los rebaños en Ontario tenían menos probabilidades de usar vacunas clostridiales que los rebaños occidentales (25, 33). Si bien las diferencias regionales en algunas vacunas pueden deberse al tamaño del rebaño, las instalaciones y la disponibilidad de mano de obra, el riesgo de enfermedades clostridiales es omnipresente en todo el país.
La vacunación del rebaño de vacas fue mayor en comparación con los informes de 2015/2016 de las provincias orientales (18-20%), pero fue similar a los informes del mismo año de las provincias occidentales (25, 33). La mayoría de los productores vacunaron a sus vacas contra virus asociados con enfermedades respiratorias y reproductivas; Sin embargo, todavía hay rebaños en los que estas vacunas no se utilizan. Menos de un tercio de los productores vacunados contra Campylobacter y el 35% de los rebaños vacunados contra Leptospira. Los productores que usaron pastos comunitarios tenían más probabilidades de vacunar a las vacas contra Campylobacter que aquellos que no lo hicieron. La revacunación anual de Campylobacter y Leptospira no se considera vacunas básicas por la Asociación Americana de Profesionales Bovinos, pero se recomiendan para rebaños considerados de alto riesgo de cualquiera de estas infecciones debido a desafíos de bioseguridad, que combinan pastos comunitarios o ubicación geográfica (19, 20). Waldner et al. informaron tendencias similares de vacunación para BVDV en vacas, pero niveles más altos de vacunas respiratorias bacterianas en vacas (39).
La vacunación de toros fue menos común que para vacas y novillas de reemplazo y continúa presentando una oportunidad de mejora. Comúnmente, los toros fueron vacunados contra BVDV, IBR, BRSV, PI3, patógenos clostridiales, podredumbre (Fusobacterium) y Leptospira spp. La mayoría de los productores siguieron las prácticas recomendadas y vacunaron a los toros antes de la cría. Según una encuesta de veterinarios de ganado de carne de Estados Unidos y Canadá, el 79% recomendó vacunar a los toros al mismo tiempo que el rebaño de vacas (19). La proporción de productores occidentales que vacunaron toros para al menos un objetivo fue similar a un estudio de 2016 (25); sin embargo, la proporción que se vacunó contra BVDV, IBR, PI3, BRSV, campilobacteriosis genital bovina y enfermedades clostridiales pareció ser moderadamente mayor. En comparación con los rebaños del este de Canadá en 2015/2016, la vacunación general de toros fue mayor en un 15-24% (33). Fue más común que los rebaños canadienses administraran una o más vacunas a los toros (83%) que los rebaños de vacas y terneros estadounidenses encuestados en 2016 (44%) (40).
Si bien las vacunas clostridiales se consideran una vacuna básica para los toros, solo el 47% de los productores vacunaron a sus toros durante 2020 (20). Algunos productores están potencialmente aumentando las vacunas clostridiales cada 2 o más años en lugar de vacunar anualmente. Por lo tanto, esta encuesta podría haber pasado por alto los rebaños donde 2020 fue un año «apagado» para las vacunas clostridiales. El uso de la vacuna clostridial fue solo modestamente mayor en las vacas. Aunque la mayoría de las prácticas de vacunación de novillas de reemplazo fueron similares a las notificadas para las vacas, la proporción de rebaños que informaron el uso de la vacuna clostridial fue mayor para las novillas que para las vacas. Esto podría reflejar protocolos de vacunación anual más consistentes para las novillas. Si bien no todos los rebaños informan el uso anual de vacunas clostridiales, todas las vacunas clostridiales aprobadas para su uso en Canadá recomiendan la revacunación anual en ganado adulto de carne. La vacunación semestral con estos productos es una recomendación fuera de etiqueta.
Las novillas de reemplazo fueron vacunadas más comúnmente que las vacas y los toros para todas las demás vacunas básicas, y estas se administraron casi exclusivamente como vacunas MLV, antes de la reproducción. A ninguna novilla de esta cohorte de rebaños se le administró una vacuna MLV BVDV/IBR/BRSV/PI3 en las pruebas de embarazo sin al menos una vacunación previa del mismo tipo. Más de 9 de cada 10 productores que usaron MLV en las pruebas de embarazo proporcionaron dos dosis previas a sus novillas según lo recomendado por al menos una vacuna comercial de uso común (38). Esta es una buena indicación de que muchos productores son conscientes de los riesgos potenciales de las vacunas MLV y las recomendaciones de la etiqueta para el uso adecuado (20). Sin embargo, mientras que más novillas de reemplazo que vacas fueron vacunadas para scours o patógenos de diarrea de terneros, menos de la mitad recibió la segunda dosis recomendada por las etiquetas de los productos.
La vacunación de terneros lactantes y destetados contra al menos un patógeno ha aumentado desde informes anteriores de rebaños del oeste de Canadá y el norte de Ontario y Quebec (25, 34). Los beneficios potenciales de vacunar a los terneros lactantes contra los patógenos BRD, particularmente para los rebaños con antecedentes de BRD, probablemente influyeron en las elecciones de vacunas (30). Muchos productores identificaron la «importancia de la enfermedad en el rebaño» como un factor influyente al determinar los protocolos de vacunación. Las vacunas más comunes administradas a los terneros fueron las vacunas básicas recomendadas por el AABP (BVDV, IBR, BRSV, PI3 y vacunas clostridiales) (20).
Las vacunas vivas modificadas se utilizaron casi exclusivamente en terneros para todos los objetivos virales. La mayoría (90-93%) de los veterinarios de ganado vacuno de América del Norte encuestados recomendaron el uso de vacunas MLV en terneros antes y después del destete (19). Según informes anteriores de rebaños occidentales, las vacunas vivas modificadas contra el BVDV se usaron exclusivamente tanto en terneros lactantes como en terneros destetados (25). No se ha notificado el uso de vacunas diferenciadas por tipo (MLV o inactivadas/muertas) en las provincias orientales.
En comparación con los puntos de referencia de vacunación de rebaños de vacas y terneros occidentales notificados en 1997 y 1998, el panorama actual de vacunación es irreconocible (41). El enfoque de la vacunación de terneros se ha desplazado a las enfermedades respiratorias. En comparación con 1997/98, la vacunación de terneros en 2020 fue mayor para todos los objetivos notificados, excepto para P. multocida. Esto incluye BVDV (↑ 53%), IBR (↑49%), PI3 (↑54%), BRSV (↑62%) y H. somni (↑7%) (41). En comparación con los rebaños del oeste de Canadá en 2016, la proporción de rebaños a los que se administró una dosis a los terneros lactantes fue de una proporción similar; La vacunación IBR, BRSV y PI3 fue mayor (7%), mientras que la vacunación contra el BVDV fue ligeramente menor (4%), pero la proporción de productores que impulsaron terneros antes del destete fue mayor para todos los objetivos respiratorios virales (4-13%) (25). Esto probablemente se atribuye al mayor uso de vacunas respiratorias intranasales, que no contienen BVDV. El uso de vacunas respiratorias virales intranasales al nacer (21%) fue mayor en comparación con informes anteriores para el oeste de Canadá (9%), Ontario (12%) y Canadá Atlántico (14%) (25, 32, 33). En comparación con las vacunas parenterales, se ha demostrado que las vacunas respiratorias intranasales administradas en terneros jóvenes producen una mejor respuesta de cebado inmune frente a los anticuerpos maternos (13, 14, 42, 43). La protección proporcionada por las vacunas respiratorias intranasales puede ser impredecible y a corto plazo (44).
Antes del destete, el 47% de los rebaños aumentaron las vacunas IBR/BRSV/PI3, pero menos del 20% aumentaron las vacunas clostridiales. La mayoría de las vacunas IBR/BRSV/PI3 y clostridial disponibles comercialmente aprobadas para su uso en terneros canadienses requieren una segunda dosis después de la vacunación inicial. Los terneros de los rebaños que recibieron una vacuna IBR/BRSV/PI3 iniciales antes de los 3 meses de edad tenían más probabilidades de recibir una segunda vacuna antes del destete.
Los productores identificaron la «conveniencia (los terneros estaban siendo manejados por otra razón)» como el factor principal que influyó en su decisión de vacunar a los terneros lactantes. La falta de mano de obra, tiempo, acceso a las instalaciones, el clima o el deseo de minimizar el estrés de manejo podrían haber contribuido a un aumento limitado de la vacuna en los terneros lactantes. Además, debido a la falta de incentivos de preacondicionamiento para los productores canadienses, el mayor retorno económico de la optimización de la protección debido a la vacunación no es visto por el productor de vacas y terneros, sino más bien por el corral de engorde. La vacunación antes del destete como parte de un programa de preacondicionamiento ha demostrado reducir la incidencia de enfermedades respiratorias y aumentar la ganancia diaria promedio en el corral de engorde (26, 27).
Las vacunas respiratorias bacterianas, incluidas M. haemolytica y P. multocida, fueron menos comunes que las vacunas respiratorias virales, lo que se espera ya que estas vacunas se consideran «basadas en el riesgo» y se recomiendan en una concentración individual (20). La mayoría de los rebaños administraron esta vacuna después de las 2 semanas de edad y antes del destete. Las recomendaciones de los veterinarios bovinos norteamericanos encuestados para el mejor momento de la vacunación inicial contra M. haemolytica fueron inconsistentes; Los tiempos recomendados fueron en la marca (45%), antes del destete (77%) y después del destete (49%) (19).
La aparente asociación entre la vacunación de terneros lactantes contra BVDV o M. haemolytica y un mayor riesgo de neumonía en terneros lactantes es consistente con encuestas previas de rebaños del oeste de Canadá que informaron que los terneros vacunados para BRD cerca del nacimiento tenían más probabilidades de ser tratados para BRD (39). Como se señaló anteriormente, los productores informaron haber usado vacunas en respuesta a la importancia de la enfermedad en sus rebaños. Esta asociación probablemente se explica por este factor, por el cual los rebaños con un problema de enfermedad respiratoria histórico o en curso tenían más probabilidades de usar estas vacunas. Además, en el 20% de los rebaños del estudio actual, estas vacunas se administraron por primera vez después de los 3 meses de edad después y después del primer riesgo máximo de enfermedad respiratoria (39).
Por el contrario, si bien el riesgo reducido de mortalidad de terneros en terneros lactantes que fueron vacunados contra la enfermedad clostridial podría reflejar el éxito de la vacuna, el uso de la vacuna también podría reflejar el manejo general del rebaño. Un estudio anterior del oeste de Canadá informó los beneficios potenciales de vacunar a las vacas contra enfermedades clostridiales y la posterior protección del cultivo de terneros, y aunque las vacunas clostridiales generalmente se reconocen como altamente efectivas, este es el primer informe específico de los rebaños de carne canadienses que documenta una asociación beneficiosa con el uso (5).
La tasa de respuesta de la encuesta fue ligeramente inferior a la encuesta de vacas y terneros del oeste de Canadá de 2016 (88% frente a 81%) y podría haberse visto afectada por las graves presiones relacionadas con la sequía ejercidas particularmente sobre los productores occidentales en 2021 durante la recopilación de la encuesta (25). Debido a los criterios para ser inscritos en el estudio, este grupo de productores probablemente representa un subconjunto progresivo de productores y podría no reflejar a todos los productores canadienses de terneros. Esta cohorte de productores representa los primeros en adoptar prácticas innovadoras y, por lo tanto, son potencialmente una sobrerrepresentación del uso de vacunas en el rebaño promedio canadiense de vacas y terneros. Se desconoce si las respuestas a la encuesta o las tasas generales de vacunación se vieron afectadas por la pandemia de COVID-19 o si las decisiones de gestión se vieron afectadas negativamente por la vacilación de la vacuna en torno a las vacunas respiratorias virales. Si bien las encuestas sufren de sesgo de recuerdo, a los productores se les proporcionaron fotos en color y un libro para ayudarlos a encontrar el nombre de los productos utilizados si no tenían acceso a recibos o registros. La clasificación errónea también se solucionó pidiendo a los productores que informaran el nombre comercial real del producto utilizado a partir de sus recibos y registros en lugar de preguntarles contra qué enfermedades vacunaron. Luego, el equipo del estudio volvió a codificar los nombres comerciales para capturar los componentes de la vacuna.
El uso de vacunas en todo Canadá ha mostrado una mejora significativa en las últimas décadas. Los productores de vacas y terneros generalmente siguieron los protocolos de vacunación recomendados para todas las vacunas básicas. El número de rebaños que vacunaron animales aumentó para casi todos los grupos de ganado desde informes anteriores. Un cambio notable es el aumento del uso de vacunas respiratorias intranasales, específicamente en terneros neonatales. Si bien se han realizado muchos cambios positivos en la industria, todavía hay algunas áreas en las que se necesita mejorar. Se debe alentar a los productores a vacunar a los terneros contra enfermedades respiratorias antes de los 3 meses de edad, en consulta con su veterinario, para permitir más tiempo para que la vacuna tenga un efecto antes de los períodos de alto riesgo para la enfermedad y para dar tiempo para administrar una segunda dosis antes del destete. La literatura es escasa en cuanto a los beneficios relativos de la vacunación mucosa de terneros cerca del momento del nacimiento, así como para el tipo óptimo de vacunación de seguimiento. Recientemente, varios proyectos que observan el refuerzo sistémico primario de la mucosa han encontrado un beneficio para el cebado de la mucosa de los recién nacidos que es variable según el patógeno y la forma de vacuna de refuerzo utilizada; se ha encontrado un beneficio para el refuerzo primario y sistémico de la mucosa para BRSV, coronavirus bovino y BVDV (14-16, 18). Se ha demostrado que el refuerzo primario y sistémico de la mucosa de los terneros neonatos mejora las concentraciones de anticuerpos neutralizantes y específicos del virus y sus respuestas de refuerzo para BRSV, BCoV y BVDV. También se ha observado una mejor protección contra la enfermedad cuando los terneros preparados y potenciados fueron desafiados con BRSV o BVDV tipo 2 (16, 18). Se necesita más investigación sobre los beneficios relativos de vacunar a los terneros cerca del momento del nacimiento y el momento óptimo de un refuerzo para minimizar los riesgos de enfermedades respiratorias asociadas con el estrés y el aumento de la densidad animal durante actividades como la inseminación artificial (24, 39, 42).
Si bien se examinaron todas las clases de ganado, este estudio aporta información única sobre los tipos, el momento y el número de dosis de vacunas utilizadas en terneros lactantes de una cohorte de rebaños de propiedad privada. Si bien los participantes probablemente representan un subconjunto relativamente progresivo de productores, más productores informaron haber vacunado a terneros lactantes para BRD en comparación con trabajos anteriores en cohortes similares. Los resultados muestran que las altas tasas de adopción para la vacunación previa al destete es un objetivo razonable para los rebaños comerciales de vacas y terneros. Sin embargo, hubo muy poca consistencia en los protocolos de vacunación para los terneros lactantes, destacando las oportunidades para optimizar el momento de la vacunación para los desafíos específicos de cada operación, como el momento de la temporada de parto y las limitaciones de recursos. Además, los protocolos pueden variar dependiendo de si el objetivo principal de la vacunación de terneros es reducir la enfermedad después del destete, o en terneros lactantes antes o después de la participación en los pastos de verano.
Para mejorar la eficacia de la vacuna, los productores deben seguir adecuadamente las instrucciones de las etiquetas del producto, específicamente con respecto a la administración de dosis de refuerzo dentro del período especificado. Este problema fue más evidente para las vacunas clostridiales en vacas y toros, y las vacunas de lavado en novillas criadas. Los incentivos económicos para que los productores vacunen a los terneros antes de la entrada en el corral de engorde deben ser una prioridad para la industria para garantizar la sostenibilidad a largo plazo de la producción de carne de res canadiense. Todavía hay un pequeño porcentaje de productores de vacas y terneros que no están utilizando las vacunas virales básicas para quienes podrían ser necesarias actividades específicas de transferencia de tecnología. Finalmente, las vacunas clostridiales están subutilizadas en vacas y toros, particularmente en rebaños orientales. Estas vacunas deben administrarse anualmente para garantizar que el ganado esté completamente protegido y una transferencia clostridial óptima de anticuerpos.
Declaración de disponibilidad de datos
Los conjuntos de datos presentados en este artículo no están fácilmente disponibles porque la información fue proporcionada por los participantes del estudio bajo la restricción de que solo se compartirían los datos resumidos. Esto se incluye en los cuadros y cifras detallados que figuran en el presente documento. Las solicitudes para acceder a los conjuntos de datos deben dirigirse a cheryl.waldner@usask.ca.
Declaración ética
Los estudios con humanos fueron aprobados por la Junta de Ética de Investigación del Comportamiento de la Universidad de Saskatchewan. Los estudios se realizaron de acuerdo con la legislación local y los requisitos institucionales. Los participantes dieron su consentimiento informado por escrito para participar en este estudio.
Contribuciones del autor
CW diseñó la herramienta de estudio y encuesta. CW y ML recodificaron los datos y completaron los análisis estadísticos. ML escribió el manuscrito. CW, NE, JC y SG editaron, revisaron y proporcionaron comentarios sobre el manuscrito. Todos los autores contribuyeron al artículo y aprobaron la versión presentada.
Financiación
Financiación proporcionada por el Consejo de Investigación de Ganado de Carne.
Reconocimientos
Los autores desean agradecer la ayuda de Sharlene April en la gestión de la distribución de la encuesta y la entrada de datos para este proyecto. Los autores también agradecieron a los productores de vacas y terneros que participaron en la Red Canadiense de Vigilancia de Vacas y Terneros.
Conflicto de intereses
Los autores declaran que la investigación se llevó a cabo en ausencia de cualquier relación comercial o financiera que pudiera interpretarse como un posible conflicto de intereses.
Nota del editor
Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, o las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo, o reclamo que pueda ser hecho por su fabricante, no está garantizado ni respaldado por el editor.
Referencias
1. Newcomer, BW, Chamorro, MF, and Walz, PH. Vacunación del ganado contra el virus de la diarrea viral bovina. Veterinario Microbiol. (2017) 206:78–83. doi: 10.1016/j.vetmic.2017.04.003
2. Recién llegado, BW, Cofield, LG, Walz, PH y Givens, MD. Prevención del aborto en bovinos después de la vacunación contra el herpesvirus bovino 1: un metanálisis. Prev Vet Med. (2017) 138:1–8. doi: 10.1016/j.prevetmed.2017.01.005
Resumen de PubMed | Texto completo de CrossRef | Google Académico
3. Sanhueza, JM, Wilson, PR, Benschop, J, Collins-Emerson, JM y Heuer, C. Meta-análisis de la eficacia de las vacunas contra Leptospira Serovar Hardjo para prevenir la excreción urinaria en el ganado. Prev Vet Med. (2018) 153:71–6. doi: 10.1016/j.prevetmed.2018.02.015
Resumen de PubMed | Texto completo de CrossRef | Google Académico
4. Waldner, C . Atributos de la vaca, manejo del rebaño y eventos de historia reproductiva asociados con el aborto en rebaños de vacas y terneros del oeste de Canadá. Teriogenología. (2014) 81:840–8. doi: 10.1016/j.theriogenology.2013.12.016
Resumen de PubMed | Texto completo de CrossRef | Google Académico
5. Waldner, C, Jelinski, M, y McIntyre-Zimmer, K. Survey of Western Canadian beef producers regarding tern-Hood diseases, management practices, and veterinary service usage. Can Vet J. (2013) 54:599–64.
6. Waldner, CL, and Garcia, GA. Cow attributes, herd management, and reproductive history events associated with the risk of nonpregnancy in cow-ternf hats in Western Canada. Teriogenología. (2013) 79:1083–94. doi: 10.1016/j.theriogenology.2013.02.004
Resumen de PubMed | Texto completo de CrossRef | Google Académico
7. Newcomer, BW, Walz, PH, Givens, MD y Wilson, AE. Eficacia de la vacunación contra el virus de la diarrea viral bovina para prevenir enfermedades reproductivas: un metanálisis. Teriogenología. (2015) 83:360–5.e1. doi: 10.1016/j.theriogenology.2014.09.028
8. Troxel, TR, Burke, GL, Wallace, WT, Keaton, LW, McPeake, SR, Smith, D, et al. Eficacia de la vacunación clostridial para estimular y mantener una respuesta inmune en vacas y terneros. J Anim Sci. (1997) 75:19–25. doi: 10.2527/1997.75119x
Resumen de PubMed | Texto completo de CrossRef | Google Académico
9. Capik, SF, Moberly, HK y Larson, RL. Revisión sistemática de la eficacia de la vacuna contra Mannheimia Haemolytica, Pasteurella Multocida e Histophilus Somni en bovinos norteamericanos. El practicante bovino. (2021) 55:125–33. doi: 10.21423/bovino-vol55no2p125-133
10. Woolums, A editor. Manejo inmunológico y vacunación del ternero de ternera predestetado. En: American Association of Bovine Practitioners 54th Annual Conference Proceedings. Salt Lake City, Utah: Ciencia con práctica (2021).
11. Gow, S, Waldner, C, y Ross, C. El efecto de la duración del tratamiento sobre los pesos de destete en un rebaño de vacas y terneros con un brote severo prolongado de diarrea en terneros. Can Vet J. (2005) 46:418-23–25-6.
12. Maier, GU, Breitenbuecher, J, Gomez, JP, Samah, F, Fausak, E, and Van Noord, M. Vaccination for the prevention of neonatal ternera diarrhea in cow-ternf operations: a scoping review. Vet Anim Sci. (2022) 15:100238. doi: 10.1016/j.vas.2022.100238
Resumen de PubMed | Texto completo de CrossRef | Google Académico
13. Erickson, NEN, Ellis, J, Waldner, C, Lardner, H, Gow, S, Campbell, J, et al. Comparación de las respuestas de anticuerpos específicos del virus de la diarrea viral bovina de terneros jóvenes vacunados con regímenes de virus vivos modificados o de virus inactivados. Can Vet J. (2020) 61:871–4.
14. Erickson, NEN, Berenik, A, Lardner, H, Lacoste, S, Campbell, J, Gow, S, et al. Evaluación de las respuestas específicas del virus sincitial respiratorio bovino (BRSV) y el virus del herpes bovino (BHV) entre terneros de carne de vacuno del oeste de Canadá vacunados contra el primer refuerzo heterólogo y homólogo. Can Vet J. (2021) 62:37–44.
15. Erickson, NEN, Lacoste, S, Sniatynski, M, Waldner, C, and Ellis, J. Comparison of virus neutralizing and virus specific Elisa antibody responses among bovine neonates differentially primed and boosted against bovine coronavirus. Can Vet J. (2023) 64:321–8.
16. Erickson, NEN, Godson, D, Gow, S, Lacoste, S, Waldner, C, and Ellis, J. Comparative efficacy of modified-live and inactivated vaccines in boost disease-sparing responses to bovine viral diarrhea virus challenge in Neonatally Mucosally primed weanling beef terneros. Can Vet J. (2023) 64:321–8.
17. Martínez, DA, Newcomer, B, Passler, T, y Chamorro, MF. Eficacia de las vacunas contra el virus respiratorio sincitial bovino para reducir la morbilidad y la mortalidad en terneros dentro de modelos experimentales de infección: una revisión sistemática y metanálisis. Front Vet Sci. (2022) 9:906636. DOI: 10.3389/fvets.2022.906636
Resumen de PubMed | Texto completo de CrossRef | Google Académico
18. Ellis, J, Gow, S, Berenik, A, Lacoste, S, and Erickson, N. Comparative efficacy of modified-live and inactivated vaccines in boost responses to bovine respiratory syncytial virus following neonatal mucosal priming of beef terneros. Can Vet J. (2018) 59:1311–9.
19. Fike, GD, Simroth, JC, Thomson, DU, Schwandt, EF, Spare, R, y Tarpoff, AJ. Una encuesta de las prácticas recomendadas realizadas por los veterinarios para las operaciones de vacas y terneros en los Estados Unidos y Canadá. Prof. Anim Sci. (2017) 33:716–28. DOI: 10.15232/PAS.2017-01642
Resumen de PubMed | Texto completo de CrossRef | Google Académico
20. Asociación Americana de Practicantes Bovinos . Pautas de vacunación de Aabp Ashland, OH (2021). Disponible en: http://www.aabp.org/committees/resources/VaccGuidelines2021.pdf.
21. WCCCSN . Encuesta de vacas y terneros del oeste de Canadá II Universidad de Saskatchewan (2018). Disponible en: http://westernbeef.org/pdfs/wcccs/WCdnSurveyII_FINAL.pdf.
22. Davidson, TM . Servicios de investigación de Canfax. Beef Cattle Research Council (BCRC): Tasas de adopción de prácticas recomendadas por operadores de vacas y terneros en Canadá (2019).
23. Brault, SA, Hannon, SJ, Gow, SP, Warr, BN, Withell, J, Song, J, et al. Uso de antimicrobianos en 36 corrales de engorde de carne en el oeste de Canadá: 2008-2012. Front Vet Sci. (2019) 6:6. DOI: 10.3389/FVETS.2019.00329
Resumen de PubMed | Texto completo de CrossRef | Google Académico
24. Fossen, JD, Campbell, JR, Gow, SP, Erickson, N, and Waldner, CL. Antimicrobial use in Canadian cow-ternf hats. Veterinario Sci. (2023) 10:50366. DOI: 10.3390/VETSci10050366
Resumen de PubMed | Texto completo de CrossRef | Google Académico
25. Waldner, CL, Parker, S, and Campbell, JR. Vaccine use in Western Canadian cow-ternf herds. Can Vet J. (2019) 60:414–22.
26. Schumaher, TF, Cooke, RF, Brandao, AP, Schubach, KM, de Sousa, OA, Bohnert, DW, et al. Efectos del momento de la vacunación contra patógenos respiratorios sobre el rendimiento, la respuesta de anticuerpos y la salud en el ganado de engorde. J Anim Sci. (2019) 97:620–30. doi: 10.1093/jas/sky466
Resumen de PubMed | Texto completo de CrossRef | Google Académico
27. Lippolis, KD, Cooke, RF, Schubach, KM, Brandao, AP, da Silva, LG, Marques, RS, et al. Alterar el tiempo de vacunación contra patógenos respiratorios para mejorar la respuesta de anticuerpos y el rendimiento del ganado de engorde. J Anim Sci. (2016) 94:3987–95. doi: 10.2527/jas.2016-0673
28. O’Connor, AM, Hu, D, Totton, SC, Scott, N, Winder, CB, Wang, B, et al. Una revisión sistemática y un metaanálisis en red de vacunas bacterianas y virales, administradas al llegar o cerca de la llegada al corral de engorde, para el control de la enfermedad respiratoria bovina en ganado de carne. Anim Health Res Rev. (2019) 20:143–62. doi: 10.1017/s1466252319000288
Resumen de PubMed | Texto completo de CrossRef | Google Académico
29. Larson, RL, y Step, DL. Efectividad basada en la evidencia de la vacunación contra Mannheimia Haemolytica, Pasteurella Multocida e Histophilus Somni en bovinos de engorde para mitigar la incidencia y el efecto del complejo de enfermedades respiratorias bovinas. Veterinario Clin North Am Food Anim Pract. (2012) 28:97-106, E1-7, IX–106.e7. doi: 10.1016/j.cvfa.2011.12.005
Resumen de PubMed | Texto completo de CrossRef | Google Académico
30. Theurer, ME, Larson, RL, y White, BJ. Revisión sistemática y metanálisis de la efectividad de las vacunas disponibles comercialmente contra el herpesvirus bovino, el virus de la diarrea viral bovina, el virus sincitial respiratorio bovino y el virus de la parainfluenza tipo 3 para la mitigación del complejo de enfermedad respiratoria bovina en bovinos. J Am Vet Med Assoc. (2015) 246:126–42. doi: 10.2460/javma.246.1.126
Resumen de PubMed | Texto completo de CrossRef | Google Académico
31. Griffin, CM, Scott, JA, Karisch, BB, Woolums, AR, Blanton, JJ, Kaplan, R, et al. Un ensayo controlado aleatorio para probar el efecto de la vacunación y la desparasitación a la llegada en la salud del ganado ganadero y el rendimiento del crecimiento. Bov Pract (Stillwater). (2018) 33:716–28. DOI: 10.15232/PAS.2017-01642
Resumen de PubMed | Texto completo de CrossRef | Google Académico
32. CAC . Resultados agregados de la encuesta de producción de vacas y terneros del Atlántico. Canadá: Maritime Beef Council (2018).
33. OCC . Ontario cow-ternf 2015/16 production survey (OCC): Universidad de Guelph. (2018) Disponible en: https://www.beefresearch.ca/files/pdf/Ontario%20Cow-Calf%20Summary%20Nov%2012%202018.pdf.
34. Lamothe, S . Soluciones de refugio del norte. Northern Beef Study: Northern Ontario and Northern Quebec Beef Cow-Calf Production (Estudio de carne de vacuno del norte: producción de vacas y terneros del norte de Ontario y el norte de Quebec) (2018).
35. Waldner, CL, Parker, S, and Campbell, JR. Identifying performance benchmarks and determinants for reproductive performance and ternf survival using a longitudinal field study of cow-ternf hats in Western Canada. PLoS One. (2019) 14:E0219901. doi: 10.1371/journal.pone.0219901
Resumen de PubMed | Texto completo de CrossRef | Google Académico
36. Johnson, P, McLeod, L, Campbell, J, Rousseau, M, Larson, K, and Waldner, C. Estimating the sensitivity and specificity of serum Elisa and Pooled and individual fecal PCR for detect Mycobacterium Avium subspecies Paratuberculosis in Canadian cow-ternf hats using Bayesian latent class models. Front Vet Sci. (2022) 9:937141. doi: 10.3389/fvets.2022.937141
Resumen de PubMed | Texto completo de CrossRef | Google Académico
37. Compendio de productos veterinarios – Canada edition beef cattle biological chart (2022). Disponible en: https://zoetis.cvpservice.com/chartindex/main?type=bio.
38. Zoetis, CA . Bovi-shield® oro Fp® 5 10 dosis. Disponible en: https://www2.zoetis.ca/species/bovine/products-and-solutions/bovi-shield-gold-fp-5-10-doses.
39. Waldner, CL, Wilhelm, B, Windeyer, MC, Parker, S, and Campbell, J. Improving beef ternf health: frequency of disease syndromes, uptake of management practices after parving, and potential for antimicrobial use reduction in Western Canadian hats. Transl Anim Sci. (2022) 6:txac151. DOI: 10.1093/tas/txac151
Resumen de PubMed | Texto completo de CrossRef | Google Académico
40. USDA . Beef 2017, «Prácticas de salud y manejo de vacas y terneros en los Estados Unidos, 2017, informe 2». Fort Collins, CO. (2020), #.782–#.1119.
41. Agricultura y desarrollo rural de Alberta . Auditoría de vacas y terneros de Alberta 1997/98 (2001). Disponible en: http://westernbeef.org/pdfs/economics/AB_CowCalf_Audit.pdf.
42. Woolums, AR, Berghaus, RD, Berghaus, LJ, Ellis, RW, Pence, ME, Saliki, JT, et al. Efecto de la edad del ternero y la vía de administración de la vacuna multivalente inicial de virus vivos modificados sobre las respuestas inmunes humorales y mediadas por células después de la administración posterior de una vacuna de refuerzo al destete en terneros de carne. Am J Vet Res. (2013) 74:343–54. doi: 10.2460/ajvr.74.2.343
43. Chamorro, MF, Woolums, A, and Walz, PH. Vaccination of calves against common respiratory viruses in the face of maternally derived antibodies (IFOMA). Anim Health Res Rev. (2016) 17:79–84. doi: 10.1017/S1466252316000013
Palabras clave: vacuna, vaca-ternero, ganado vacuno, control de enfermedades, manejo
Cita: Lazurko MM, Erickson NEN, Campbell JR, Gow S y Waldner CL (2023) Uso de vacunas en rebaños canadienses de vacas y terneros y oportunidades de mejora. Frente. Vet. Sci. 10:1235942. doi: 10.3389/fvets.2023.1235942
Recibido: 07 Junio 2023; Aprobado: 24 de julio de 2023;
Publicado: 09 agosto 2023.
Editado por:
David Renter, Universidad Estatal de Kansas, Estados Unidos
Revisado por:
Robert Larson, Universidad Estatal de Kansas, Estados Unidos Michael Sanderson, Universidad Estatal de Kansas, Estados
Unidos
Derechos de autor © 2023 Lazurko, Erickson, Campbell, Gow y Waldner. Este es un artículo de acceso abierto distribuido bajo los términos de la Licencia de Atribución Creative Commons (CC BY).
*Correspondencia: Cheryl L. Waldner, cheryl.waldner@usask.ca
Renuncia: Todas las afirmaciones expresadas en este artículo son únicamente las de los autores y no representan necesariamente las de sus organizaciones afiliadas, o las del editor, los editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo o reclamo que pueda ser hecho por su fabricante no está garantizado ni respaldado por el editor.
Date de alta y recibe nuestro 👉🏼 Diario Digital AXÓN INFORMAVET ONE HEALTH
Date de alta y recibe nuestro 👉🏼 Boletín Digital de Foro Agro Ganadero
Noticias animales de compañía
Noticias animales de producción
Trabajos técnicos animales de producción
Trabajos técnicos animales de compañía